在一众制药巨头中,衔着金钥匙出生的艾伯维显得独特且年轻。2013年成立之时,艾伯维便凭借修美乐这张王牌在自免市场风生水起,稳居全球药企排行榜前列,市值也是扶摇直上,从最初的180亿美元跃升至2500亿美元左右。
但是站在下一个十年的新起点上,艾伯维也面临着自己的增长难题。如今,修美乐专利到期的“达摩克利斯之剑”已经落下,另一大拳头产品伊布替尼也遭遇了竞品围剿。业绩承压已是不争事实。2023年前3季度,艾伯维总营收400.17亿美元,同比下降6.8%。
如此局面下,艾伯维的一举一动都尤为关键。近期,艾伯维便豪掷百亿美金加码ADC赛道,又斥87亿美元收购补强神经科学管线。回顾这一年,也能看到艾伯维做出了不少调整动作。以外部合作交易和内部管线进展作为串联全局的草蛇灰线,我们或许可以进一步了解艾伯维在进退之间的取舍抉择。
断舍离

今年,艾伯维释放的信号之一是终止了不少外部合作的肿瘤领域项目。
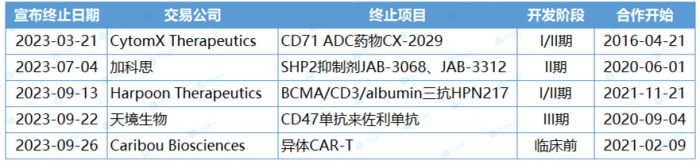
艾伯维2023年终止的合作项目
3月,艾伯维放弃CytomX Therapeutics的CX-2029,它是一款具备first-in-class潜力的CD71靶向条件激活ADC药物。这项合作起始于2016年,7年时间开发进度从临床前推至I/II期,然而并没有转化为惊艳的数据。Ib期研究显示,CX-2029治疗鳞状食管癌的ORR为21%,鳞状非小细胞肺癌(sqNSCLC)的ORR为10%。
7月,艾伯维基于资产组合与战略决策,退回了加科思的SHP2抑制剂JAB-3068和JAB-3312。上一个在SHP2赛道离场的大药厂是赛诺菲。无可否认,SHP2靶点开发前景仍不甚明朗,其单药的治疗效果不理想,与KRAS G12C、EGFR和PD-1等靶点的联合也有待验证。
值得注意的是,在加科思和艾伯维合作的I/IIa期研究(NCT04720976)中,与JAB-3312进行联合应用的无一例外都是别家的产品,比如默沙东的帕博利珠单抗、阿斯利康的奥希替尼等。环视艾伯维的管线,就能发现问题所在——内部明显缺乏成熟的联用搭档。
艾伯维并没有布局KRAS抑制剂,其PD-1单抗budigalimab还处于II期阶段,自身的协同优效尚未得到充分验证,多项budigalimab联合的临床试验已被终止。同样的,艾伯维也没有获批的EGFR产品在手,主要管线为EGFR ADC新药ABBV-637,处于I期阶段。在EGFR抑制剂的升级上,艾伯维试图以ADC技术突围,但ABBV-414、ABBV-221和ABBV-321等多项资产不幸成为试错的垫脚石。
9月,艾伯维先后终止了3项合作,退货名单上再添Harpoon的CD3/BCMA/albumin三抗HPN217、天境生物的CD47单抗来佐利单抗和Caribou的异体CAR-T。结合药物类型和靶点赛道来看,这些管线在当时看来是相当前沿,全球尚无同类产品获批,显示出艾伯维超前的布局眼光。
只是追逐first-in-class创新需要与极大的不确定性博弈。以CD47单抗开发为例,整个领域先是经历了血液毒性的考验,之后先驱者吉利德和ALX Oncology又因疗效不足而终止研究,这给该靶点的成药留下了一个待解谜题。投入产出前景不明之下,艾伯维就不再愿意用有限的资源去押注高风险的产品。
另一款被艾伯维舍弃的HPN217未显示出重大的疗效或安全性问题。I期研究显示,在接受12mg药物治疗的复发/难治性多发性骨髓瘤患者中,总缓解率(ORR)为63%;细胞因子释放综合征(CRS)的发生率为16%(都为1-2级),无神经毒性(ICANS)事件发生。至于艾伯维为何选择退回HPN217,可能与管线中已有的CD3/BCMA双抗ABBV-383不无关系。两者都针对多发性骨髓瘤这一适应症,靶点高度重合。相对来说,双抗的开发技术比三抗成熟,艾伯维所需承受的风险可能也相应小些。
不止是外部合作的调整,艾伯维今年也砍掉了一些内部管线,包括所有囊性纤维化(CF)项目。
一直以来,艾伯维都对CF市场虎视眈眈。2013年,艾伯维牵手Galapagos,正式切入CF领域。彼时,Vertex开发的CF新药依伐卡托已成功上市,它是首款针对CF治病根源的疗法。面对实力不一般的对手,艾伯维没有退却,并希望通过联合疗法进行迭代。
2016年,艾伯维与Galapagos就CF三联疗法开发深化合作。2018年,在两项临床数据不尽如人意的情况下,艾伯维仍以4500万美元的预付款收购了Galapagos的CF管线,包括ABBV-119。ABBV-119联合ABBV-3067、ABBV-2222的应用成为了艾伯维探索的重点,但通过概念验证发现,ABBV-119的补充,并没有在原本的双药方案上实现增效。即便把ABBV-119换成具有全新结构的ABBV-576,也没有达到理想的效果。
至此,艾伯维在CF领域的所有尝试均以失败告终,终止CF项目开发也是别无选择之举。
再进攻

多番断舍离之下,艾伯维剔除了冗余的管线,更加明确了进攻的重点之一——ADC。11月末,艾伯维以101亿美金将ImmunoGen收入麾下,获得了其核心资产索米妥昔单抗。
实际上,艾伯维在ADC赛道的布局早就开始了。2016年,艾伯维便以58亿美元首付款收购了Stemcentrx,囊获了包括靶向DLL3 Rova-T在内的多款产品。
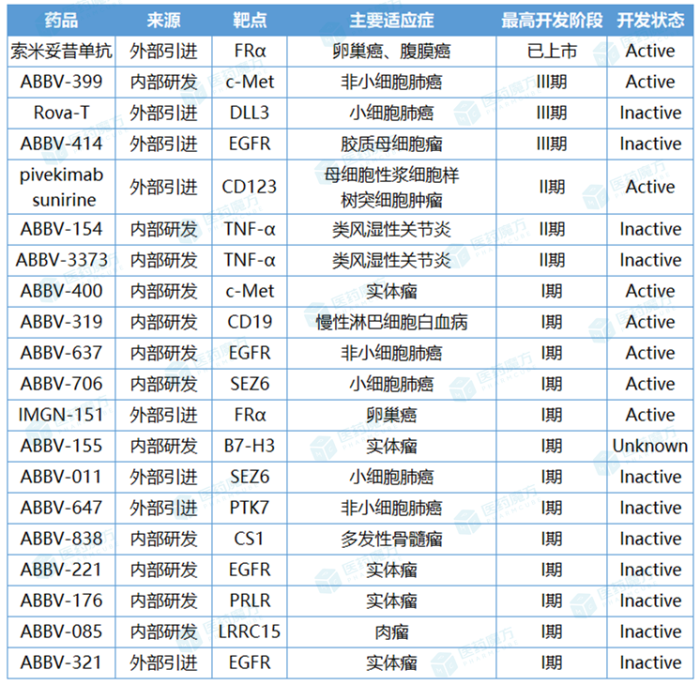
艾伯维主要的ADC产品管线
艾伯维对ADC的看好已经全然体现在产品管线布局中。其ADC药物靶标多种多样,既有围绕成熟靶点的迭代,又有瞄准新兴靶点的探索。在ADC的载荷元素上,艾伯维也玩出了花样,除常见的MMAE、Top I抑制剂外,还尝试了糖皮质激素受体调节剂(GRM)和Bcl-xL抑制剂等。治疗领域也不局限于传统的实体瘤领域,而是大胆延伸到血液瘤和自免领域。
可惜的是,多数项目夭折在了不同的开发阶段,从Stemcentrx收购获得的ADC管线更是几乎都已被证伪。
今年,除退还CD71 ADC药物CX-2029外,艾伯维还陆续砍掉了3条ADC管线,分别是TNF-α靶向的ABBV-154、SEZ6靶向的ABBV-011和PTK7靶向的ABBV-647。管线变动对于跨国大药企而言不足为奇,但这么密集的削减,无疑暴露出艾伯维在ADC赛道的困境。
当然,艾伯维手上仍有筹码,c-Met靶向的ABBV-399已进入全球注册性III期临床,领先阿斯利康、再生元等竞争对手一个身位。
最新的II期LUMINOSITY研究显示,ABBV-399在c-Met高表达、EGFR野生型非鳞状非小细胞肺癌(NSCLC)患者中的ORR为35%。艾伯维把这一结果描述为“令人信服的(compelling)”,并将基于该研究向全球监管机构寻求加速批准的可能性。
二代c-Met ADC ABBV-400也即将进入II期临床,还有一款SEZ6 ADC ABBV-706拟用于治疗小细胞肺癌,正在进行I期临床。
从ImmunoGen收购获得的索米妥昔单抗头顶“first-in-class”光环,乃是全球首款获批上市的FRα ADC。2022年11月,索米妥昔单抗在美获批治疗既往接受过1-3种系统治疗的FRα阳性的铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌患者,这也是FDA批准的首个用于铂耐药卵巢癌的ADC药物。
上市短短一年,索米妥昔单抗展现了亮眼的商业化前景。2023年前九个月,其销售额超2.1亿美元。ImmunoGen首席执行官Mark Enyedy表示:“索米妥昔单抗正朝着十年来肿瘤领域最成功的首发产品之一迈进。”艾伯维认为,索米妥昔单抗有着数十亿美元的市场空间,未来有望拓展早期和更大范围的卵巢癌市场。
艾伯维还非常看好ImmunoGen带来的新一代FRα ADC药物IMGN-151,同样主攻卵巢癌,正在开展I期临床试验;还有CD123靶向的pivekimab sunirine,用于罕见的血液肿瘤母细胞性浆细胞样树突细胞肿瘤, 目前处于II 期临床。
神经科学领域,是艾伯维瞄准的下一个蓝海。
日前,艾伯维便出手87亿美元收购了Cerevel Therapeutics,该公司主要聚焦精神病学方面,这与艾伯维在神经科学领域关注的三大重点之一不谋而合。
Cerevel的晚期资产emraclidine是一款高度选择性靶向毒蕈碱M4的正向变构调节剂(PAM),被认为是具有best-in-class潜力的下一代抗精神病药。此外,emraclidine在阿尔茨海默症以及帕金森病等痴呆相关精神病方面也显示出一定的治疗可能性。
再往前追溯,也能看到艾伯维在神经科学领域不少的外延动作,于今年10月收购Mitokinin,获得一款潜在FIC帕金森病新药MTK-458;于2022年8月与Sosei Heptares达成新合作,共同开发与神经系统疾病相关的靶向新型G蛋白偶联受体(GPCR)的小分子;于2022年4月与Plexium合作,挑战用于神经系统疾病的新型靶向蛋白质降解(TPD)疗法开发。
除了精神病学,艾伯维还看到偏头痛和神经退行性疾病领域藏有偌大商机。Ubrogepant、atogepant和A型肉毒毒素这3款产品打出组合拳,覆盖所有偏头痛人群。艾伯维预计前两款产品均有可能达到10亿+美元的销售峰值。
晚期帕金森病新药ABBV-951离上市还差“临门一脚”。今年3月,艾伯维收到FDA就ABBV-951新药上市申请(NDA)发出的完整回复函(CRL)。在信中,FDA要求艾伯维提供ABBV-951设备(泵)的额外信息作为NDA的一部分,不需要再额外做与该药相关的疗效和安全性试验。艾伯维表示,将会尽快重新提交NDA。
修炼内功

作为公认的自免巨头,艾伯维长期布局的主线就是专注于自免领域,以修炼内功筑高竞争壁垒。曾凭借修美乐一款产品打遍天下无敌手,如今修美乐的生命周期已进入下行阶段,艾伯维也在积极实施战略转向,从单一产品发力到差异化组合互补。IL-23单抗利生奇珠单抗和JAK1抑制剂乌帕替尼两款重磅产品接力修美乐。
利生奇珠单抗以斑块状银屑病为首要突破口,于2019年4月获得FDA批准上市,又于2022年获批治疗银屑病关节炎和克罗恩病。利生奇珠单抗的成长速度惊人,上市第4年就跨越了50亿美元的大关。要知道,即便是修美乐,也花费了9年才实现这一成绩。
彪炳的战绩背后,是艾伯维高举高打的策略在奏效。根据医药魔方数据库,艾伯维作为申办方和合作方围绕利生奇珠单抗共开展了58项临床研究,主要布局在斑块状银屑病和克罗恩病这两个细分适应症上。而这两个赛道也是自免玩家的必争之地,可谓高手如林。
因此,艾伯维还强势发起了数场头对头战役来铺平利生奇珠单抗的征伐之路。目前,利生奇珠单抗已击败乌司奴单抗、阿普米司特和司库奇尤单抗等对手,甚至不惜踩着修美乐“上位”。
乌帕替尼是全球首款获批上市的选择性JAK1抑制剂。从2019年8月上市至今,乌帕替尼已迅速斩获了7项适应症,覆盖类风湿性关节炎、银屑病关节炎、特应性皮炎、溃疡性结肠炎、强直性脊柱炎、非放射学中轴型脊柱关节炎和克罗恩病。在不断拓宽适应症的同时,乌帕替尼也快速打开了美国、欧洲、日本和中国几大重要市场。
在其他疾病领域,乌帕替尼还有很大的治疗潜力待释放。今年5月,乌帕替尼治疗系统性红斑狼疮的II期研究达到主要终点;10月,针对非节段性白癜风的IIb期研究告捷。基于此,艾伯维顺利将相关适应症的研究推进至III期,JAK系列产品中乌帕替尼的开发进度位列前三。
乌帕替尼用于化脓性汗腺炎的全球III期研究已完成首例患者给药。据估计,化脓性汗腺炎影响着全球高达1%的人口,但目前尚无治愈方法,治疗方案也十分有限[1]。近十年来仅有两款疗法获批,而其中一款便是修美乐,这为乌帕替尼的新适应症拓展提供了可贵的开发经验。此外,乌帕替尼用于斑秃的III期研究也在开展中。
对于利生奇珠单抗和乌帕替尼这两款产品,艾伯维予以的厚望不单是补齐修美乐的市场缺口,更意在超越。到2025年,艾伯维预期两者合并营收将达175亿美元,到2027年超过修美乐的峰值收入,向210+亿美元迈进。在自免领域,艾伯维或将铸就一个强者愈强的故事。
小结
从前景未明的领域果断抽身,再进攻自己坚定看好的赛道,同时不断深耕优势业务板块,艾伯维已在新十年的开局打出关键球。
在充满不确定性的创新药竞赛中,没有永远安全的避风港可供玩家停靠,而唯有像艾伯维这般积极求变,才有可能穿越周期,赢得长期的胜利。
撰稿人 | 医药魔方
责任编辑 | 胡静
审核人 | 何发

















评论
加载更多