TCE双抗吹起挑战Car-T的号角!
01
BCMA的舞台上
Car-T和TCE双抗同台竞技
今年以来,BCMA相关的新闻此起彼伏。
2月,在万众瞩目中传奇生物与强生合作的BCMA Car-T治疗产品Carvykti获得美国FDA批准,代表着中国源头创新的成功出海。8月初,安进悄然透露已终止管线中最后一个BCMA药物AMG701的开发,从曾经的坐拥该靶点2个双抗和1个ADC,到现在的清仓,变化之大令人唏嘘。短短两周后,便传来强生的CD3xBCMA双抗Tecvayli获得了欧盟的有条件上市许可。
BCMA这个靶点,怎么这么火?
BCMA (B-cell maturation antigen),主要表达在成熟B淋巴细胞和浆细胞表面。当位于骨髓中的浆细胞异常增生,可导致多处骨损伤,逐渐发展成多发性骨髓瘤 (Multiple Myeloma, MM)。MM主要发生在65岁以上的老年群体,是美国第二常见的血液瘤1。过去中国的发病率较低,为美国的20%左右。但近年来,随着经济发展,就诊率提高,加上人口老龄化,MM在中国的发病率持续上升,有数据显示已达到美国的40-45%。
MM目前仍是难以治愈的疾病,患者大多会发生一次以上复发,且每一次复发后的治疗缓解时间会缩短,使得对复发或难治性MM(relapsed/refractory MM,R/RMM)的治疗提出较大诉求。研究发现,BCMA过度表达和激活,在无论是新诊断还是复发的病人中都存在,使得BCMA成为R/R MM药物开发的一个高潜力靶标2。
从第一个BCMA药物在2020年上市至今,已有4款针对该靶点的药物获批,涵盖了ADC、Car-T和CD3双抗三种类型(表1)。
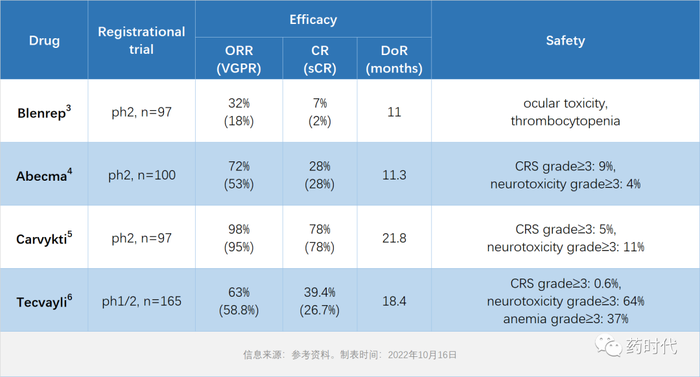
表1:已上市的BCMA靶向药物

虽然适应症均是4或5线治疗R/R MM,但从临床疗效上可明显看出后来者较先行者的不断突破。相较于第一个Car-T产品Abecma,第二个Car-T产品Carvykti,在有效性(ORR、CR、DoR三个指标)和CRS安全性上,都有大幅提升。而最新获批的双抗Tecvayli,虽然响应率(ORR、CR)不如Carvykti,但已经媲美Abecma,且在DoR上也紧追Carvykti,作为一种“现货型”药物,可谓是来势汹汹(表2)。
其实无论是Car-T还是CD3双抗,作用机制都是把杀伤性T细胞带到BCMA表达的肿瘤细胞,并通过T细胞杀伤功能消灭肿瘤细胞。区别在于Car-T可以通过体外扩增增加T细胞的数量,而CD3双抗调动的是机体内现存的T细胞,因此Car-T可以一次给药,效果强且持久,而CD3双抗则类似传统药物,需要定期给药。但同时,不同于Car-T的个性化、定制型疗法,CD3双抗是一种现货型产品,无论是便利性、可及性,还是生产成本上,都具有天然优势,这些也是Car-T疗法实现普适性所需要克服的挑战。
-
Amgen BiTE® vs Janssen DuoBody®
-
TCE开发的挑战 vs 双抗平台的能力
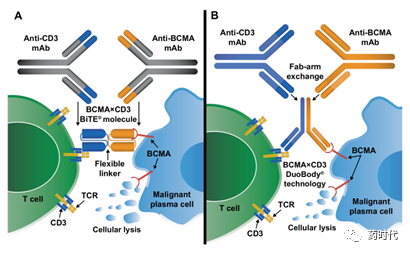
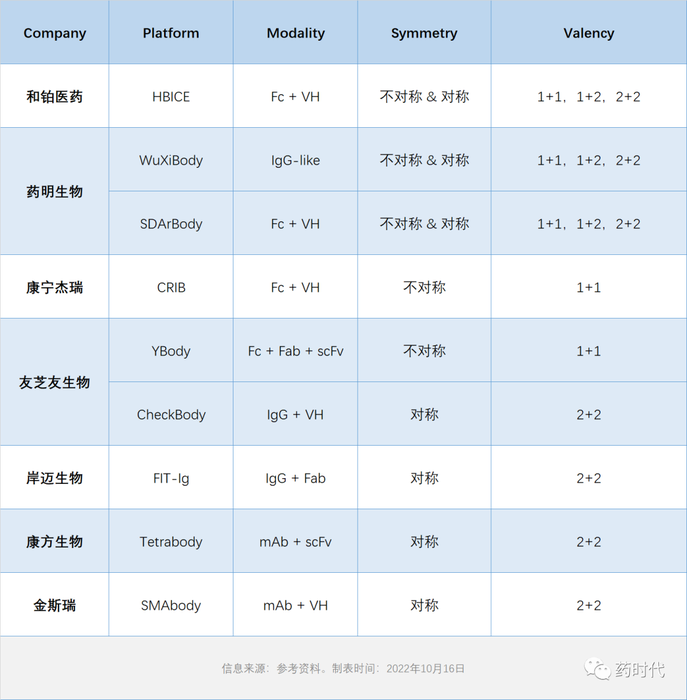
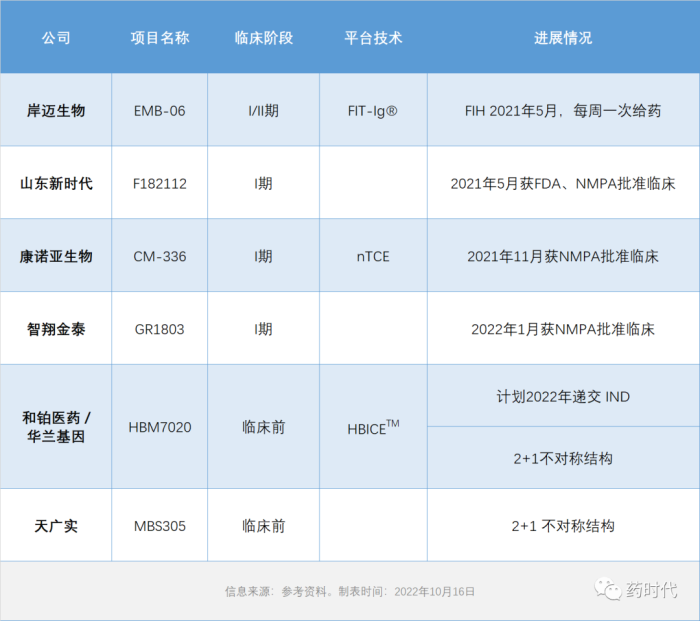
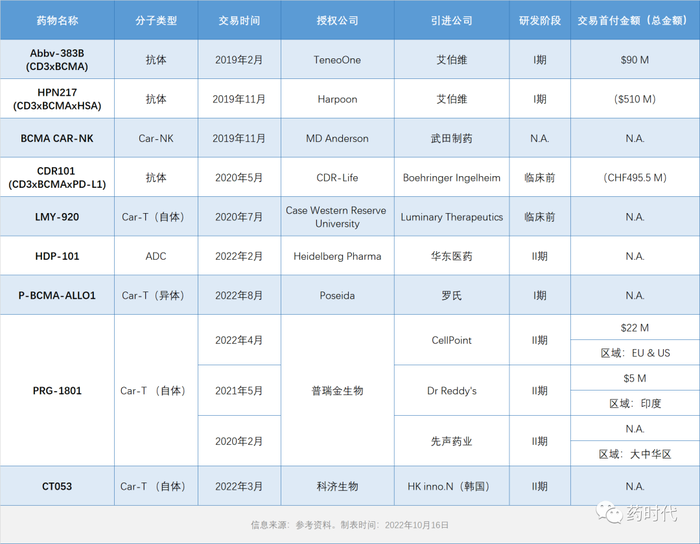
表5:近3年涉及BCMA靶向治疗的授权交易概览
参考资料:
1. Pradala et al., Med Sci. (2021) 9:3
2. Shah et al., Leukemia (2020) 34:985
3. www.blenrephcp.com based on data at 13 months
4. www.abecma.com
5. www.carvykti.com
6. Moreau et al., N Engl J Med (2022) 387:495-505
7. Ellerman D, Methods (2019) 154:102
8. Nie et al., Antibody Therapeutics (2020) 3:18-62
9. 其它公开资料
文章来源于药时代
邵丽竹
何发
热点文章
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
微生物发酵技术在植物活性成分提取中的应用研究进展
2026-03-06
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多