微生物实验室检查要点:环境条件

环境微生物测试设备(图片来源于网络仅供学习交流用)
1、环境监测
1.1 9203药品微生物实验室质量管理指导原则的相关规定
微生物实验室应按相关国家标准制定完整的洁净室(区)和隔离系统的验证和环境监测标准操作规程,环境监测项目和监测频率及对超标结果的处理应有书面程序。监测项目应涵盖到位,包括对空气悬浮粒子、浮游菌、沉降菌、表面微生物及物理参数(温度、相对湿度、换气次数、气流速度、压差、噪声等)的有效控制和监测。环境监测按药品洁净实验室微生物监测和控制指导原则(指导原则9205)进行。
1.2 洁净区和隔离系统的验证相关内容检查要点
1) 洁净区的验证
通常我们认为的就是洁净区的洁净级别确认,然而实际上最需要关注的是洁净区相关的物理参数,前者只是一个结果,后者才决定了空调系统的有效性。其次因为验证的数据有限,日常对物理参数的检测数据更能反馈出空调系统的实际运行状况。基于以上考虑洁净区验证时我会更关注一下几点:
a) 洁净区验证的证据资料,除了实验记录,相关的视频等证据更具有参考价值;
b) 洁净区验证的结果与日常测试结果的对比,通常可以结合年度回顾报告一起看,如果有问题特别容易发现;
c) 洁净区验证的可操作性,例如采样布局图是否有指导意义,很多布局图只是一个方框里面有几个点没有体现现场的设备等现场情况,这样的布局图就没有指导意义;
d) 洁净区验证过程异常数据的处理和分析。发现某些洁净区验证时静态测试的数据接近超标但合格,然后判合格就没然后了。为避免出现这种情况建议做好人员培训和执行规划(例如人员移动轨迹和辅助器具的使用等),不能因为是静态就把采样碟扔地上了。
e) 检查洁净区验证和日常监测的风险评估报告。风险评估最有价值的不是结论而是对风险的认知(特别是风险识别和控制措施等)和对己方情况的认知(例如工艺概述、空调系统概述)。因局限于专业,通常该部分评估需要相关各部门的协作。
2) 超净工作台和生物安全柜的定期验证
气流流型和高效过滤器检漏(气溶胶挑战测试)两点因为没有相应设备很多公司做不到,不具备条件时可以考虑每年计量时进行相关测试项目也可达成相应目的。
3) 高效过滤器定期检测和更换
关注这一点主要原因是很多公司工程人员并不清楚如何去做。有一些人认为每年进行一次高效过滤器更换但不进行更换前不进行任何测试,这种操作常会被挑战如何确保换下来的高效过滤器仍满足要求。
其次个人比较关注中效和初效的更换级维护,如初效和中效更换频次低,其高效的生命周期也应缩短。高效的使用时间并不是一个独立事件。

高效过滤器检漏(图片来源于网络仅供学习交流用)
其中附录1(PIC/S P032-2)的技术诠释,A/B级每6个月进行泄露测试,C/D级则为12个月。这一点可以作为我们进行检测的参考。
其次高效过滤器泄露是可以修补的,修补的面积不能超过单个过滤器面积的0.5%。
高效检漏可以是判断高效是否需要更换的一个判断标准。从实践角度来说,高效的最常使用时间直接取决于压降。只有在压降达到一定高值影响到通风系统的性能或者是能量需求超过过滤器更换成本时过滤器的更换才有意义。
4) 隔离器系统的验证
关于隔离器的验证是一个复杂的问题,其中有三点需求特别关注(以过氧化氢灭菌隔离器为例):
a) 验证的装载方式及采样点的布置,因为过氧化氢气体并不具备灭菌能力,因此装载时如果直接接触台面的装载通常不能满足要求,隔离器内部的支架应尽可能镂空,这些挑战难点均需要进行布点。
b) 隔离系统内部环境的无菌维持,进行隔离系统内部环境无菌维持的验证时,个人认为需要根据操作周期内的实际进行模拟操作,因为检验用具和供试品进入舱内的过程最可能造成微生物污染,如单纯的验证空载或满载时进行微生物监测是不充分的。
c) 包装完整性验证又是一个大坑,避免假阴性和假阳性这两方面都需要考虑。
1.3 环境监测标准操作规程
1.3.1 操作规程是否可以指导日常操作
1) 只是照抄药典规定最少取样量等操作是不适宜的;
2) 日常取样的采样点要有布点图且布点图要体现区域内设备等信息,且日常测试应有风险评估;
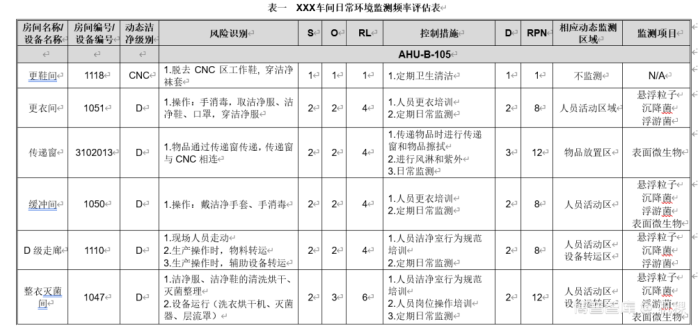
日常环境测试评估表(图片来源于网络,仅供学习交流用)
3) 为避免不必要的偏差需要明确工作细节,如不要从已打开平皿上方经过或进入层流采样要有延迟时间等细节。通常文件和培训资料里面如都没体现以上信息,那么这样的培训存疑;
4) 环境测试或监测相关的定义应明确,或者在培训资料中明确;
1.3.2 是否将日常测试和洁净区级别确认分开规定,或者起草两个文件,只是照抄国标会发现无法进行指导日常工作;
1.3.3 相关法规依据是否体现在文件中,体现可以作为支持,注意太多时注意其适用范围的不同。如布点问题,按ISO14644-1是一种做法,而按照自己日常管理进行评估又是一种做法。
1.3.4 记录及辅助记录是否符合数据完整性的要求;
1.3.5 环境测试结果如何进行观察,因为环境测试结果是主观判断的一个结果,建议至少双人出样,至少做到一个人计数另外一个人复核。
1.3.6 环境监测项目和监测频率是否满足产品需求和法规规定。
1.3.7 对超标结果的处理除有书面程序外,不建议按照OOS处理,调查时最好可以及时调动各相关部门进行调查而不是先死查QC然后贻误战机。
1.3.8 辅助文件确认,例如洁净室管理、更衣程序、物料进入洁净区程序、洁净服清洗和灭菌等,内容过多此处不展开。
1.3.9 带菌废弃物的处理和人员管控
1.4 其他确认内容
仪器设备等此处不提及;环境监测现场确认是否放置与实验无关的物品这一点可以反馈出实验室的一个整体状态。
2、清洁消毒和卫生

疫情消毒宣传图(图片来源于网络,仅供学习交流用)
除却工程人员对空调系统的维护对基础环境条件至关重要外,日常的清洁消毒和卫生又是我们需要关注的重点。关于清洁消毒部分内容较多,后续补充,此处不展开,只提及检查的关注重点。
2.1 消毒剂配制使用的SOP及详细记录
2.1.1 定期轮换使用;
2.1.2 除菌过滤;
2.1.3 在效期内使用;
2.1.4 消毒剂的存放地点;
2.1.5 消毒剂容器应贴有标签。
2.2 要有清洁、消毒的标准操作规程
2.2.1 洁净区使用前后都要消毒,定期监测消毒效果,有足够的洗手和手消毒设施;
2.2.2 所用的消毒剂种类应满足洁净实验室相关要求并定期更换;
2.2.3 A级和B级洁净区应当使用无菌消毒剂和清洁剂。
2.2.4 所用消毒剂和清洁剂的微生物污染状况应进行监测,并在规定的有效期内使用。
3、小结
微生物实验室的监测只是发现问题一种手段,工程人员的维护和相关人员对洁净区的维护更为关键。微生物实验室需要确保环境监测结果有效且真实,最好是不同阶段结果均可比,真的要做好环境监测是一件了不起的事情。
关于清洁消毒和卫生,微生物实验室应该是整个公司的标杆。以上就是个人的全部总结,欢迎各位老师指导,共勉。
本文来源于博普智库制药前沿
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多