限制进入屏障系统 (RABS)(例如开放式 RABS、封闭式 RABS、和隔离系统)的使用在减轻风险和确保遵守不断变化的监管标准方面发挥着至关重要的作用。更新后的附件 1 对屏障技术进行了全面的说明。当前的要求需要对现有生产线进行战略改造,以增强风险降低和监管准备。
传统无菌灌装的灌装线通常保持为 A 级。配备高效过滤器 (HEPA) 的 A 级房间可保持单向气流。研究已证实,人为因素和相关的无菌行为会导致活性和非活性的污染。为了最大限度地减少污染还可以确保对“首过空气”影响的最小化(即破坏从HEPA 过滤的空气到加工区域的单向气流)。常用的 RABS 等屏障技术成为传统生产线的理想选择,其可以最大限度地减少意外操作,最大限度地减少破坏首过空气的可能性,并尽可能让操作员远离关键流程。
由于其精确的无菌保证水平计算、验证和控制,最终灭菌是确保产品无菌的首选。然而,由于产品固有的特性,无菌工艺对于某些生物制品、疫苗和注射剂至关重要,因此被认为是最终选择。因此,为其制定了严格的要求,以最大限度地降低无菌生产过程中可能会对患者所产生的风险。洁净室污染的很大一部分归因于人为来源,活动的增加所带来的直接影响污染。为了缓解这种情况,人员需要接受培训,例如采取减少移动和尽量减少跨房间沟通的做法。研究证实,加强洁净室环境和人员管理可有效减少颗粒物和微生物污染,主要来自人员密度和活动。进入洁净室之前进行的活动也可能会影响生物负载水平,导致洁净室内微生物数量偶尔增加。
水也是常见的细菌内毒素和生物负载的来源,可能携带革兰氏阴性菌。因此,进一步监控使用链中的工艺水也非常重要,例如配制或清洁环节。内毒素源自革兰氏阴性菌,进入血液后会产生严重后果,导致炎症反应、感染性休克和死亡。这些脂多糖分子由脂质、核心多糖和称为 O 抗原的多糖侧链组成,其因细菌菌株而异。脂质成分将内毒素固定在细菌细胞膜上,在细菌感染期间引发炎症。脱落的内毒素与动物细胞表面的 Toll 样受体 4 结合,引发炎症反应。其热稳定性需要持续监测活细胞(生物负载)和内毒素。制药工艺和设备面临着各种来源的微生物污染的持续风险,包括人体接触、环境灰尘、包装材料、受污染的冲洗水和微生物生长。可接受的内毒素水平取决于产品类型、疾病适应症、给药途径和剂量。
根据应用和传统生产线的状态,主动或被动开放式 RABS 或封闭式 RABS (cRABS) 可能是合适的。如果涉及控制房间环境和处理高活性化合物,cRABS是更好的选择。主动 RABS 通常将 HEPA 过滤器和风扇单元全部封闭在屏障框架内。另一方面,被动式 RABS 使用现有的室内 HEPA 过滤器,非常适合改造场景(见图1)。在此类设计中,屏障一直保护到洁净室 HEPA 的首过空气供应。适合用途的改造设计提供了防护和策略性进入的组合,使操作员能够隔离并远离首过空气,同时仍然可以进行装载胶塞等工艺活动。
安装专门设计的快速转移端口 (RTP) 和其他集成转移端口,以在无菌操作期间执行操作或将材料转移到 RABS 内部。初始设置完成后,仅在必要时才打开门,并进行相应的监控和记录。在设置操作之前,RABS 的内表面使用杀孢子剂进行消毒和净化,并使用 70% 异丙醇 (IPA) 擦拭。当有了新引入的污染控制(例如被动 RABS)后,还可以考虑将洁净室重新定级分类,从无菌工艺 A 级洁净室变到屏障内的 A 级、背景保持 B 级,前提有培养基灌装数据支持。
可定制的基于模块化的 RABS 为升级改造过程提供了更好的灵活性。必须高度重视操作员的人体工程学,特别是从传统系统到基于屏障的系统,因为最初的空间设计没有考虑封闭环境内的移动。合规的 RABS 应具有适当的气流管理和控制功能,以确保产品受到保护。此外,还需要进行全面的风险评估,以确定所需的功能,确定额外的程序,确定常规和非常规干预措施并确定失败模式。
从传统洁净室灌装系统过渡到 RABS 时,全面分析辅助组件的引入至关重要,例如工具、更换部件、RABS 手套和拖把头(见图2)。它们在RABS 环境中的功能和操作中发挥着重要作用。将工具集成到 RABS 设置中需要评估其大小、形状、位置和使用频率。镊子、RTP 工具、推杆等工具应有策略地放置和设计,以保证顺利操作,而不会阻碍屏障系统或污染关键环境。为这些工具选择适当的材料和灭菌方法也很关键。在此类改造过程中,预计会出现用于设备调整或产品转换的新更换部件。更换部件本身不应增加安装或更换过程中的污染风险。正确的处理程序和设计考虑对于最大限度地减少对受控环境的干扰至关重要。它们的设计、放置和利用可能会影响气流动力学、颗粒分散和遏制效率。
在从传统灌装工艺向 RABS 转变的过程中,必须全面评估新引入的干预措施的影响。这些评估应涵盖几个关键方面,例如它们对制造过程验证状态的影响、对烟雾研究的影响、对产量的考虑、对首过空气的关注、干预措施的危害性以及其在培养基灌装计划中的包容性。主要关注点之一是这些干预措施如何影响不同产品的验证过程。
目的是确保引入新的干预措施或更改不会损害关键设置方面,否则可能导致需要重复工艺验证并更改现有提交的文件(例如,生产线速度、过程中控制等)。
在许多情况下,引入新的干预措施将影响现有的烟雾研究,需要重复这些研究。新的干预措施也会影响生产线的产能。就 RABS 系统而言,与传统生产线相比,干预措施通常会导致处理速度变慢。这种放缓可能会影响生产线的保持时间和最大产量,值得仔细检查。同时,评估新设计是否会无意中引起与不可避免的首过空中泄露也很必要。此外,必须根据这些干预措施的关键性来评估干预措施,以确保新的干预措施或新的干预方式不会改变已经备案的干预措施的危险程度,从而防止影响无菌确效标准。必须适当考虑培养基灌装计划的包容性,确保涵盖所有预期的固有干预措施和纠正干预措施。同样重要的是建立一个有效的流程,根据需要在后续的培养基灌装试验中不断更新此干预列表。
用户要求规范 (URS) 应根据监管指南、对制造商的需求和工艺要求明确定义并记录 RABS 的要求。然后设计确效活动来评价 RABS 设计,包括其规格、布局、功能以及对 URS 的遵守情况。安装认证验证 RABS 是否已根据制造商的设计和法规要求正确安装。操作效果确认测试确认系统在正常操作条件下的功能和性能,以确保其满足定义的规范要求。最后,性能确认表明 RABS 在实际操作条件和模拟生产环境中始终按照规范执行。
使用 RABS 进行多次培养基灌装运行,以代表实际产品灌装过程中可能遇到的不同场景和条件,例如无菌干预、设备故障和偏差,这些可能会对监管指南规定的无菌过程提出挑战。在适当的条件下,监测灌装后培养基的微生物生长以确定无菌工艺过程的有效性。无菌灌装过程受到持续监控,并且需要定期重复培养基灌装研究,以确保 RABS 的持续有效性。此外,挑战研究要求尽可能多的人员以较高的活动水平出席(根据标准操作程序 [SOP] 的允许)。案例研究应将无菌工艺污染追溯原因于人员操作不当、环境控制缺失和操作设计缺陷中的一种或多种组合。
通过遵循彻底的确效活动和培养基灌装策略,企业可以证明 RABS 在灌装过程中维持无菌条件的有效性。
RABS 装置采用手动清洁,包括喷洒和擦拭方法进行生物净化。挑战在于使用手动方法实现一致、可重复和完整的生物净化。现在,验证 RABS 系统中使用的清洁和生物净化解决方案的有效性是证明手动清洁过程合理性的重要一步。作为清洁过程验证的一部分,从 RABS 内的各个位置采集样本来测试清洁度和微生物含量,并擦拭用于灌装操作和其他需要操作员交互的任务的手套口。清洁操作应从最清洁的区域开始到最不清洁的区域,以尽量减少污染物的扩散,遵循顺序:
天花板
设备、RABS 门内表面
手套、RABS 门外表面
柜台、推车
墙壁、窗户、门、突出表面、通道
-
清洁操作时使用适当的个人防护装备,包括手套、护目镜、洁净服和不脱落的清洁材料和工具。应特别注意可能与产品接触的任何可移动部件和组件。密封条/圈也应被彻底清洁和消毒,特别注意进入点和门周围的密封。用 70% IPA 擦拭,然后进行消毒并与杀孢子剂接触一段时间。必须制定常规的前处理、后处理、每日、每周、每月的清洁标准和清洁剂。维护详细的清洁记录,包括日期、时间、使用的清洁剂、有效期以及清洁过程中遇到的任何偏差至关重要。在关键阶段进行适当的生产线清洁。
RABS 的复杂性可能需要额外的操作时间。RABS 的设置活动可能包括开门活动和闭门活动,需要额外的时间和精力。在灌装操作过程中,在严格遵守 RABS 方案方面需要更加精确和专注,这可以通过常规无菌实践培训来实现。培训应重点教育人员在 RABS 环境中工作所需的无菌技术,包括更衣、材料处理和保持无菌。操作员需要了解RABS 的设计、功能和操作。培训模块应详细说明 RABS 内的逐步操作程序,例如设备设置、材料转移、灌装过程、干预和清洁。此外,它还应涵盖应急计划以及对 RABS 环境中的偏差或紧急情况的响应。员工应接受关于完成批次记录、日志和任何特定于RABS 操作的文件的培训。
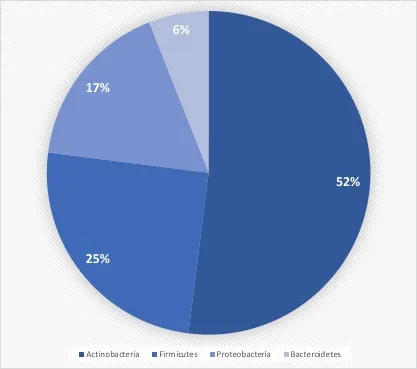
例如,据了解,皮肤层上的细菌种类多种多样(见图3),包括1,000多种。此外,研究表明,穿着防护服的操作员每小时有可能释放多达 10,000 个菌落形成单位,因此需要对操作员进行全面的无菌操作培训(见图4)。训练有素的员工队伍对于向 RABS 的成功过渡有着重大贡献。
用流动的温水洗手 20 秒,在肘部用力涂抹肥皂,然后冲洗双手,不要接触任何东西。
要求操作人员常规使用 70% IPA 进行消毒。70% IPA 比 100% IPA 更有效,因为它会缓慢穿透细胞壁并凝固所有蛋白质。100% IPA 蒸发速度快,而 70% IPA 的活性保持时间更长。
在无菌处理过程中避免以圆周运动擦拭。使用平行擦拭的单向擦拭非常适合去除污染物并有效地最大限度地减少其扩散。擦拭是从最干净的地方到最不干净的地方进行。
面罩紧贴脸部轮廓。面罩形成至鼻梁。取下和丢弃时,不会触及口罩的正面。
从传统灌装流程过渡到 RABS 时,必须更新、修订或创建一些重要文件,以适应新流程和技术。需要详细说明 RABS 系统的操作、维护、清洁和监控的新 SOP。必须修订批次记录,概述 RABS 内灌装的步骤和程序,包括 RABS 流程特有的任何附加检查或要求。将引入详细说明 RABS 系统清洁和维护的记录,包括任何使用前和使用后检查。专门用于验证 RABS的方案和报告,确保其符合无菌加工工艺所需的标准。QMS 文件,例如质量政策、目标和监控流程,应纳入 RABS 引入的变更。必须重新评估环境监测 (EM) 程序,以确保符合所需标准。
这一变化可能会影响产品的监管提交状态。根据市场情况,监管机构可能需要对 RABS 实施带来的变化进行彻底评估,这可能会导致供应中断。制造商必须与监管机构、客户和消费者密切合作,确保所有必要的文件均得到更新并准确提交,以减少潜在的延误和相关挑战。尽早分享有关其好处的信息可以增强对变革过程的信心。诸如 ICH Q12:药品生命周期管理的技术和监管注意事项等监管工具可通过利用批准后变更管理协议 (PACMP)实现更快的审批途径。在所有情况下,必须详细阐述引入 RABS 来改进产品无菌灌的策略和方法,并且必须明确定义验收标准。
隔离器技术被认为可以消除操作员的潜在污染,从而提高无菌保证水平,同时保持较低的 C 级背景。尽管如此,在 A 级运行的传统洁净室设置可能更喜欢采用 RABS 技术进行升级,因为它可以提供类似的无菌保证水平,同时减少投资。它们对于减轻污染风险和确保遵守不断变化的监管标准至关重要。强调使用 RABS 等屏障技术,可最大限度地减少污染并尽量减少破坏首过空气的机会。根据应用和遗留生产线的状态,考虑环境控制和处理高活性化合物,从而评判主动或被动 RABS的适用性。
为了有效保护产品,改造设计应优先考虑操作员人体工程学、气流管理和密封功能。过渡到RABS 需要更新 SOP、批次记录和培训材料。至关重要的是让质量保证、制造、工程和验证团队等相关利益相关者参与进来,以确保顺利过渡到 RABS 灌装工艺。从传统无菌操作到采用 RABS 的历程代表了技术进步和战略演变,朝着更安全、更合规和高效的制药制造方向发展。
文章翻译自:
Legacy Filling Lines EvolveSafeguarding with RABS Technology
BY Ahmed Elsaid, Emergent Biosolution and Ajay Pazhayattil, PhD, cGMP World
PUBLISHED ON Apr 3, 2024, PDA letter
撰稿人 | 拾西
责任编辑 | 邵丽竹
审核人 | 何发


















评论
加载更多