Trilink专利国内获批,避之不及?No!赢难而上,打破封锁才是正道!



打破该专利壁垒的方式,我们在市场上听到了2种声音,有退而求其次,主张“酶法”的【保守派】,同时,我们很骄傲的看到,更多具有自主研发能力的【创新派】企业选择迎难而上,打破困局。在生物医药这种强调技术创新的行业里,用攻坚克难的毅力,用真材实料的质量,合成新型结构的帽类似物,从学习Trilink到超越Trilink,完成打造自身企业“坚实脊梁”的华丽转型!
Trilink此次获批的“用于合成5’-加帽RNA的组合物和方法”,该专利保护的是复合体(其包含起始加帽寡核苷酸引物和DNA模板),专利中展示了所述起始加帽寡核苷酸引物包含的结构。复合体实际上就是帽类似物以及和该帽子所匹配的DNA模板。简单的说,更换一种新的帽类似物结构或者不使用转录起始位置+1位和+2位碱基与传统帽类似物互补配对的DNA模板(AG模板),就可以解开该壁垒的封锁。

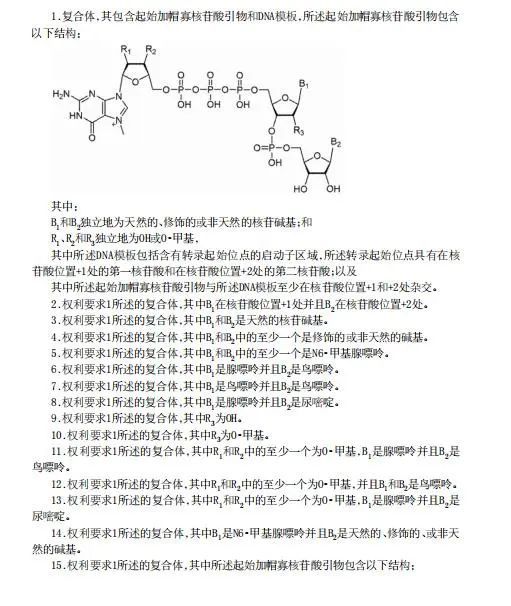
这两年,关于酶法加帽和一步法加帽的优劣势对比,不论在各大公众号平台的推文上,还是展会现场的演讲中,已经被反复提及,优劣对比不言而喻。无论是从工艺的复杂程度、杂质的含量、成本的控制等多方面,都有大量的数据论证。酶法加帽在过去的一段时间里,确实为生物医药行业的发展立下汗马功劳,随着技术的不断革新,一步法加帽应运而生,是顺应技术变革浪潮的必然选择。
酶法加帽是使用专门的酶对其进行加帽反应,即使用VCE(牛痘病毒加帽酶)处理IVT产物,先将其修饰成Cap 0 mRNA,然后再进行甲基化处理,变成Cap 1 mRNA。从该工艺过程可以看出,多了加帽过程和甲基化步骤,且引入了两个额外的蛋白和SAM,导致制备工艺复杂,需多次纯化,也增加了QA/QC质检的难度,势必会使成本显著上升。
“共转录加帽”则是在IVT反应体系中直接加入Cap 1帽类似物,实现一步法获得含Cap 1结构的mRNA,全程只需一次纯化,一步到位!这种“一锅法”反应减少了制造步骤,进而有效缩短整体处理时间、简化纯化步骤,可迅速提升mRNA疫苗/药物的产能,是目前mRNA产业化制备最受青睐的mRNA加帽方式,必然也会成为未来mRNA合成的主流工艺。
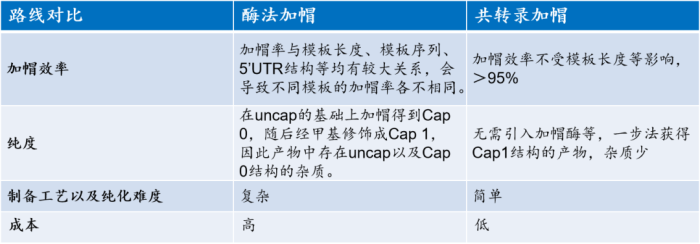
我们都知道,在上市COVID-19 mRNA疫苗中,BioNTech选择的是共转录加帽,而Moderna选择的是酶法加帽。但是,据业内人士反馈,Moderna目前在研管线已经选择了共转录加帽。Trilink专利最早在美国、欧盟、澳大利亚等布局,因此,海外面临的帽类似物专利问题远大于国内,为什么大多数公司还是选择用共转录加帽而不用酶法加帽?业内人士给出了这样的解答:
酶法加帽存在的问题:
✅ 酶的批间差异比作为小分子的帽类似物要大很多,是医药行业比较忌讳的;
✅ 酶法加帽工艺和杂质都会更复杂,不易纯化;
✅ 酶法成本相对共转录加帽,还是太高。
壁垒?动力?逃避?破局?中国优秀企业在行动!
帽类似物难道只能选择进口吗?NO!
虽然帽类似物制备工艺复杂,但是,绝不让帽类似物成为我国mRNA疫苗和药物相关领域发展的“卡脖子”技术,这是国内原料企业的心声!新时代、新技术、新发展,为全球的生物医药下游企业提供更多的原料“选择权”,是每一个原料企业的责任和使命!
为了实现mRNA行业自上而下的全产业链替代,让中国mRNA产业发展自主可控,国内的一些优秀企业已经布局了自主开发国产替代的帽类似物产品,并取得了一定成绩,获得了专利许可。如,江苏申基生物科技有限公司,从获得的资料显示,该公司已获得7项帽类似物结构专利,除了已经获批的帽类似物专利,还有10余项申报中的其他新型帽类似物专利,且获批的帽类似物结构专利,均不在此次Trilink获批的专利保护范围之内!

期待更多如申基生物的高精尖企业,加入到新型帽类似物以及新型原料的研发生产当中!
结语
相对于那些唱衰国内mRNA行业的声音,我们应该更理性的看待Trilink此次应用专利的获批。让我们看到有那么多中国企业,在用实际行动证明【中国制造】到【中国创造】的转变,在这种良性竞争下,促使国内企业开始进行到创新研发工作,从整个生物医药大格局上看,下游药企有了更多的选择,专利是壁垒,也是动力!逃避解决不了问题!面对Trilink应用专利国内获批,迎难而上,打破封锁, “新质生产力”才是王道!
撰稿人 | 生物药大时代
责任编辑 | 邵丽竹
审核人 | 何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多