一次性生产,最大限度地提高效率
为了设计一座工厂,人们应该考虑每个特定的单元操作,并与决策因素保持平衡。每个单元操作都有一个明确的目的,每个步骤都是不同的。单元操作中使用的设备可能相同,也可能不同。例如,所有层析步骤可能使用相同的仪器/系统,而切向流过滤(TFF)需要另一个, 病毒灭活则需要更简单的器具。必须考虑以下列出的问题:
(5) 预期的需求水平是多少,因此需要多少产能?
他们的答案将说明工厂的设计和产能应该是什么。在上游,由于生物负荷风险较高,存在严格的CIP 和 SIP 要求。另一方面,在下游工艺中,药物在提高纯度和质量方面得到纯化。因此,与生物反应器耗材相比,将需要高端分析仪器,导致SUT 耗材成本较高。
近年来,一次性系统不断得到创新和改进,解决了与灌流工艺相关的问题,例如一次性生物反应器、过滤器、层析柱和细胞截留装置。
在某些需要尽快进入市场的情况下,建议选择一次性技术以获得更快的结果,因为相比失去早期市场机会,一次性技术的成本相对更可承受且具有成本效益。我们必须决定在USP 或 DSP 中使用一次性技术,还是两者均使用,策略的制定基于多方面的因素,例如在多个产品、临床前批次或临床批次之间的切换。
一次性技术在生物制造新时代的好处
如果滴度高且工作体积较少,一次性技术的成本优势就存在。例如,如果需求不高,则无法建造工厂,然后等待并观察需求的到来。一次性技术可以节省时间,因为建造一个不锈钢工厂需要 5年左右的时间。
无需或更少的清洁验证、占地面积小以及灵活的工艺设计是一次性技术的另一个优势。
管理一次性技术的成本
最好在早期开发阶段拥有一次性技术,然后转移到不锈钢设施,以缩短时间。一次性技术可以集成在不同的单元操作之间,例如一次性层析,然后是过滤步骤。
一次性技术的限制包括基于关键的一次性产品编写SOP、一次性产品的库存维护、一次性技术的流路套件在最大流量和压力等级方面的限制,以及与传统传感器相比灵敏度较低的一次性传感器、可溶出物/可析出物和完整性测试挑战等。对于一次性技术,供应商很重要,它需随时准备提供耗材(图6.7)。
表 6.2 与基于不锈钢的生产平台相比,一次性系统可以提供的优势和挑战。
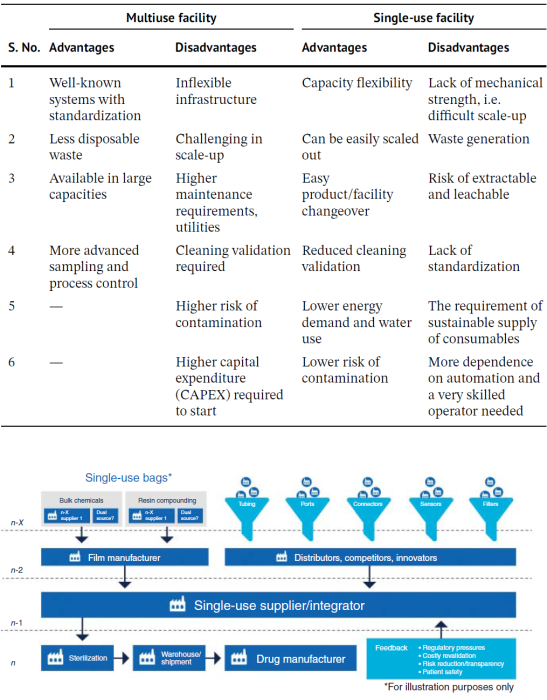
图 6.7 一次性供应链。
在线配液
在线配液是一种特定的方法,通过该方法,可基于系统中的自动操作,以原液制备所需强度的缓冲液,而无需任何人工干预。这可以确保您获得符合规范的正确缓冲液。如果系统检测到任何规格偏差,它会根据设定的规格更正制备工作。
通过在 USP 和 DSP 中使用一次性技术,可以提高mAb 生产。然而,仍然要从具有成本效益的生产方面评估受益程度,可能需要一些额外的先进方法。在不锈钢生物反应器中,从摇瓶到小型生物反应器的种子制备需要多个步骤,波浪式生物反应器可用于高达500 L 的体积。
一次性使用策略对商品生产成本的影响
传统工艺与旧流程一起运行,并且未满负荷运行。同时,设备也不能灵活地适应技术的新进步并满足新的 监管指南的期望,因此需要通过其它方式以遵循指南,从而增加了 COG。另一方面,由于更少或没有 CIP 验证要求、更少的资本支出、低风险、低成本、耗时更少以及更少或没有污染,一次性技术越来越受欢迎。
Biosolve 和SuperPro Designer 是可以模拟和开发经济模型的软件,该模型有助于评估采用一次性策略的最佳生产工艺设计。由于大多数制造商不愿分享其工艺和设施的信息,因此在采用一次性技术的mAb 领域中,可用的信息很少。但是,可以在现有设施中安装一次性技术,以提供更高的吞吐量并更有效地应对监管障碍,从而构建并实现负担得起的工艺。
通过 Biosolve 分析表明,由于一次性技术对维护、公用设施、劳动力和废物管理的要求较少,与不锈钢设施相比,每克mAb 的运营成本降低了 22%。在剑桥健康技术研究所组织的 PepTalk 会议上,一项案例研究表明,在一个装有一次性原液冷冻容器和缓冲袋的设施中,每年可在注射用水(WFI) 生产方面节省了 250,000 美元,在人工方面节省了 60,000 美元,即不锈钢设施的构建和CIP 所需的成本。
针对 1,000 和 5,000 L规模的、不同滴度mAb 的 Biosolve Processmodel 评估显示,在生产设施中,用 一次性膜形式替换精纯填料,可显著减少高达 55% 的缓冲液体积,并将成本降低 19-33%。
通过接受一次性技术建造新设施,无需担心空间紧张、调度限制、安装困难和非优化的布局。尽管会存在初始成本,但与针对多种产品、使用系统和硬件构建不锈钢设施相比,前者成本更低。由于仪器会更小,因此占用空间也会更小。
Biopharm Services Limited 发布了一份白皮书,他们在其中提到,通过使用建模软件,已经表明使用 30 × 2,000 L一次性生物反应器设施的工艺成本为2.5 亿美元,而使用相同容量的不锈钢设施的工艺成本为 3.52亿美元。
根据 Xcellerex 的 FlexFactory 概念,随着设施中一次性操作的整合,洁净室的区域可以设计为容纳带有一次性管组的单个单元,并降低操作员污染的风险。在国际制药工程学会 (ISPE) 斯特拉斯堡会议上,报告已经表明,通过 FlexFactory 设施设计的 2,000 L mAb 设施,与不锈钢设施相比,成本降低了67%,用水量减少了 87%,空间需求最终减少了 45%,从而使商品成本减少了32%。
未来,采用模块化方法的灵活设施可以在场外设计和建造,以安装在世界上任何未分类的区域。通过这种方式,可以使用这种方法设计整个工艺,其可快速生产,并可以选择横向扩展。这种类型的模型与针对一次性技术的Xcellerex FlexFactory 相同。此外,mAb的 CoG 约为 $85/g,而新设施的成本节约预计为 2,500万美元。
对于降低污染风险、暴露于生物危害物质和实时过程条件,一次性实时监控系统等一次性PAT 越来越受欢迎。例如,SciLog Bioprocessing Systems 提供一次性传感器,如SciTemp SciPress 和SciCon 传感器,用于在线温度、压力和电导率监测。
对于培养基、补液和缓冲液制备的应用,Sartorius Stedim Biotech 提供带有内置 pH 和温度一次性传感器的一次性生物工艺设备,例如磁力混合器 LevMixer®。对于低 pH 病毒灭活、pH调节、稀释和产品制剂,Sartorius Stedim Biotech 还提供 Flexsafe 生物反应器,该反应器带有由 ABER Instruments 开发的焊接BioPAT ViaMass 传感器盘,并通过射频阻抗谱测量细胞培养中的细胞密度水平。
一次性技术的局限性
由于一次性工具通常由塑料衍生物制成,因此不可忽视溶出/析出化合物的问题。这包括增塑剂、固化剂和抗氧化剂,它们可能会影响最终产品的质量。此外,由于塑料一次性产品的使用,由于塑料成分混合,回收利用的可能性非常有限,因此引发了对其潜在环境危害的争论。因此,剩下的唯一选择是焚烧和填埋。
其它一些团体表示,与重复使用不锈钢设施相比,一次性技术可以通过以水和清洁剂中的能量形式整体减少碳足迹来弥补这一缺点。具有相同质量的一次性产品的持续供应是另一个问题,因为由于验证和QA 规定,生产需要这种材料的稳健供应。
如上述案例研究所示,其它限制包括在大规模生产(如每年数吨)时经济性较差(一次性生物反应器的最大尺寸一般为 2,000 L,预装填料层析柱限制为 80 cm)。然而,在未来,这些限制可以通过一次性技术的进步来克服。
工艺经济性
使工厂适应新工艺流程的主要挑战包括战略规划、教育用户以及处理新问题。
如上游的情况,与灌流相关的问题已得到解决,并且该工艺变得稳健、简单、可放大且污染风险低。在下游,工艺强化获得了处理更高滴度生产率的优势。与批次工艺模式相比,连续操作的成本降低了 6到 10 倍。反对在上游和下游使用连续生物工艺的评论仅仅是因为成功实施的案例研究的数量有限,并且对该工艺的接触较少。
在今天的 mAb 生产中,为了取得成功,市场不断倾向于一次性技术变革,从而在操作中提供一定的灵活性。这样,人们可以在短时间内以较低的资本成本获得巨额利润(图6.8)。好处包括:
-
劳动力需求少: 由于不需要CIP和SIP,因此也不需要清洁验证。 -
更短的转换时间: 与需要一周时间的不锈钢设施相比,一次性技术使操作员能够在几个小时内使系统为下一批做好准备。 -
减少占地面积: 设施要小得多,最终降低了运行该设施所需的其它公用设施的成本,包括冷却和加热装置、空调等。
每个生物制药公司都希望在他们的管线中拥有创新的分子和/或在患者护理方面大获成功的药物。因此,在这个竞争激烈的世界中,成本效益成为行业的主要支撑。为了在竞争中生存,该行业必须能够根据时间和要求(如工艺强化和灵活的多产品设施设计)接受变化,以更低的生产成本生产药物。
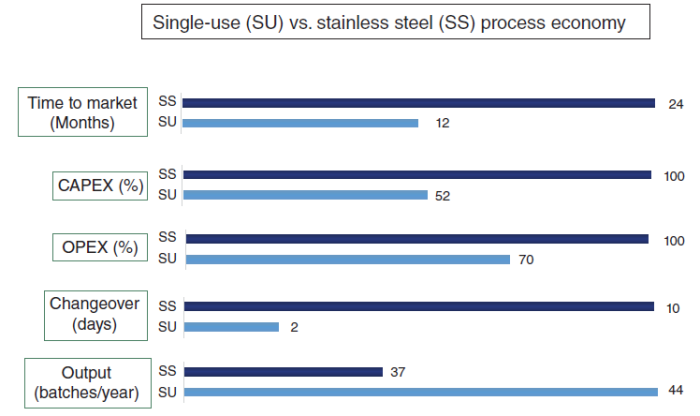
图 6.8 工艺经济性:一次性 vs. 不锈钢设施。
生物制药市场动态
与血浆产品一起,生物制药分子,特别是mAb, 在过去20 年中的市场价值从 110 亿美元增加到 2,300 亿美元。未来一、二十年,mAb生物仿制药将成为市场增长的主要动力。
尽管促红细胞生成素(EPO)和生长激素形式的生物仿制药在市场上已有十年之久,但mAb生物仿制药在获得上市批准后已成为几乎每个细分行业的最高创收分子,一些mAb如此受欢迎,以致于超过 20 家公司正在同时进行这项工作。对于其它即将推出的生物仿制药,这一数字也在不断增加,这表明未来行业之间的竞争将有多么激烈。
新的生物仿制药正在与创新药和现有的生物仿制药进行激烈的斗争,以至于市场上现有的药物正在失去收入。然而,由于严格的监管指南,生物仿制药的批准对行业来说变得困难。与生产工艺陈旧的原研分子相比,新的生物仿制药正在推出改进版本的仪器和工艺,帮助它们降低药物价格并维持市场份额。疗法和分子创新的步伐也为生物制药的未来铺平了新的道路。由于Keytruda、Opdivo等新型抗肿瘤药备受世界瞩目,针对这些分子处于开发阶段的生物仿制药非常多,但主要问题是它们的高价格可能并非所有患者都能负担得起。
除生物仿制药外,基因和 CART 细胞疗法、ADC 和双特异性抗体等创新产品也正在进入市场。细胞和基因治疗的挑战在于它们是针对个体的,其次是它们将作为针对少数患者群体的个性化药物进行少量生产的方式。
新兴市场的关键风险管理
由于无法确定市场动态,因此应如何以及在何处建造生产设施以及达到何种产能是行业的另一个问题。决策基于三个因素:
-
市场碎片化: 如前所述,有些药物是针对小患者群体的,你不知道将来会有多少竞争者。因此,仅根据需求决定生产规模变得非常困难。 -
全球化: 新兴市场是许多生物仿制药可以产生良好收入的地方,许多行业公司希望在这些市场生产他们的药物,因为它提供了一定程度的医疗保障以及经济增长的迹象。 -
需求: 特定药物的需求量是不确定的。在某些情况下,根据需求,可能 <500 kg,而在某些情况下,可能<100 kg。建成的大型设施和低需求将导致高COG。此外,如果设施规模小且需求量大,则可能会错失良机。该设施通常是在监管部门批准之前建造的,不幸的是,如果产品未获批准,该设施可能将不被使用。
因此,要建立一个最佳尺寸的设施,生产商必须牢记上述因素,并确保原材料的持续供应,以满足需求。它还有一些挑战。例如,如果在监管机构的建议下必须进行一些更改,并且如果这样做会使工艺变得昂贵,那么原材料或工艺时间会显著增加,然后COG 就会变高。这就是为什么需要一个稳健的工艺,即使在工艺发生重大变化后也能生产出相同质量的产品。
不仅层析填料、细胞培养基和耗材等工艺成本会加到产品的COG 中,而且很大的成本是包括电力、安全和GMP 认证在内的设施运行成本。这个固定成本是成本的60-70%,无论工艺流程是否运行,它都会继续。解决这个问题的唯一方法是以可控的方式通过工艺强化来提高产量,以免浪费市场上高价值的额外材料,即使只是1%。
随着上游在高滴度方面提高效率,下游也在降低成本,使用具有高结合载量的新填料,并以少量填料更好地去除杂质。现在,这些工艺被设计成这样一个连续和一次性使用模式,它减少或最小化步骤之间的保持时间。
今天,模块化设施的新概念正在推进,可以根据他们的要求为多种产品进行设计。为了降低在生产初期未使用或未充分利用的大型设施的风险,横向规模扩展是一个更好的选择,而不是在单个大型设施内规模放大。规模扩展是指可能有多个小型设施,生产与单个大型设施相同的产品量。
这可以从安进和三星两大生物制药公司树立的榜样来理解。2015年,三星宣布将在韩国仁川松岛建设大型工厂。这将生产 4,500 kg/年,产能为 18 万升,设施成本为7.5 亿美元。另一方面,安进在新加坡建立了一个120,000 平方英尺的模块化小型设施,可以在不同的产品操作之间轻松切换。
根据 BioPlan 发布的 2020 年年度报告,更多的CMO 将在明年评估工艺强化并采用连续的生物工艺(53%将测试 DSP,38%将考虑生物生产设施),而40% 的 CMO 和 28% 的生物制造商希望供应商专注于为他们提供先进的连续上游技术。根据初步数据,今年已经确定了大约20 项受关注的新技术,其中包括一次性生物反应器(45.9%的受访者提及)和细胞培养基优化,其次是上游和下游连续生物工艺。
未来展望
倾向于新的连续生物工艺技术的主要原因之一是在批次工艺模式下上游产品滴度小于 1 g/L。灌流过程克服了这一限制,在灌流工艺中,细胞数保持恒定平衡,细胞培养上清液与新鲜培养基定期交换。然而,这项技术仍有一定的改进空间,因为一些问题还有待解决,例如保持长期无菌条件、增加的工艺时间和成本、生物反应器容器中的不均匀性。
正如 FDA 所建议的,需要高级控制策略来监控复杂性并控制连续工艺,以确保更好的产品质量。为了满足未来对连续生物工艺中监控控制的期望,PAT和自动化工具对于显著减少过程监控所需的时间至关重要。
新的和先进的传感工具(如光谱和软传感器、化学计量学、无线传感器和高级图像分析)的应用支持了向工业的发展,通过这些工具,信息过程监控在连续生物工艺中变得容易。这些设备不同于传统上可用的传感器,如pH 值、压力、流量和温度,它们生成与过程开发状态相关的数据,例如,采用非侵入式仪器粒子技术的无线传感器,即使在扰动的条件下,也可以访问过程数据。
一项研究表明,除了使用无线传感器进行过程监控外,一种新的创新工具是先进的图像分析,当与化学计量学和机器学习算法相结合时,它被证明是发酵过程中持续监控的创新工具。在使用化学计量学处理光谱后,光谱传感器在测试时可以一次感应和记录多种化合物,没有时间延迟。在严苛的生产环境中,红外光谱仪 和拉曼光谱等新研究正在被修改,以供应用。
全球领先的市场研究公司 Meticulous Research 发表了题为“按产品(过滤、层析、生物反应器、离心机)、应用 [商业(单克隆抗体、疫苗生产)、研究] 和最终用户(制药和生物技术、CDMO) - 到 2027 年的全球预测。”根据这份最新出版物,全球连续生物工艺市场预计将从2019 年起以 8.8% 的复合年增长率增长,到 2027 年达到73.3 亿美元。
本文为以下文献内容简介,详细内容,请参考原文。本文旨在知识、信息分享,转载请注明出处和原文。
原文:A.K.Joshi, S.K.Gupta, Single-Use Continuous Manufacturing and Process Intensification for Production of Affordable Biological Drugs. Process Control, Intensification, and Digitalisation in Continuous Biomanufacturing, 2022.
来源:开朗的豌豆射手 生物工艺与技术
责任编辑:胡静 审核人:何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多