制药人员应打破传统思维:抗体药物的亲和力不一定是“越高越好 ”
由于对靶抗原的高度亲和力和特异性,抗体被广泛用作治疗众多疾病的选择。目前已有100多种基于抗体的药物被批准用于人类疾病治疗,涉及单抗、BsAb、ADC药物以及CAR-T细胞产品等。高亲和力对天然产生的和常规的直接靶向治疗性抗体的活性至关重要。然而,近年来发现基于抗体的多类型药物的靶标亲和力并一定是越高越好。
对于一些单抗药物,特别是激动型抗体,例如如肿瘤坏死因子受体CD40和4-1BB,可诱导细胞内信号。与天然抗体和直接靶向抗体不同,激动型免疫调节抗体的作用机制不同,除了特定的靶标参与外,还需要诱导产生有效的受体信号。已知表位、isotype和FcγR engagement共同参与了调节激动型抗体的活性。最近,关于亲和力对于激动型抗体活性的调节也进行了一些研究。
例如,近日在Nature期刊上了发表了题为“Reducing affinity as a strategy to boost immunomodulatory antibody agonism”的研究。通过对CD40, 4-1BB 和PD-1三个免疫受体的研究,发现中等亲和力而不是高亲和力可通过增加clustering提供更强大的激动活性。
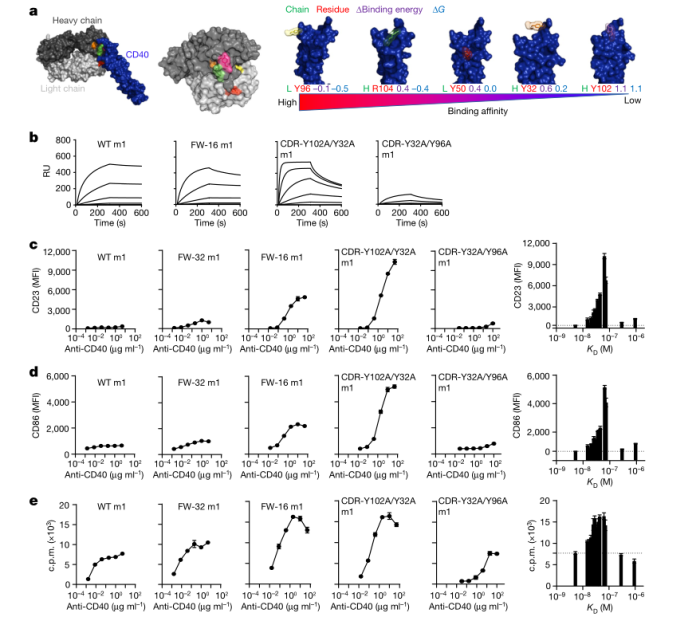
以CD40为例,研究者设计了具有一系列亲和力(5.22-925 nM)的CD40抗体,其具有相同的isotype,并且结合相同的CD40表位。结果发现,亲和力和激动型之间的关系是钟形的,随着亲和力降低,抗体的激动能力增强,但是当亲和力进一步降低时,抗体的激动性减弱,最佳亲和力在50 nM左右。另外抗体的解离速率 (kd), 而不是结合速率(ka),与激动性呈现类似的钟形关系,这表明更快的解离是降低亲和力而增加激动活性的关键。
在4-1BB 和PD-1上也得到了同样的结论。这些发现揭示了增强不同受体家族激活的新范式,为未来激动剂抗体的开发提供了新思路和借鉴意义。
另外,MedImmune的科学家在 PLoS One期刊上发表了题为“Enhancement of Immune Effector Functions by Modulating IgG’s Intrinsic Affinity for Target Antigen ”的研究。该研究发现,抗体与靶抗原的亲和力明显影响Fc介导的效应机制的程度和效率,降低亲和力反而可以使抗体的Fc的效应功能活性明显增强。
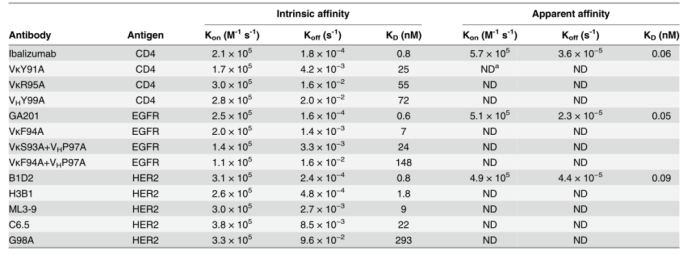
MedImmune的科学家通过使用点突变改造了三种不同单抗的亲和力:抗CD4 ibalizumab,抗EGFR GA201和抗HER2 C6.5。结果证明,在饱和抗体浓度下,1)亲和力的降低可以增强抗体的效应功能(ADCC、ADCP、CDC),但需要一个最低亲和力的阈值;2)介导增强的细胞毒活性的能力与靶细胞上的受体密度无关;以及3)抗体与靶抗原的结合效价明显调节效应功能的程度和效率。
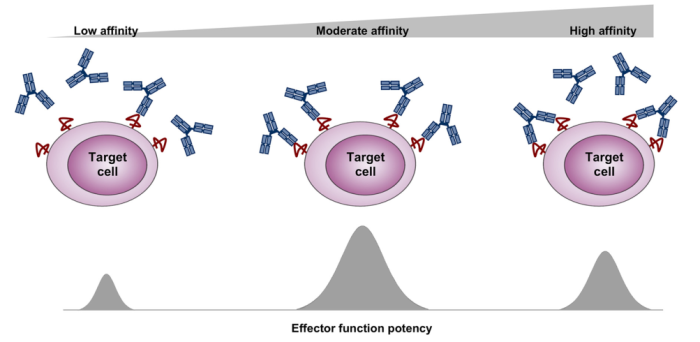
对于该现象的解释,MedImmune的科学家推测,高亲和力抗体由于强大的亲和力效应,能够以二价的形式与靶细胞的两个抗原结合。相反,表现出较快解离率的抗体可能会更快地将单个结合臂从细胞表面解离,导致与靶细胞抗原单价结合的可能性更高。而单价结合将允许更多的抗体分子与靶细胞相互作用,导致结合细胞表面的抗体Fc结构域数量增加。这将有助于改善效应器元件的招募,进而产生更强的活性。然而,在抗体结合亲和力太低的情况下,没有足够的抗体分子与靶细胞结合,与效应细胞的结合也大大下降,进而导致整体效应器活性降低。
靶标亲和力和效应器功能效力之间的这种不可预测的关系表明,对于下一代免疫疗法的开发,应需仔细和谨慎进行抗体分子设计和选择。
对于双特异性抗体(BsAb),可以通过优化BsAb的设计进一步提高治疗窗口。例如,基于CD3的T-BsAb通过将TCR复合体交联并在T细胞和靶细胞之间形成免疫突触来激活T细胞。随后,穿孔素和颗粒酶通过这个突触传递,从而导致靶细胞被杀死。这一过程可以受到多种因素的调节,包括结合臂长度、连接子设计和CD3与靶抗原结合位点之间的灵活性、以及对CD3和靶抗原的亲和力/价态等。
其中一个关键因素是T-BsAb对CD3和靶抗原的亲和力。天然的免疫反应,T细胞识别低亲和力的抗原肽-MHC复合体(KD值约为1-100 µM)。一般抗体对其同源抗原的亲和力通常要高得多,KD在nM范围内。虽然T-BsAb与CD3和靶抗原的结合亲和力较高与T-BsAb的体外效力呈正相关,但这也伴随着T细胞产生的细胞因子的增加以及细胞因子释放综合征的风险增加。理想情况下,设计良好的T-BsAb应能够在不引起过度产生炎性细胞因子的情况下,对靶细胞产生足够的细胞毒作用。
对于T细胞来说,杀伤细胞活性的激活阈值比产生细胞因子的激活阈值低得多。Blinatumomab的CD3结合臂是从OKT3主干发展而来的,其KD已降低到µM范围。Xencor和MacroGenics等公司也开发了基于另一种CD3抗体(SP34)的CD3结合臂。这些新型的CD3结合臂对CD3的亲和力都相对较低,希望使T-BsAb在保持较强细胞毒作用的同时,引起较少的细胞因子释放,从而降低细胞因子释放综合征的风险。
对于ADC药物,解决其肿瘤穿透问题的一种方法是根据抗体与靶抗原的结合亲和力来选择抗体,使其仅呈现在肿瘤表面。较低的结合亲和力可以允许抗体更深地渗透到肿瘤中,因为肿瘤周围的未结合浓度有助于其渗透。
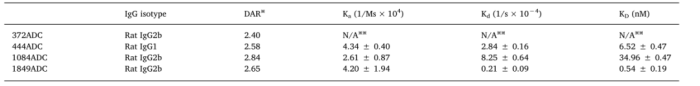
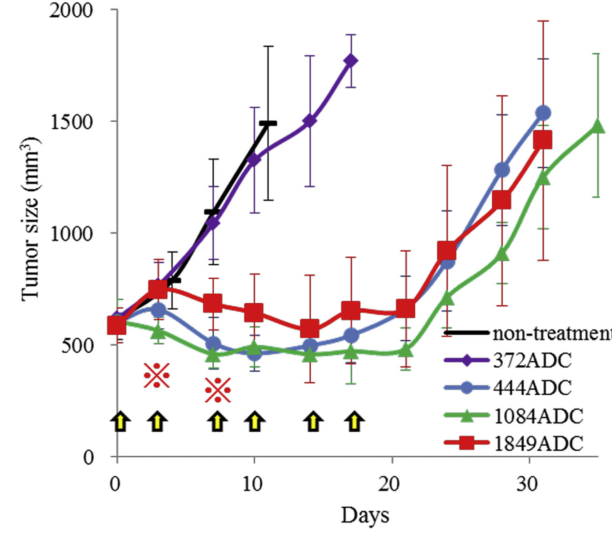
例如,在Journal of Controlled Release 期刊上发表了题为“Influence of the dissociation rate constant on the intra-tumor distribution of antibody-drug conjugate against tissue factor”的研究。TSumura等人建立了三种抗组织因子(TF)的ADC:低KD的1849ADC、中等kD的444ADC和高KD的1084ADC。
这三种抗TF的ADC的体外细胞毒性和药理生化特性基本相同,但结合动力学参数不同。在体内,所有ADC对BxPC3小型肿瘤具有相同的抗肿瘤作用。然而,在较大的BxPC3肿瘤上,低亲和力的1084ADC(高KD)比高亲和力1849ADC(低KD)具有更高的抗肿瘤活性。
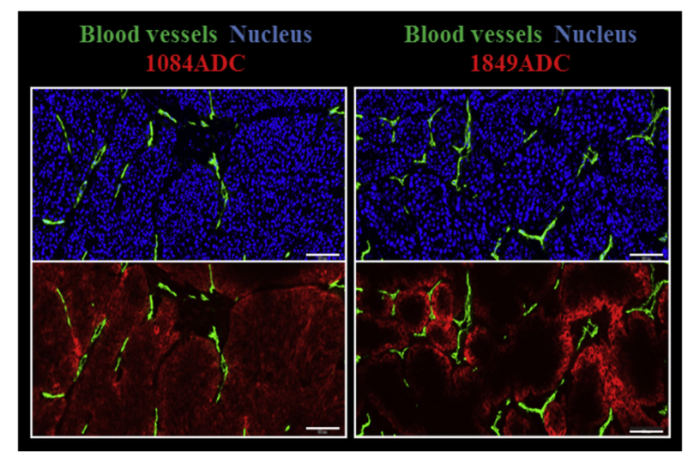
免疫荧光染色显示,1084ADC分布于整个肿瘤组织,而1849ADC主要定位于肿瘤血管附近。因此,具有较高KD的ADC具有更强的抗肿瘤作用,因为它在整个实体瘤中穿透并均匀分布。这些发现突出了抗体的的亲和力在ADC设计中的重要性。
靶点在正常组织中的分布对于ADC药物的抗体亲和力设计也很重要。例如,Trop-2的在正常组织中具有相对较广的分布,不同公司对该靶点的抗体的亲和力进行了不同的设计。吉利德开发的靶向Trop-2 的ADC药物Sacituzumab Govitecan(SG)抗体部分的KD值为0.3 nM,而第一三共的开发的靶向Trop-2 的ADC药物Datopotamab deruxtecan(Dato-DXd,DS-1062a)的KD值为27 nM。两者之间有90倍的差异。第一三共可能选择了一种低亲和力抗体来降低DS-1062a在正常组织中的毒性。当然这种平衡的设计是否会取得更加优异的临床结果还有待观察。
对于CAR T细胞疗法,高亲和力一般是CAR构建的首选,因为它们可以诱导强大的T细胞激活和检测低水平的抗原。然而,目前抗原亲和力如何影响实体瘤CART的抗肿瘤效果依然研究较少。
最近,在Frontiers in immunology期刊上发表的一篇“The affinity of antigen-binding domain on the antitumor efficacy of CAR T cells: Moderate is better”的文章,研究了CAR T的疗效与抗原亲和力的关联。
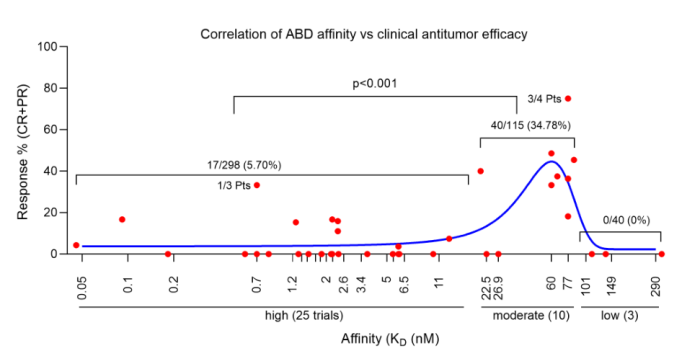
该研究首先分析了38项已发表的实体肿瘤CART试验,并将它们与抗原亲和力的应答率进行了关联。亲和力分为高亲和力(KD<20 nM)、中等亲和力(KD=20-100 nM)和低亲和力(KD>100 nM)。毫无意外,大多数(25次试验)的CAR-T使用了高亲和力的CAR,但却只产生了5.7%的应答率。相比之下,使用由中等抗原亲和力制备的CAR T治疗的患者中有35%有临床反应。当ABD亲和力太低(KD>100 nm)时,CAR T没有临床反应。因此,具有中等抗原亲和力的CART不仅脱靶毒性较小,而且可能更有效。
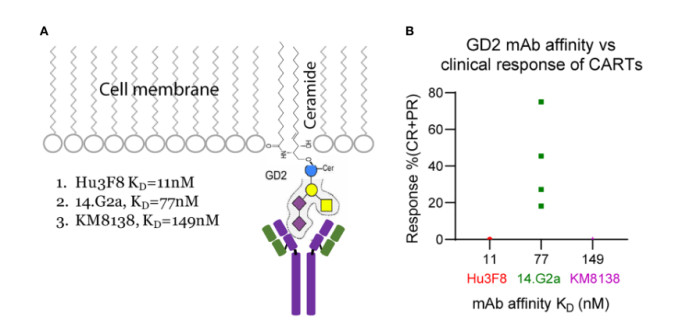
以GD2靶点为例,用于临床开发CAR T的三种GD2抗体具有不同的亲和力,但靶向相同的膜-近端糖基表位。因此,在比较CAR T效率时,表位位置的影响可以忽略不计。在使用中等亲和力抗体14.G2a(KD=77nM)制成的GD2 CAR T进行的四项临床试验中,37名患者中有13名患者出现PR或CR(有效率为35%)。然而,用高亲和力Hu3F8抗体(KD=11 nM)或低亲和力KM8138抗体 (KD=149 nM)构建的GD2 CAR T没有产生临床应答。
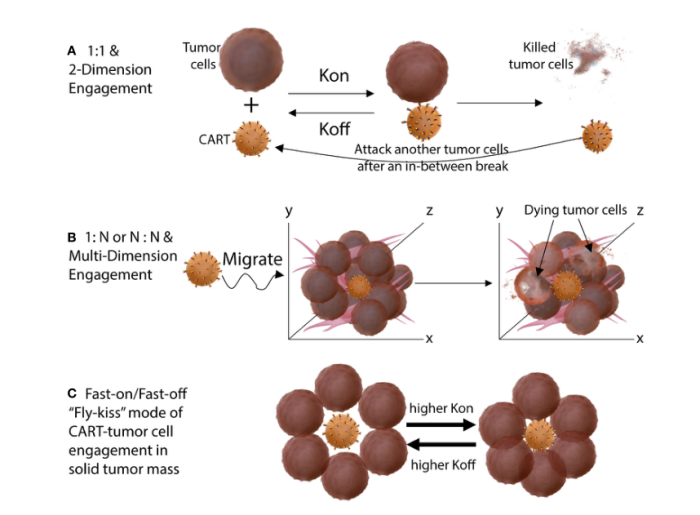
对于亲和力对CART生物学和功能影响的分析,一定程度上解释了适度亲和力对于CAR T效力更好的原因。1)当CART-肿瘤细胞结合太强时,CART难以与被杀死或垂死的肿瘤细胞分离。被占据的CAR T将不能与其他的靶细胞重新结合,并诱导肿瘤细胞的系列杀伤。2) 高亲和力CART与肿瘤细胞的强结合可允许CAR蚕食靶细胞膜的一部分和其他相关抗原。这种trogocytosis过程将会引起CAR T的自相残杀。另外trogocytosis还会由于靶细胞上的抗原丢失而导致肿瘤逃逸。3) 高亲和力CAR T与肿瘤细胞的强烈和持续接触可能导致CAR T耗竭和细胞死亡。而中等亲和力CAR T可能耗竭较少。4) CAR的抗原亲和力影响CART的多功能性。例如,使用CyTOF技术,比较FMC63(高亲和力)和CAT(中等亲和力)CD19 CAR T的研究发现,在与CD19+肿瘤细胞结合后,CAT CD19 CAR T包含的多功能T细胞明显多于FMC63来源的CAR T。这表明中等亲和力的CAR可能允许CAR T保留其多功能性,这对于抗肿瘤效果是重要的。5) CAR的抗原亲和力影响记忆T细胞的形成。中等亲和力的CART包含更多的记忆T细胞,并且在实体肿瘤中持续时间更长。6) 亲和力降低有助于CAR T基于抗原定量差异将肿瘤细胞与正常细胞区分开来,有助于肿瘤的选择性靶向。
最后,研究人员提出,实体肿瘤中CART-抗原结合的快开/快关(high Kon和Koff)动力学将允许CAR T产生足够的信号来杀死肿瘤细胞,而不会产生耗竭。
因此,研究CAR 的抗原亲和力和CAR T-肿瘤相互作用的动力学也将是设计CAR T有效治疗实体瘤的关键。
小结
近年来,对于基于抗体的多类型药物的亲和力与疗效和治疗窗口的关联进行广泛的研究。众多的研究结果这打破了人们的传统思维,抗体的亲和力并不一定是越高越好,这需要研发人员更加深入的了解靶点的信号通络以及抗体的详细作用机制,这也对制药企业和研究人员对抗体的开发和设计提出了更高的要求。













评论
加载更多