创新速递|“魔法子弹”ADC药物筛选全解析
复杂的ADC胞内毒素传递过程的第一个阶段是ADC药物的内吞,分析靶受体和ADC的内吞作用可以极大地促进临床前研究、临床转化和患者治疗效果。
2017~2020年是ADC药物快速发展的时期。2017年上市的奥英妥珠单抗Besponsa用于治疗复发或难治性前B细胞急性淋巴细胞性白血病; 次年,莫塞妥莫单抗作为一种冻干粉剂的ADC药物上市;2020年4月,Trodelvy获得美国FDA加速批准,是FDA批准的第一个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个以Trop-2为靶点的ADC药物。
随后ADC药物发展进入成熟期。2020年1月,T-DM1获得NMPA批准在中国上市,开启了中国ADC药物元年,2022年4月24日,阿斯利康&第一三共联合开发的德喜曲妥珠单抗(DS8201)在中国申请上市。两年时间,中国ADC药物市场从无到有,快速加入全球ADC药物市场。

▶3.1. 销售额



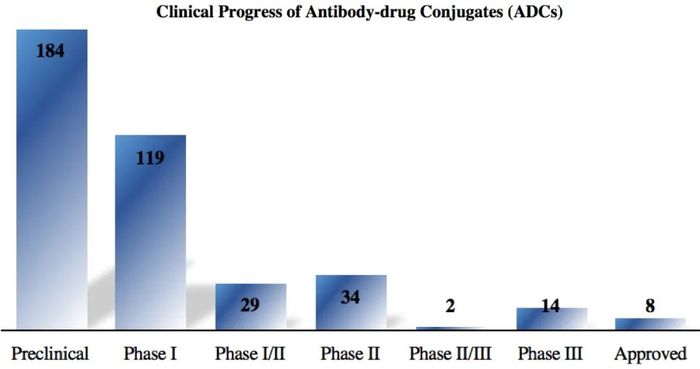
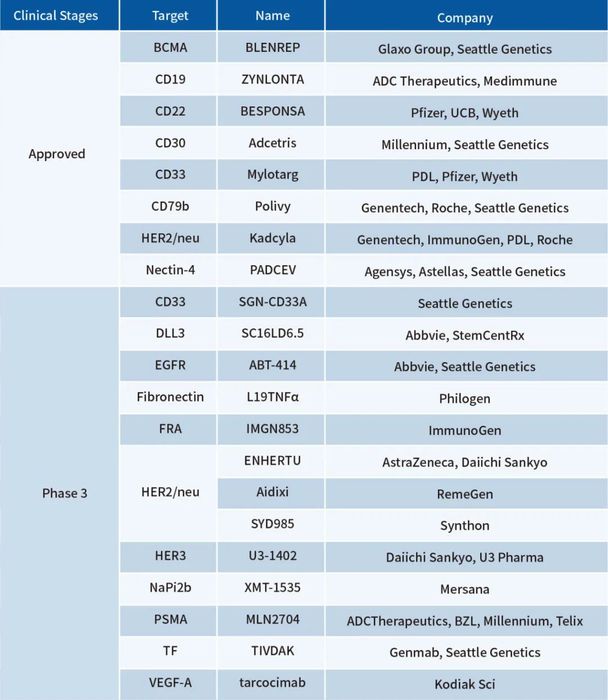

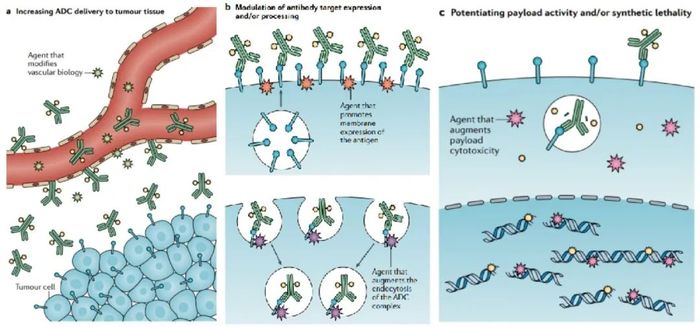

4) ADC小分子毒性:高效的药效学作用,无免疫原性,通过修饰能与连接子结合。如何鉴定抗体的内化是ADC项目推进的关键。
邵丽竹
何发
热点文章
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
微生物发酵技术在植物活性成分提取中的应用研究进展
2026-03-06
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多