一文读懂单抗开发关键质量属性——糖基化修饰
本文将重点介绍半乳糖、岩藻糖、高甘露糖、N-乙酰神经氨酸(NANA)和N-糖基神经氨酸(NGNA)等不同糖型对抗体的安全性/免疫原性、有效性/生物活性和清除性(药效学/药代动力学性质(PD/PK))的影响。此外,本文还将总结常规的分析技术,如亲水作用层析(HILIC)、高效阴离子交换层析-脉冲安培检测(HPAEC-PAD)和质谱仪(MS)用于表征和监测单抗的糖基化。
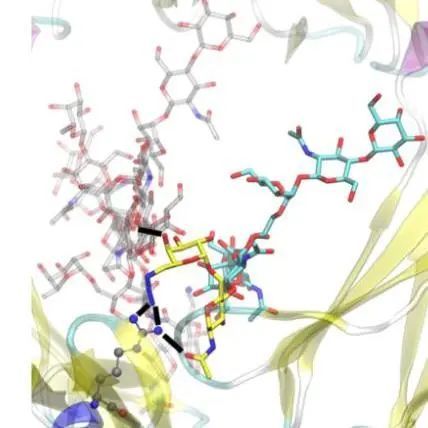
治疗性抗体两种基本类型的蛋白质糖基化:
IgG是人体血清中含量最丰富的一类免疫球蛋白,占血清总免疫球蛋白的75%。IgG由抗原结合部位片段(Fab)和可结晶片段(Fc)组成,Fc与细胞表面受体(FccR)和补体系统组件(C1q)相互作用,介导抗体效应功能,包括ADCC、CDC和吞噬作用。在人类中,存在四种不同的免疫球蛋白亚类,包括IgG1、IgG2、IgG3和IgG4,它们在结构、抗原结合部位和结合亲和力上各不相同。目前为止,大多数已被批准的治疗性抗体属于IgG1类,通过中和作用、ADCC或CDC的作用机制来抑制靶分子的病理生理功能。
► N连接的糖基化
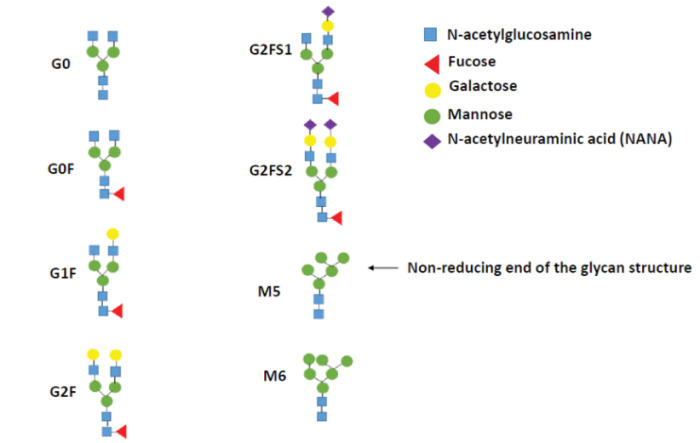
图1 单抗中常见的N-糖基化修饰化学结构(图片来源:参考文献2)
N连接的糖基化是将含14个单糖的糖链(大多数真核生物中的Glc-3-Man-9-GlcNAc-2)通过N-糖苷键从类异戊二烯脂质载体焦磷酸多利酚转移到蛋白质天冬酰胺的酰胺基团上,直接与N原子连接。
N-连接的糖链合成起始于内质网,完成于高尔基体。
►O连接的糖基化
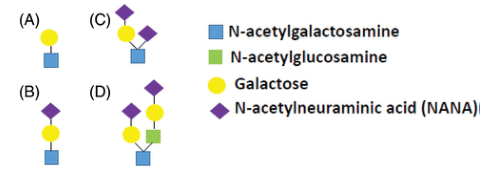
图2 O-糖基化(A-D)的化学结构,通常存在于单抗和融合蛋白中(图片来源:参考文献2)
O连接的糖基化将N-乙酰半乳糖胺作为第一单糖,逐次地添加到丝氨酸(Ser)和苏氨酸(Thr)侧链的羟基。
O-连接的糖基化在高尔基体中进行。
表1 真核生物蛋白质N-连接糖基化和O-连接的糖基化的差异。

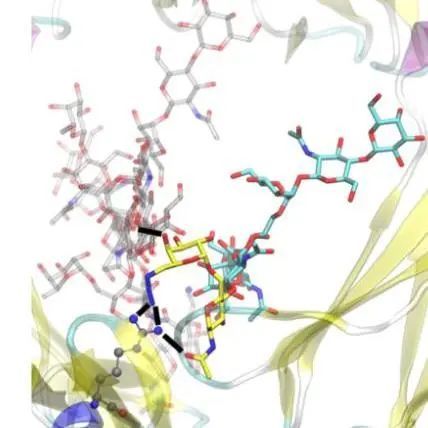
糖基化对治疗性抗体药物功效的影响
►岩藻糖基化
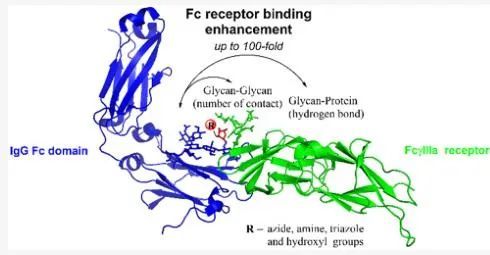
图3 通过岩藻糖基化修饰Fc和Fc受体之间的糖链接触数量增加(图片来源:参考文献1)
抗体的ADCC活性高度依赖于Fc寡糖链中的岩藻糖水平,而与核心岩藻糖化水平成反比。研究证明,IgG1中的岩藻糖基化(或去除核心岩藻糖,G0-G1,G2)可增强其与FccRIIIa的结合能力,提高ADCC活性。在同一研究中,缺乏岩藻糖对FccRI、FccRIIa和FccRIIb类受体和补体成分1q(C1q)的结合却几乎没有影响。
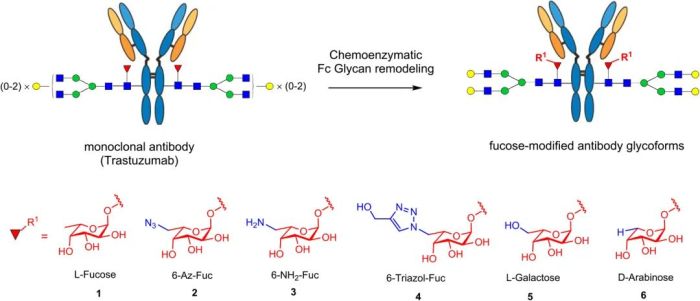
图4 用化学酶方法对单抗核心岩藻糖进行定点修饰(图片来源:参考文献1)
通过X射线结晶学分析,证明了独特的碳水化合物-碳水化合物相互作用以及新形成的氢键和范德华力有助于增加Fc和糖基化受体之间的结合。最新研究发现,用6-叠氮或6-羟基-L-岩藻糖(L-半乳糖)取代核心L-岩藻糖,会增加Fc和Fc受体之间的糖链接触,显著增强抗体对Fc-γRIIIa受体的亲和力,并显著提高其ADCC活性。
► 半乳糖基化
另一种会显著影响抗体药物治疗功能的糖基化是末端半乳糖基化。研究证明,抗体药物去半乳糖会抑制CDC功能,与半乳糖激化的单抗相比活性降低了一半。然而,去半乳糖化和半乳糖化并不影响ADCC活性。
增加C1q蛋白与抗体Fc结构域的结合可促进半乳糖基化,提高CDC活性。与果糖相比,半乳糖化对ADCC活性的影响很小,果糖糖基化是ADCC活性的主要驱动因素。
► 高甘露糖基化
高甘露糖(甘露糖5、甘露糖-M5、甘露糖6、甘露糖-M6等)是寡糖结构,结合到的蛋白的非还原末端。有多项研究表明,在抗体中含有高甘露糖多糖结构能够在体内更快被清除,从而影响单抗的药代动力学。高甘露糖型不影响药物的清除能力,但是与其他形式的甘露糖(G0F、G1F和G2F)相比,甘露糖-M5在人体内清除更快,这对疗效有不利影响,应谨慎将其用于抗体药物的治疗。
► N-乙酰神经氨酸(NANA)和N-糖基神经氨酸(NGNA)
唾液酸也称神经氨酸,是一种带负电荷的亲水分子,通常以两种形式存在:N-乙酰神经氨酸(NaNA或Neu5Ac)及其N-糖基神经氨酸(NGNA),它是由N-乙酰基上的氢原子被羟基取代而生成的。
唾液酸或神经氨酸是9-碳羧化形成的2-酮糖,在单克隆抗体中以α-2,3和α-2,6的连接方式连接到末端的半乳糖上。唾液酸化通过降低ADCC活性、增加体内半衰期、降低稳定性和蛋白质的靶结合来影响其理化性质和生物活性。研究表明,Fc唾液酸化会使IgG与FccRIIIa受体的结合减弱,从而降低ADCC活性。
此外,N-乙酰神经氨酸存在于大多数非人类哺乳动物中,人类缺乏有活性的CMP-N乙酰神经氨酸羟基酶基因(CMAH)。CMAH基因可将CMP-NANA转化为CMP-NGNA,导致NGNA转移到N-连接的糖蛋白的半乳糖残基。因此,注射含有NGNA的抗体可能会诱发免疫反应,从而对药物的药代动力学或生物活性产生负面影响。
糖基化分析方法及优缺点
糖类结构的多样性和复杂性使得从复杂的寡糖混合物中分离、鉴定和量化单糖成为一项相当具有挑战性的任务。结合化学和生物化学,研究人员在产品开发的不同阶段采用了大量的分析方法对糖类进行结构表征。
在特定的糖类应用中,方法的选择取决于样品类型、样品的数量、技术和设备的可及性、方法的效率、成本和所需信息的种类。这些分析技术不仅可以确定成品药物物质和药物产品的实时质量属性,还可以在单克隆抗体开发的早期阶段进行质量鉴定,如克隆选择和工艺优化,特别是在蛋白质滴度较低或蛋白质样品中的杂质分析方面。
下面,将总结开发抗体药物过程糖类结构分析方法及优缺分析:
表2 抗体药物开发过程糖类结构分析方法及优缺点概览


结 论
单克隆抗体是由单一B细胞克隆产生的高度均一的抗体,由于单抗能够识别并结合相同或不同抗原表面上的特定表位,因此已被用作治疗肿瘤、皮肤科、眼科和血管疾病等多种疾病靶点的分子。2017年至2023年,全球单抗治疗药物市场预计将以约12.5%的复合年增长率增长,到2023年底,收入将达到2189.7亿美元。
抗体是天然糖基化,这种糖基化模式在决定抗体的结构和效应功能(如ADCC、CDC)及其药代动力学/药效学特性方面起着关键作用。由于糖基化因物种而有所差异,而且细胞培养条件的微小变化也会对抗体的治疗行为产生重大影响,因此在开发早期就必须对mAbs的糖基化模式、糖基形式的组成和糖基化的部位进行详细的描述和彻底的分析。
参考文献:
1.Li C, Chong G, Zong G, Knorr DA, Bournazos S, Aytenfisu AH, Henry GK, Ravetch JV, MacKerell AD Jr, Wang LX. Site-Selective Chemoenzymatic Modification on the Core Fucose of an Antibody Enhances Its Fcγ Receptor Affinity and ADCC Activity. J Am Chem Soc. 2021 May 26;143(20):7828-7838. doi: 10.1021/jacs.1c03174. Epub 2021 May 12. PMID: 33977722; PMCID: PMC8283798.
2.Kaur H. Characterization of glycosylation in monoclonal antibodies and its importance in therapeutic antibody development. Crit Rev Biotechnol. 2021 Mar;41(2):300-315. doi: 10.1080/07388551.2020.1869684. Epub 2021 Jan 11. PMID: 33430641.
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多