武装CAR-T:临床试验中的Armour设计
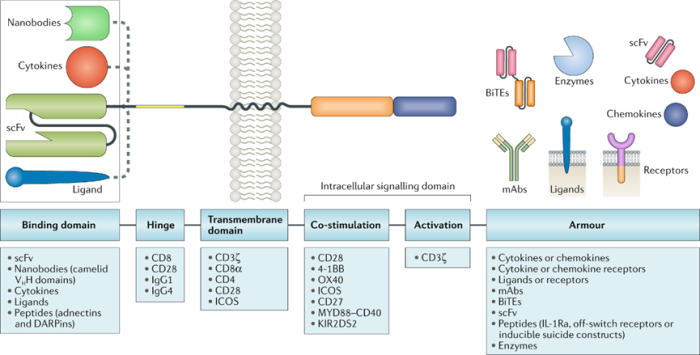
图1 CAR设计蓝图
下面就来介绍一下临床试验中的Armour设计,以及正在临床试验中的相关产品。
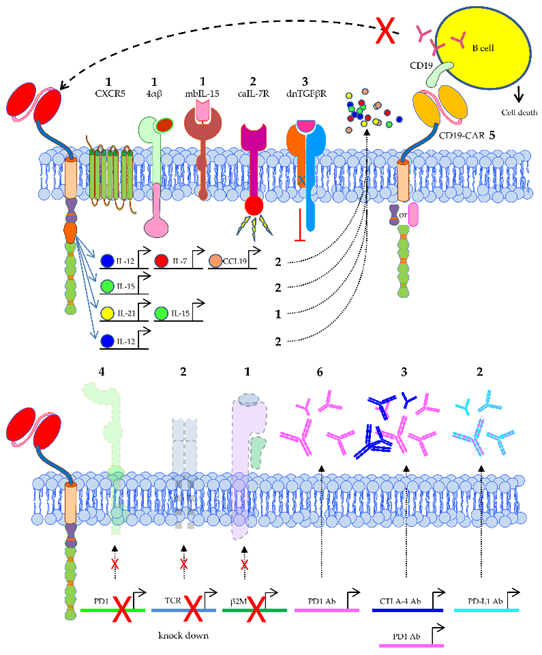
图2 用于治疗实体瘤的临床试验中采用Armour设计的CAR-T细胞
①Armour:细胞因子(IL-12、IL-7、IL-15)、趋化因子(CCL19、CXCR2、CXCR5)
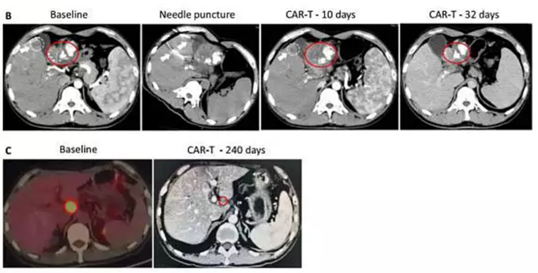
昭泰医疗:IL-7 × CCL19(NCT031985546)
他们在靶向胰腺癌和肝癌,这两个实体瘤的靶点上面做了6例病人研究,1例胰腺癌达到CR(1/6, 16.7%),1例肝癌患者达到PR(1/6, 16.7%),2例SD(2/6, 33.3%),疗效不错。
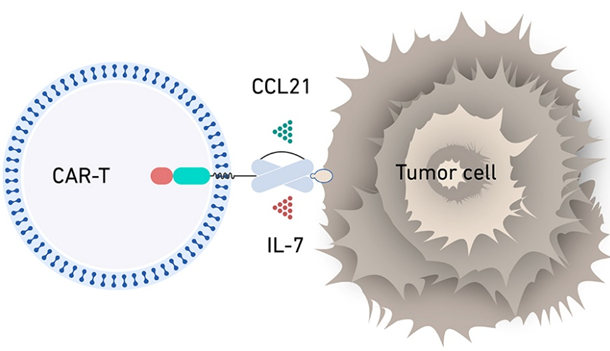
科济:IL-7× CCL21(CycloCAR-T平台)
CycloCAR-T细胞,通过设计表达细胞因子IL-7和趋化因子CCL21,有望显著增强针对实体瘤CAR-T细胞的疗效。
IL-7 作为一种细胞因子,可以增强CAR-T细胞的增殖和存活,而 CCL21作为一种趋化因子,可以驱动淋巴细胞和树突状细胞募集到肿瘤部位。
在体内研究中,CycloCAR-T细胞显示出优于传统CAR-T细胞或7x19 CAR-T细胞(共表达IL-7和CCL19)的优越治疗效果。
Alaunos:mbIL-15(NCT04844086)
白细胞介素-15(IL-15)是一种稳态细胞因子,支持T细胞和其他免疫细胞(例如NK细胞)的存活,并在其受体(IL-15受体-α)的背景下反式呈现。
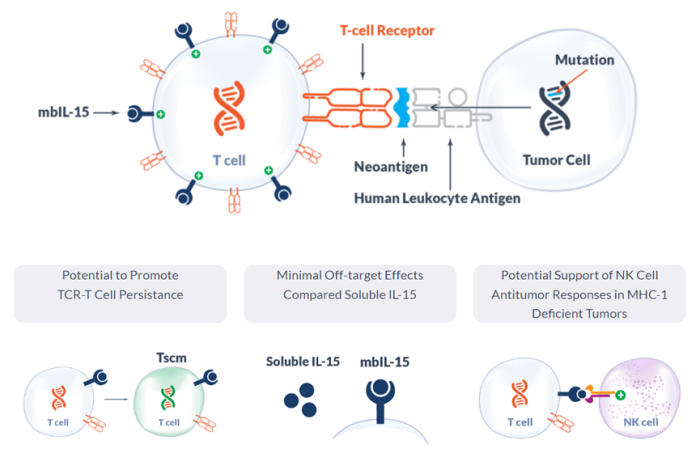
Alaunos 已经开发出新抗原特异性 TCR 与专有的膜结合IL-15 (mbIL-15) 共同表达,以模拟 IL-15 反式呈递,从而提高输注 TCR-T 细胞的存活率和持久性。在临床前研究中,mbIL-15促进了能够在没有外源性生长刺激的情况下存活的长寿命T干细胞记忆(Tscm)细胞的发展;在再刺激时,这些细胞分裂产生效应TCR-T细胞,具有介导肿瘤杀伤的潜力。此外,通过将IL-15分子拴在T细胞表面,可溶性全身IL-15给药观察到的脱靶毒性概率降低。
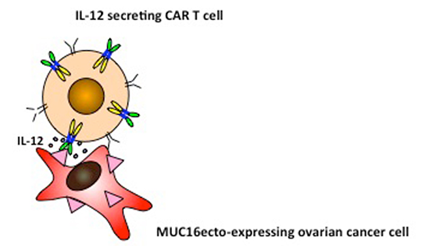
MSKCC:IL-12(NCT02498912)
在I期卵巢癌研究NCT02498912中,患者自身的T细胞被基因修饰以靶向MUC16ecto肿瘤抗原并分泌IL-12,克服实体瘤微环境的抑制作用,促进输注的CAR-T细胞的增殖,并增强肿瘤部位的免疫反应。
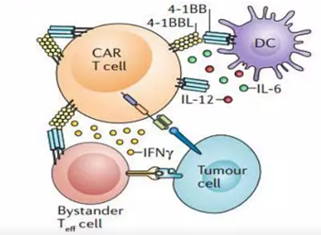
②Armour:共刺激信号(4-1BBL、OX40)
MSKCC:EGFRt/19-28z/4-1BBL CAR-T (NCT02315612)
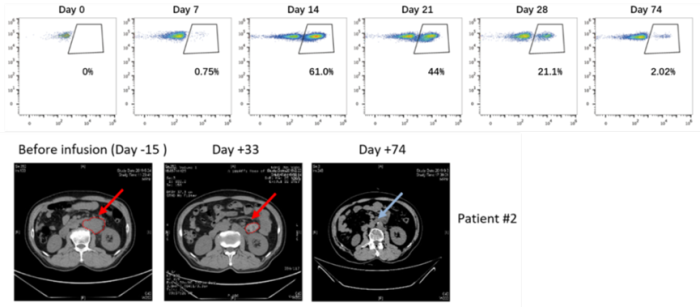
上海隆耀生物:20BBZ-OX40 CAR-T (NCT03576807)
对难治复发转移性B细胞淋巴瘤患者进行初步临床试验,5例患者均完成20BBZ-OX40 CAR-T细胞治疗,有效率100%,其中2例完全缓解,3例部分缓解。
③Armour:转录因子
通过Cas9技术进行全基因的筛选,通过敲除或者高表达,确定引起T细胞exhausting或者persistent显著变化的基因。
NR4A/TOX、C-JUN
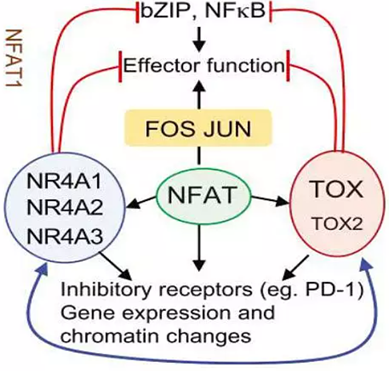
BATF/IRF4、Regnase-1
19年,研究表明敲除Regnase-1后T细胞增殖水平显著提升,对机理的研究发现Regnase-1调控的BATF的表达水平。
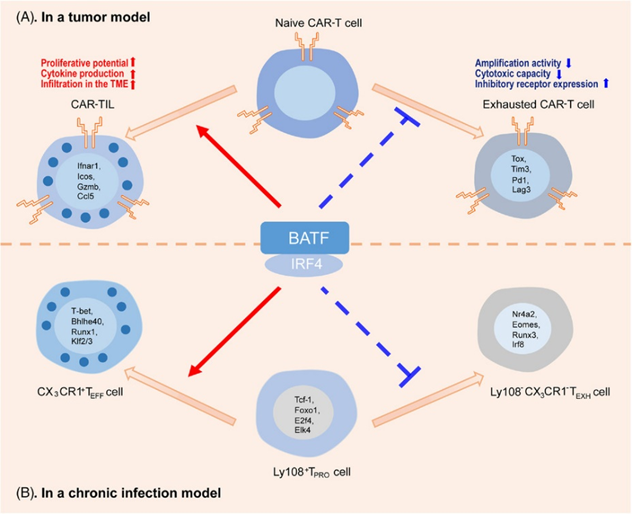
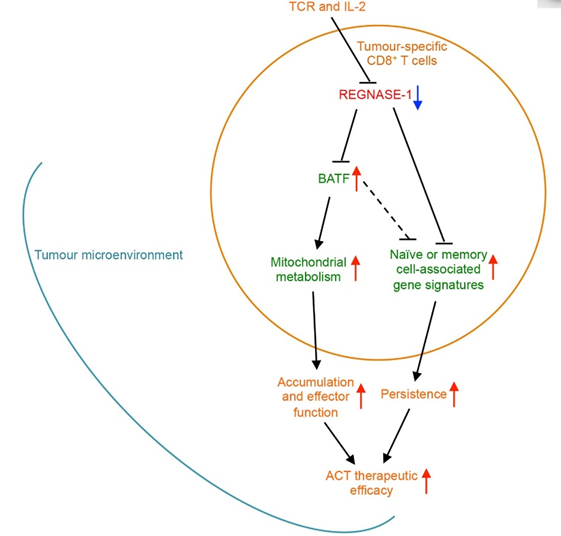
④Armour:肿瘤浸润(FAP)
趋化因子受体或靶向基质
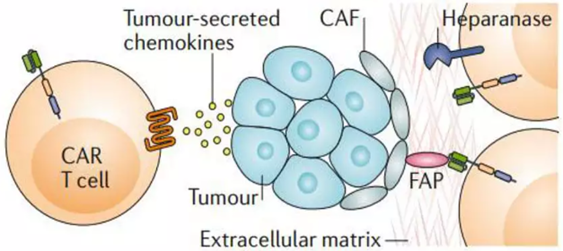
华夏英泰:GPC3 STAR-CXCR2
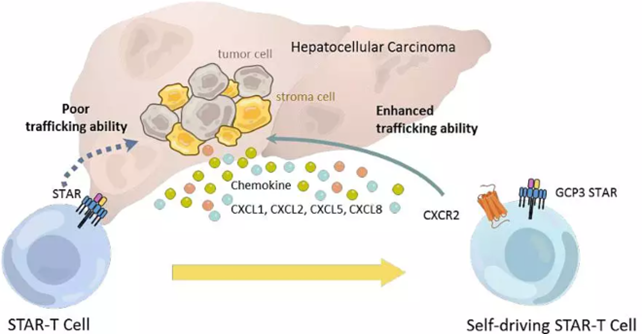
⑤Armour:肿瘤抑制性微环境(PD-1、TGFβ、IL-4)
Atara:PD-1-DNR
Atara正在开发一种用于晚期间皮瘤的间皮素靶向自体CAR-T(ATA2271),并且还在开发一种针对中皮素的同种异体CAR-T免疫疗法(ATA3271)。
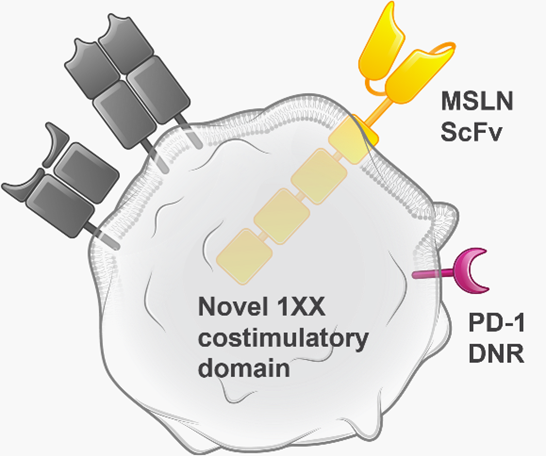
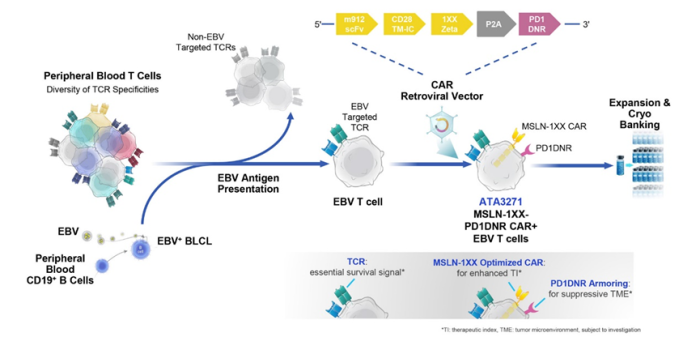
文章来源于BiG生物创新社
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多