PDE 在药品共线风险评估中的应用探索
药品多产品共线生产的质量与安全管控是制药行业面临的重要课题。每日允许暴露量(PDE)评估作为核心技术支撑,对共线生产风险识别与控制具有关键意义。本文基于风险管理理念,系统构建了药品共线生产风险评估体系:首先明确了 PDE 的获取方式及多文献数据差异的优先级判断原则,在此基础上从法规符合性、产品预定用途、产品特性、共线产品厂房设施设备四个核心维度开展全面评估。其中,法规符合性评估依据 GMP 及相关指南明确了禁限共线品类及不同 PDE 值产品的生产要求;产品预定用途评估聚焦于药物相互作用及氧化还原反应风险;产品特性评估重点分析物料特性、活性 /毒性及残留限度计算;厂房设施设备分析则从多风险点识别出发确定共线可行性。结合小容量注射剂生产实践,进一步制定了涵盖生产线管控、清洁验证 / 确认、品种动态管理、多区域污染控制及 OEB/PDE 层面的全链条控制策略。研究表明,该评估体系与控制策略可有效降低共线生产的污染、交叉污染及混淆风险,保障药品质量安全。但受产品特性复杂性影响,风险评估在量化预测方面仍存在局限性,未来需通过积累更多生产数据、深入研究产品特性影响机制以提升评估精准性。
Part
0
前言
每日允许暴露量(英文 Permitted Daily Exposure,简称 PDE)是指在人的终生时长内,药物或产品每日可接受的最大摄入量。对于制药企业而言,在生产线引入新产品时,均需计算、审核和评估药品 PDE,一是确认该产品 PDE 是否科学、权威、专业,二是判断引入该产品是否能与现有生产线产品共线生产,三是用于制定设备清洁残留限度、杂质限度、生产环境残留物限度的可接受标准。
制药企业多数会采用委托第三方权威机构或毒理学专家计算,或通过权威监管机构文献等方式获取 PDE。在实际毒理评估工作中,如果同一物质在多份文献中出现且数值不一致或存在差异,通常会按照文献的权威性、数据原始程度、GLP 合规程度来进行优先级判断。
开展药品每日允许暴露量(PDE)评估时,首先应充分收集药品活性成分的非临床试验数据和人体临床使用数据。接着,通过数据评估识别关键效应,并选出相应的毒性起始点(PoD)。然后,根据相关指导原则和本标准的评估原则设置调节因子及其他因子,并依据公式计算得到 PDE 数值。这一流程确保了 PDE 评估的科学性和准确性,为药品的生产、研究和检测活动提供风险评估和管理的依据。
Part
1
基于风险管理的药品共线生产风险评估
启动的共线评估报告 [1] 应包含法规符合性、产品工艺、产品预定用途、产品基本信息以及残留限度(含溶解度最差、PDE 最小、残留限度最小)、共线产品厂房 / 设备 / 设施共用等多个方面。首先需要收集共线评估信息,包含的内容有:剂型、产品规格、最小 / 最大批量、给药途径、临床适应症、药理作用、用药禁忌、配伍禁忌、用药对象、用药剂量、长期用药(药品在体内是否蓄积并产生毒性)、产品类别、活性成分通用名或化学名、致敏性、活性微生物、原辅料性状(包含颜色、气味、状态等)、原辅料溶解度、毒理相关数据(毒性试验数据、ED50、LD50、PDE/ ADE、OEL 等)、清洁剂等。共线评估的风险评估方法采用 ICH Q9 的工具进行,本文不进行阐述。
根据《药品共线生产质量风险管理指南》[2] 规定,PDE ≤ 10 μg/ 天(具有细胞毒性类)的化学药品目前只能在高毒性药品专用生产车间生产;PDE ≤ 10 μg/ 天(无细胞毒性)的产品不能在普通化药车间共线生产,生产时需用专用设备(如采取一次性配液系统);PDE在 10 ~ 100 μg/ 天(包含 100 μg/ 天)范围内,若为在研产品的试制批、临床试验用药品,应执行清洁残留分析方法的转移确认或验证、清洁确认;若为在研产品的验证批,应执行清洁残留分析方法的转移确认或验证、清洁验证;若为商业批,按照已有的清洁验证参数执行清洗,并进行定期清洁再验证。除以上措施外,还会采取阶段性生产方式,若有必要可采取一次性配液系统或对直接接触药液的器具进行专用化、限定化排产等。
PDE 报告至少包含以下内容:(1)物质一般信息:化学性质、化合物名称、CAS 号、相关理论数据等;(2)化合物的药理作用机制(MOA)及适应症;(3)非临床数据:药理学和安全药理学数据、药物动力学和代谢、毒理数据、单剂量毒性、重复给药毒性、基因毒性、致癌性、发育和生殖毒性、局部耐受 /(皮肤)致敏;(4)人类的数据:人的治疗剂量(所有适应症、途径和患者人群,包括使用的易感人群、最低药理活性剂量)和 / 或临床试验数据、药物代动力学和药物 - 药物相互作用、临床试验 / 治疗使用中的不良反应,包括禁忌症和注意事项、妊娠和哺乳期资料;(5)PDE/ADE 详细计算过程;(6)PDE/ADE 详细选择过程和结论;(7)参考文献和参与评估的专家列表。
开展药品每日允许暴露量(PDE)评估时,首先需充分收集药品活性成分的非临床试验数据和人体临床使用数据。接着,通过数据评估识别关键效应,并选出相应的毒性起始点(PoD)。然后,根据相关指导原则和本标准的评估原则设置调节因子及其他因子,并依据公式计算得到 PDE 数值。这一流程确保了 PDE 评估的科学性和准确性,为药品的生产、研究和检测活动提供风险评估和管理的依据,图 1 所示为 PDE 评估的一般流程。
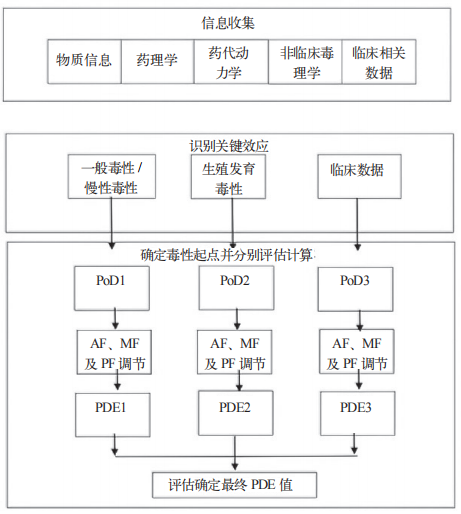
图 1 PDE 评估的一般流程 [3]
Part
2
PDE 在产品特性中的评估
产品特性评估是通过比对拟共线生产的多个产品的各项特性,以评估是否具备共线生产的可能性。拟共线生产品种特性相似或相近,可多产品共线;若拟共线生产品种特性具有特殊性,则不可多产品共线。产品特性评估主要包括以下内容。
(1)将产品类别、生产过程中所用物料的特性 [4](包括物料状态如粉末、液态、固态、性状如颜色、气味、黏度,溶解度等具体数据)输出至车间原辅料溶解度信息表,对比各产线上品种的物料差异性。存在特殊性质(如溶解度较差不易清洗)的品种,应执行清洁残留分析方法的转移确认或验证、清洁确认或清洁验证等风险控制措施。
(2)对产品的活性 / 毒性(如是否具有细胞毒性、致癌性,PDE/ADE、OEL、TTC 等)、致敏性、活性微生物(疫苗或病毒)进行评估。依据《药品共线生产质量风险管理指南》的要求,化学物质基于健康的暴露限度(HBEL)在评估清洁残留数据时更具科学性和优势。在评价 HBEL 时,每日允许暴露量(Permitted Daily Exposure,PDE)及每日可接受暴露量(Acceptable Daily Exposure,ADE)是被普遍接受的标准。将产品的 PDE(若无 PDE,需提供药理毒理资料)及最大日剂量等数据输出至车间产品基本信息表。若无 PDE,则需根据最严格的毒理学关注阈值 TTC 值 1.5 μg/ 天进行计算,该标准源自 ICH M7(R1):评估和控制药物中DNA 反应性(致突变)杂质以限制潜在致癌风险。随后,对比各产线上的 PDE 最小品种,对产线中 PDE 最小的品种执行清洁残留分析方法的转移确认或验证、清洁确认或清洁验证等风险控制措施。
(3)引入品种采用最科学的方法(PDE 法)计算最小允许残留总量,将共线评估需求表中已有信息(如产品最大日剂量、批量、理论浓度等数据)输入至车间计算矩阵表,并由另一人复核输入数据的正确性。同时使用传统方法“1/1000 最低日剂量法、10PPM”计算最小允许残留总量。若传统方法计算的残留总量低于 PDE法,如有必要,可将传统方法计算的残留限度作为警戒限;若传统方法计算的残留总量高于 PDE 法,则继续沿用 PDE 法作为最小允许残留总量。
Part
3
清洁验证 / 确认中 PDE 的应用控制策略
基于 PDE 值的清洁验证控制策略的核心在于根据化合物的毒理学数据、产品类型及生产阶段,实施分级管理与动态调整,具体应用体现在以下几个方面。表 1所示为不同 PDE 值产品的清洁验证控制策略举例。
表 1 不同 PDE 值产品的清洁验证控制策略举例

(1)对于上市产品,应根据产品的年度质量回顾及评估制订清洁再验证周期 [5]。对于 10 μg/ 天<PDE ≤ 100 μg/ 天的品种,应在阶段性生产的最后一批执行清洁效果确认;对该产线上市产品中条件最差的品种,每半年执行一次清洁效果确认。根据产品的生产工艺,应对涉及的工序中最难清洗的部位进行评估并确定取样位置(如称量器具表面、配液罐排放口、配液罐的搅拌桨、滤壳、分液器最远端、陶瓷泵、灌装针等)进行淋洗水或擦拭取样,检测项目包括但不限于目视检查、活性残留、微生物限度、总有机碳(TOC)、电导率等。
(2)对于在研产品(试制批、验证批),均需执行清洁确认或清洁验证品种。此外,还需执行清洁残留分析方法的转移确认或验证。对于同品种、同工艺的产品,若在产线上已有品种进行清洁验证,则可视为拟引入的品种已执行清洁验证,但后续转商业化生产时需重新评估。
(3)对于临床试验用药品,每批次均需执行清洁确认,后续转商业化生产时需重新评估。
(4)首次进行清洁验证或确认时,需根据产品的生产工艺,对涉及的工序中最难清洗的部位进行评估并确定取样位置进行淋洗水或擦拭取样;在进行再验证或再确认、阶段性生产清洁确认时,可根据首次清洁验证或确认的情况对最难清洗部位进行取样评估。取样检测项目包括但不限于活性残留等项目。
Part
4
基于 OEB/PDE 层面建立控制策略举例
为将基于 OEB/PDE 的风险分级原则转化为具体、可执行的控制方案,可依据不同的 PDE 范围,对生产线的使用策略及清洁验证等控制措施进行差异化设计,具体示例如表 2 所示。
表 2 基于 OEB/PDE 层面建立控制策略举例

Part
5
结论与展望
风险评估和控制策略是药品共线生产在小容量注射剂中实践的关键 [6]。在风险评估方面,通过准确计算药品每日允许暴露量(PDE),全面评估法规符合性、产品预定用途、产品特性以及共线产品厂房设施设备等因素,可以有效识别共线生产中的风险点。在控制策略方面,制定科学合理的生产线控制策略、清洁验证 / 确认的控制策略、生产线品种动态管理策略,以及从生产区、仓储区、检验区层面和基于 OEB/PDE 层面建立控制策略,能够有效降低风险,保障药品质量和生产安全。
在风险评估的精准性上,虽然采用了多种评估方法和工具,但由于共线生产涉及的因素复杂多样,不同产品的特性差异显著,如活性成分的结构、稳定性和代谢途径各不相同,使得风险评估在量化和预测风险方面仍存在一定的局限性。应进一步深入研究不同产品特性对共线生产风险的影响机制,可通过收集大量的药品共线生产数据,包括产品特性、生产工艺参数、设备运行数据等,实现风险的准确预测和评估。
参考文献
[1] 田文淼,梁毅. 小容量注射剂共线生产的质量风险控制研究[J]. 中国医药工业杂志,2020,51(6):789-794.DOI:10.16522/j.cnki.cjph.2020.06.019.
[2] 国家药品监督管理局食品药品审核查验中心. 药品共线生产质量风险管理指南[EB/OL] (2023-03-06) [2025-5-12].https://www.cfdi.org.cn/cfdi/resource/news/15186.html.
[3] 浙江省药品监督管理与产业发展研究会. 药品每日允许暴露量评估方法:标准号T/ZJDAIR 011-2024[S/OL].(2025-04-28)[2025-05-12]. https://www.ttbz.org.cn/Home/Show/100143.
[4] 国家药典委员会. 中华人民共和国药典:2025年版·四部[M]. 北京:中国医药科技出版社,2025:3-4.
[5] 广东省药品监督管理局. 关于进一步加强广东省药品委托生产监督管理有关事项的通知[EB/OL]. (2024-07-12) [2025-5-12]. https://mpa.gd.gov.cn/zwgk/gzwj/content/post_4454682.html.
[6] 中华人民共和国卫生部. 药品生产质量管理规范(2010年修订):卫生部令第79号[EB/OL].(2011-01-17 )[2025-5-12]. https://www.samr.gov.cn/zw/zfxxgk/fdzdgknr/bgt/art/2023/art_d5e1dbaa8f284277a5f6c3e2fc840d00.html.
邵丽竹
何发
相关推荐
-
盘点 | 2024制药行业十大新闻评选开启(戳~投票留言互动有惊喜哦!)
时光的车轮滚滚向前,又一年制药征程落下帷幕。这一年,实验室里的瓶瓶罐罐见证着创新火花的迸发,生产线上的机器轰鸣奏响着品质提升的乐章。在这岁末之际,让我们共同开启制药行业的年度盘点,回味那些攻坚克难的日夜,梳理行业发展的脉络,一同探寻制药领域的过往、当下与未来,感受它为守护人类健康所付出的不懈努力与坚实力量。为此PharmaTEC制药业也为大家整理了这一年来的行业新闻和企业新闻,看看哪些令您印象深刻,一起评选出来吧!
2024-12-31 cici
-
固体制剂高活性车间设计策略
口服固体制剂作为临床应用非常广泛的剂型之一,其传统生产模式存在产尘量大、生产暴露环节众多以及工序复杂等特点。因此,在生产 OEB4-5 级标准的口服固体制剂时,面临的挑战是多方面的。本文从车间建设的角度出发,探讨了针对高毒性或高活性等固体制剂生产所需采取的技术手段与措施。
2024-12-18 卞强、陈宁
-
重磅!药物共线生产HBEL/PDE评估指南来了
2024年12月11日,浙江省药品监督管理与产业发展研究会发布了《药品每日允许暴露量评估方法》的征求意见稿,这是自2012年EMA发布HBEL指南以来,国内首个关于药物HBEL/PDE方面的指南,同时也弥补了国家药监局核查中心《药品共线生产质量风险管理指南》和《清洁验证技术指南(征求意见稿)》在这一方面的内容。算是大家翘首以盼的指南了。
2024-12-17
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略
















评论
加载更多