浅谈无菌制剂生产过程中无菌保障措施的优化
无菌制剂生产过程的潜在污染风险源涉及人员操作、无菌工艺等关键要素,需依据法规制定系统化的污染控制策略。本研究对各风险源的控制要点进行系统分析,并提出无菌保障体系的优化策略,为构建符合要求的无菌生产工艺控制体系提供科学参考及技术依据。
Part0 前言
无菌制剂指的是法定药品标准中列有无菌检查项目的制剂,包括注射剂、眼用制剂和无菌软膏剂等 [1]。其核心在于生产全程严格控菌,包括灭菌工艺、无菌操作及环境控制,以确保产品安全有效 [2]。
无菌制剂生产过程的污染来源具有多方面性,其中对人员及工艺的无菌控制尤为关键。欧盟GMP附录1《无菌药品生产》中明确提出,无菌药品的生产应符合其特殊要求,尽量降低微生物、微粒和内毒素 / 热原污染的风险 [3]。此外,欧盟 GMP 附录 1《无菌药品生产》对生产技术提出了新要求,对无菌保障能力设定了更高标准 [4]。在此背景下,为更好地保证药品质量,需将“质量源于设计”的理念引入无菌制剂生产管理。根据无菌制剂生产过程的主要污染来源,本文将重点阐述无菌生产中的污染控制策略,探讨无菌生产过程中无菌保障措施的优化方案,并制定系统化、可追溯的培训与资格确认体系,以促进行业有针对性地提高无菌制剂生产过程的无菌保障能力和水平,确保产品质量安全。
Part1 无菌制剂生产过程的污染来源及控制
1.1
人员
1.2
无菌工艺
Part2 无菌保障措施的优化
2.1
优化人员行为规范
因此,通过对动作进行分解以及对风险进行量化,建立了“三定原则”的分工体系。
定岗:固化角色,明确主 / 辅操作人员。主操作人员负责 A 级区关键操作,辅助人员负责物料表面消毒及脱包;
定位:明确每位操作人员的固定空间位置;
定姿:操作人员在 B 级区域时,肘部弯曲角度需保持在 90˚±10˚。
在相应的标准操作程序(standard operating procedure,SOP)中,对人员的主辅分工及站位进行规定,并在后续生产中严格按照规定执行。人员固定岗位及站位后,每位操作人员能明确自身的岗位职责及固定工位,可有效避免人员在洁净区内进行无意义的行为及走动,防止因无意义操作导致正常的气流形态发生变化,从而降低污染风险。
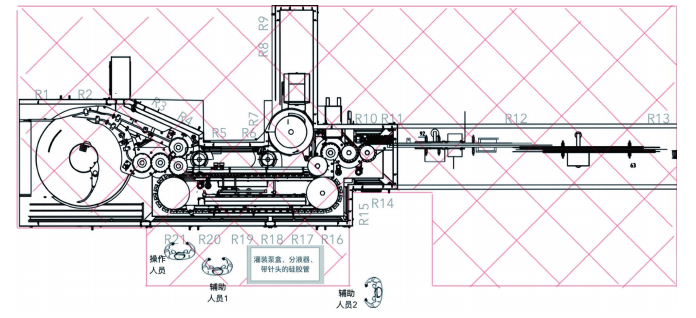
图 1 灌装系统安装过程人员分工及站位
2.2
优化无菌装配工艺
层流失稳风险:安全门开启时,延展层流保护存在局限性,打开安全门后,层流风速会急速衰减;
微生物污染风险:传统方法打开安全门进行安装操作,平均暴露时间达 12 ~ 15 min,增加了微生物侵入的风险;
扰动气流:气流可视化研究表明,开门操作会产生直径达 1.2 m 的湍流区,导致粒子扩散系数增大。
为降低打开安全门带来的污染风险,探索出“闭门式手套装配法”,即通过限制进入屏障系统(restrictive access barrier system,RABS)手套进行灌装泵装配。该装配方法仅需在装配前打开安全门,将已灭菌灌装泵盒放入灌装机 A 级层流内,然后关闭安全门。待悬浮粒子监测合格并自净至少 10 min 后,操作人员通过RABS 手套进行后续装配。
同时,为进一步提升无菌保障,在灌装组件预处理环节实施创新性防护措施:
硅胶管道出口端采用双层呼吸纸进行密封包裹,外层使用聚四氟乙烯鱼线捆扎;
灌装针头采用特制硅胶保护套与呼吸纸复合包装,外层使用聚四氟乙烯鱼线捆扎,确保在 121℃湿热灭菌过程中既能保持蒸汽穿透性,又可避免灭菌后运输阶段的二次污染。
采用“闭门式手套装配法”具有以下优势:
安全门开启时间缩短至< 5 min,且装配过程中无需开启安全门,可有效降低因长时间打开安全门导致污染的风险;
通过气流可视化验证发现,在安全门闭合状态下通过 RABS 手套进行灌装泵安装,气流流型符合规定,且使用 RABS 手套操作时对气流的扰动半径明显小于打开安全门进行操作,可有效降低传统灌装泵安装过程中微生物污染的风险。
Part3 培训与资格确认
3.1
优化培训机制
因此,基于风险控制理念构建的标准操作视频培训体系,通过拍摄关键操作的标准视频,实现了无菌操作的可视化质控:
采用摄影技术记录人员更衣程序,重点呈现无菌服穿戴顺序、手部消毒规范等关键控制点,确保受训人员精准掌握更衣过程的无菌操作规范;
基于物料传递流程规范,设置多机位拍摄物料转运流程,详细解析物料进入洁净区的脱包流程、物料表面消毒流程、无菌转运舱转运及双人复核机制等关键操作节点,便于操作人员掌握物料转运操作细节;
设置多机位拍摄分装器具组装流程,运用三维动画模拟灌装泵安装过程,确保受训人员掌握无菌装配技术规范;
设置多机位拍摄清洁消毒程序,重点解析无尘抹布折叠方式、消毒剂润湿程度控制及单向清洁路径规划等核心要素,建立可视化清洁验证标准;
通过慢动作回放解析灌装干预动作的风险点,建立干预操作的微观控制标准,使人员更清晰地了解干预动作注意事项;
建立标准化环境监测示范模板,重点解析采样高度、采样时间及环境监测设备操作流程,将模糊要求转化为精准指令,使取样方式规范化。
3.2
优化资质确认体系
Part4 讨论与总结
参考文献
[1]国家药品监督管理局食品药品审核查验中心. 药品GMP指南 无菌制剂[M]. 2版. 北京:中国医药科技出版社,2023:14-15.
[2] 黄玮. 无菌制剂生产中的无菌操作技术探讨[J]. 大医生,2018,3 (Z1):279+282.
[3] European Commission. EU GMP Annex 1: Manufacture of Sterile Medicinal Products[EB /OL]. (2022-08-22) [2023-01-10]. https://health.ec.europa.eu/system/files/2022-08/20220825_gmp-an1_en_0.pdf.
[4] 胡敬峰,明奕,王金子,等. 欧盟与我国GMP无菌药品附录差异分析与探讨[J]. 药学研究,2023,42 (8):636-640.
[5] 王似锦,王杠杠,余萌,等. 国内外无菌药品生产法规指南中人员的管理[J]. 中国医药工业杂志,2022,53(08):1222-1226.
[6] 陈西勇,于淑渤,梁宏. 无菌药品生产发生微生物污染的因素分析(上) [J]. 首都医药,2009,16 (6):23-25.
[7] 胡敬峰,刘荣,周勇,等. 生物制品无菌保证的特殊性分析与探讨[J]. 中国医药工业杂志,2024,55 (10):1426-1429+1441.
邵丽竹
何发
相关推荐
-
基于绿色低碳理念的制药厂循环水系统变频改造与能效优化实践
为响应绿色低碳发展要求,提升制药企业用能效率,对某典型制药厂循环水系统开展了变频节能改造与运行优化研究。
2026-02-24 熊伟,程鑫,周伟豪
-
节能理念在某生物疫苗生产厂房设计中的运用
在生物疫苗生产企业中,生产厂房是生产活动的主要集中地,并且生产厂房的设施设备能耗较高,其中以空调能耗最为明显。
2026-02-13 杨红斌 朱毅 杜有径 吴志超 李杨 杨磊
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略
















评论
加载更多