【药厂】如何做好培养基?
不同培养基可根据实际需要,添加一些自身无法合成的化合物,即生长因子。
例如:高氏一号培养基(淀粉琼脂培养基)制作:在烧杯中加水95毫升,加热至沸腾,取可溶性溶粉2克,用5毫升水调成糊状,倒入沸水中和匀。再称取其它药品,陆续加入烧杯内(待一种药品溶解后,再加入第二种药品)。待全部药品溶解后,停止加热,补足失水,调pH值至7.2~7.4。分装后,高压蒸汽灭菌。本培养基常用于培养放线菌。
例如:肉汁蛋白胨液体培养基的制作:取新鲜牛肉500克,去净脂肪、筋腱后,绞碎或剁碎,加水1000毫升浸泡,15℃下放置12小时或50℃下放置半小时。用纱布将肉汁过滤,补足失水。向肉汁中加入蛋白胨和食盐。将肉汁加热,放入苏打(碳酸钠)至红色,调整pH值。分装,高压蒸汽灭菌。将上述已灭菌的培养基用棉花滤去凝集的蛋白质,制成液体培养基,如需制成固体培养基,可在每100毫升液体中加入2克琼脂,加热溶化后,分装,再次进行高压蒸汽灭菌。常用于培养细菌。
例如:豆芽汁葡萄糖(或蔗糖)培养基的制作:称取新鲜黄豆芽100克,放入烧杯中,加1000毫升水,煮沸30分钟,用纱布过滤,补足失水。再加葡萄糖(或蔗糖)50克,琼脂15克,加热至融化,补足失水。分装,加棉塞,高压蒸汽灭菌。常用于培养霉菌。
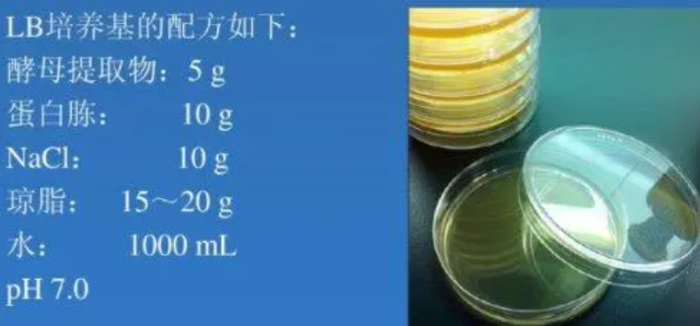
为满足生物产品的生产需求,必须支持高密度细胞的生存,促进生物产品的合成和细胞外运输。培养基的制备程序不同类型培养基制备的程序也不尽相同。培养基按状态分有固体培养基和液体培养基,一般培养基需要完成以下十个主要步骤:选择配方、记录制备、称重成分配料、配制溶液、调整成分,矫正pH、澄清过滤、分装、灭菌及检定等,过程中要要注意培养基的温度,各类营养物质的浓度的比例, PH值,用水和营养液配置,要注意碳源和氮源的浓度的比例。

为了使菌能正常生长发育,培养基除了必须有足够的碳、氮营养外,还应注意碳与氮的比例(碳氮比,C/N)。这样既能保证营养生长阶段对营养的需要,也能保证生殖生长的顺利进行。例如,巴西蘑菇培养料适宜的碳氮比(C/N)为28~30∶1,含氮量1.4%~1.6%,投料量30~35千克/米²。
1.选择培养基配方:同一种培养基,其表达方式往往存在着差异。所以,除了应当严格按照标准方法的规定编制之外,我们一般应尽可能收集有关数据,加以比较和核对,然后根据自己的目的选择和记录数据来源
2.记录培养基的制备:培养基的制备记录包括培养基的名称、配方及其来源、pH值、灭菌温度、时间、配制日期、制备人等,并且要复印记录和保存原始记录备查。对副本的记录应该和培养基一起保存,以防出现混乱。
3.称重培养基的成分配料:培养基成分要准确称量,并注意防止混淆。每一种成分称量完毕后,都要在分装的一面打上记号,然后将分装的药物一起放在左边。每一个成分称量完之后,都会向右移动。全部称量完毕,应再次检查。按培养基处方准确称取各种成分,先在三角烧瓶中加入少量蒸馏水,再加入各种成分,以防蛋白胨等粘附于瓶底,然后再以剩余的水冲洗瓶壁。
4.配制溶液:向容器内加入所需水量的一部分,按照培养基的配方,称取各种原料,依次加入使其溶解,最后补足所需水分。对蛋白胨、肉膏等物质,需加热溶解,加热过程所蒸发的水分,应在全部原料溶解后加水补足。配制固体培养基时,先将上述已配好的液体培养基煮沸,再将称好的琼脂加入,继续加热至完全融化。并不断搅拌,以免琼脂糊底烧焦。
5.调整培养基成分:介质中使用的化学物质应该是化学纯品,铜锅或铁锅易导致铜、铁混入培养基,使细菌难以繁殖。用不锈钢锅加热溶解较为适宜。将各种成分混匀于水中,*以流通蒸汽溶化半小时,如在电炉上溶化应随时搅拌,如有琼脂成分时geng应注意防止外溢。溶化完毕,补足失去的水分。溶解于水的锅子,可用温水加热,随时搅拌,防止结焦。若发现结焦,则不能使用介质,需重新调配。在溶解大多数固体成分之后,用少量热将其全部溶解,直到沸腾。
6.调整培养基的pH值:由于加热消毒过程中培养基的 pH值会发生变化,因此应在培养基组分完全溶解后,调整 pH值。用pH试纸(或pH电位计、氢离子浓度比色计)测试培养基的pH值,如不符合需要,可用10%HCl或10%NaOH进行调节,直到调节到配方要求的pH值为止。举例来说,牛肉汁的 pH值下降了0.2左右,而肠浸出物的 pH值则明显上升。所以,在这一步中,操作者要注重不断探索经验,掌握培养基的最终 pH值,保证培养基的质量。pH测定,取与标准管同口径的试管(通常用华氏试管)3支,于第1、3管各加入欲测定pH的的培养基5ml,并于第1管中加入0.2g/L的酚红0.25ml作为测定管,混匀于第2管加入蒸馏水5ml,第4管为pH标准比色管。pH的校正,若测定管过酸或过碱可用0.1mol/L氢氧-化钠或0.1mol/L盐酸溶液矫正,直至颜色与标准管相同为止,加碱或加酸时要精-确缓慢,每加1滴后要充分混匀,比色后再加第2滴(有时仅加半滴)准确记录加入的量。计算,设5ml培养基矫正pH至7.4时需0.1mol/L氢氧-化钠0.15ml,现有培养基4990ml,需加氢氧-化钠的量可按下列方法计算:5∶4990=0.15∶X X=0.15×4990/5=149.7(ml),如将此0.1mol/L的氢氧-化钠改用1mol/L的氢氧-化钠时,则需14.9ml即可。在调整 pH值后,要将其煮沸几分钟,以利于培养基沉淀。
7. 过滤澄清:用滤纸、纱布或棉花趁热将已配好的培养基过滤。用纱布过滤时,最好折叠成六层,用滤纸过滤时,可将滤纸折叠成瓦棱形,铺在漏斗上过滤。培养基配制后一般都有沉渣或混浊出现,需过滤成清晰透明后方可使用,常用的过滤方法如下:液体培养基必须清晰,以便观察细菌的生长情况,常用滤纸过滤,亦可在加热前加入用水稀释的鸡蛋白(1000ml培养基用1个鸡蛋白)在100℃加热后保持60~70℃40~60分钟,使其不溶性物质附于凝固的蛋白上而沉淀,然后再用虹吸法吸出上清液或以滤纸过滤。固体培养基如系琼脂培养基,于加热融化后需趁热以绒布或两层纱布中夹脱脂棉过滤;亦可用自然沉淀法,即将琼脂培养基盛人铝锅或广口搪瓷容器内,以高压(103.43kPa)蒸汽融化15分钟后,静置高压锅内过夜,次日将琼脂倾出,用刀将底部沉渣切去,再融化即可收清晰的琼脂培养基。
8. 分装与加塞/包扎:已过滤的培养基应进行分装。如果要制作斜面培养基,须将培养基分装于试管中。如果要制作平板培养基或液体、半固体培养基,则须将培养基分装于锥形瓶内。分装时,一手捏松弹簧夹,使培养基流出,另一只手握住几支试管或锥形瓶,依次接取培养基。分装时,注意不要使培养基粘附管口或瓶口,以免浸湿棉塞引起杂菌污染。装入试管的培养基量,视试管和锥形瓶的大小及需要而定。一般制作斜面培养基时,每只15×150毫米的试管,约装3~4毫升(1/4~1/3试管高度),如制作深层培养基,每只20×220毫米的试管约装12~15毫升。每只锥形瓶装入的培养基,一般以其容积的一半为宜。分装完毕后,需要用塞堵住管口或瓶口。堵塞的主要目的是过滤空气,避免污染。塞应采用普通新鲜、干燥的棉花制作,不要用脱脂棉,以免因脱脂棉吸水使塞无法使用。制作棉塞时,要根据棉塞大小将棉花铺展成适当厚度,揪取手掌心大小一块,铺在左手拇指与食指圈成的圆孔中,用右手食指插入棉花中部,同时左手食指与姆指稍稍紧握,就会形成1个长棒形的棉塞。棉塞作成后,应迅速塞入管口或瓶口中,棉塞应紧贴内壁不留缝隙,以防空气中微生物沿皱折侵入。棉塞不要过紧过松,塞好后,以手提棉塞、管、瓶不下落为合适。棉塞的2/3应在管内或瓶内,上端露出少许棉花便于拔取。塞好棉塞的试管和锥形瓶应盖上厚纸用绳捆札,准备灭菌。
9. 灭菌:不同成分、性质的培养基,可采用不同的灭菌方法。高压蒸汽灭菌法:高压灭菌的温度与时间随种类及数量的不同有所差别,一般少量分装时高压(103.43kPa)灭菌15分钟即可,分装量较大时,可高压(103.43kPa)灭菌30分钟,含糖的培养基高压(55.16kPa)灭菌15分钟。以免糖类被破坏。某些畏热成分,如糖类,应另行配成20%或更高的浓液,以过滤或间歇灭菌法消毒,以后再用无菌操作技术、定量加于培养基。明胶培养基亦应用较低温度灭菌。血液、体液和抗生素等则应以无菌操作技术抽取和加入于经冷却约50°C左右的培养基中。琼脂斜面培养基应在灭菌后立即取出,冷至55℃-60℃时,摆置成适当斜面,待其自然凝固。
10.检定保存:培养基应存放于冷暗处,最好能放于普通冰箱内。每批制成后须经检定方可使用,检定时将培养基放37℃温箱内培养24小时后,证明无菌,同时用已知菌种检查在此培养基上生长繁殖及生化反应情况,符合要求者方可使用。制好的培养基,不宜保存过久,以少量勤做为宜。每批应注明名称,分装量,制作日期等,放在4℃冰箱内备用。放置时间不宜超过一周,倾注的平板培养基不宜超过3天。每批培养基均必须附有该批培养基制备记录副页或明显标签。

制作培养基是生物制药的基础步骤,以上十步是制作培养基的主要步骤。制作培养基容易,但制作契合的培养基则并不容易。配置培养基需要注意诸多问题,例如:
1、 根据不同微生物的营养需要配制不同的培养基。
2、 注意各种营养物质的浓度及合适配比,保持合适渗透压。
3、 将培养基的 pH 控制在适宜的范围之内,以利于不同类型微生物的生长繁殖或代谢产物的积累。
4、要注意各种原料的配比,每种培养基的配比合适的配比,可以按照老师的要求去做。
5、如需要加热的时候注意时间的把握。
随着AI应用技术的不断发展,制作培养基得到了质的飞跃,快速开发定制化培养基的设想逐步成为现实。
本文来源于制药人职场加油站
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多