浅谈干粉吸入制剂固相表征的研究进展
对于治疗呼吸道疾病如慢性阻塞性肺病等,吸入给药已经成为常用的给药方式。吸入给药是通过特殊的给药装置将药物颗粒递送到肺部,可以实现靶向肺部给药。吸入肺部给药的优点如下:①可以对疾病和感染进行局部治疗;②起效快;③减少药物剂量和副作用。干粉吸入剂是指微粉化药物或与载体以胶囊、泡囊或多剂量贮存形式,采用特制的干粉吸入装置,由患者主动吸入雾化药物至肺部的制剂,在肺部沉积,发挥全身或局部作用的给药系统。由于使用简单,易于携带,患者的顺应性好,所以干粉吸入剂应用较为广泛,是最具有开发潜力的肺部给药制剂,也为某些作用于全身的药物提供了新的开发思路。
吸入粉雾剂的处方组成较为简单,但是,产品开发的难度却相当大。大多数 DPI 产品的处方仅由原料药物微粒组成或者由药物与载体混合而成,一般认为,只有空气动力学粒径在 1μm~5μm 的颗粒才能进入肺部发挥药效。粒度小的药物颗粒的内聚力和黏附力对DPI产品的微细粒子剂量起到重要作用,其物理性质如粒度分布、形态、流动性等直接影响药物颗粒之间的作用力。所以,在开发 DPI 产品之前,充分了解药物和辅料颗粒的物化性质是非常重要的。本文将从干粉吸入制剂的粒径、粒子形态、粉末流动性及晶型等方面进行固相表征技术及其进展的介绍,并讨论不同方法的适用条件与优缺点,以期促进干粉吸入剂的新药研制。
一、粒径测定
一些研究证明,由于肺的解剖结构,粒径和粒度分布直接影响药物在呼吸道和肺部的沉积,在处方筛选和工艺优化中,吸入剂药物的颗粒大小是 DPI 配方设计中最重要的因素之一。粒子的粒径大于 5μm,通常沉积在口腔或咽喉部位,容易被清除;若粒子的粒径小于 1μm,则不会在肺部沉积,很容易随着气流流动,由于布朗运动悬浮,沉降得非常缓慢。一系列研究表明,制剂的最佳粒径通常是1μm~55μm。评价粒径和粒度分布的方法有显微镜测定法、撞击器法、现代光学仪器测定法等。
(一) 激光衍射法
激光衍射法是一种快速的粒度分析技术,主要是基于衍射光传播角度和光能强弱,与被测颗粒的粒径和数目有一一对应关系,粒径小的粒子衍射角偏大,粒径大的粒子衍射角偏小。利用光散射的数学模型将光散射图案转换为体积加权的粒度分布。
对于激光衍射粒度分析,粉末样品可以分散在液体(湿分散)或气体(干分散)中。当样品分散在液体中,液体分散介质应使用透光的,其折射率与样品粒子的折射率应相差很大,且不影响样品粒子的大小,样品在此液体内的溶解度不超过5g/kg。异丙醇和丙酮满足 α- 乳糖的一水合物和甘露醇的标准,这种辅料广泛用于基于载体的 DPI 制剂配方,通常需要将分散介质与样品进行预饱和,搅拌和超声波有利于样品的分散。
当样品分散在气体中,例如空气,气体压力提供了粒子解聚所需的能量,气体压力应优化至使粒子充分分散且不会使粒子粉碎。通常将湿分散作为参考,与湿分散具有相同粒度分布的压力为最佳压力。激光衍射图样的分析,即将衍射图样转换为粒度分布,通常使用 Mie 光散射理论或 Fraunhofer 衍射理论。Mie光散射理论适用于任何大小的均匀、各向同性粒子。对于具有未知光学特性的直径大于 50μm 的微粒和具有不同折射率的大颗粒(直径大于50μm)的混合物,通常使用 Fraunhofer 理论[1]。
(二) 图像分析法
粉末颗粒的大小分布也可以通过分析光学或电子显微镜获得的图像来确定,但是,为了获得有代表性的测量结果,需要分析大量的粒子图像。虽然可以实现自动化,但与激光衍射测量的方法相比,需要消耗大量的劳动力和时间。对于 DPI 载体,应保留对显微镜图像的分析以及在产品开发中需要对颗粒进行改性的情况[1]。
(三) 撞击法
虽然利用不同的几何特征或理化性质来确定颗粒大小及其分布的方法有很多,但空气动力学直径是与肺输送和最终的治疗效果最相关的,重力沉降和惯性冲击都取决于颗粒的气动直径,其粒径分布大小能直接影响药物在肺部和呼吸道的沉积及分布。因此,递送API的空气动力学粒径分布(APSD)是口服吸入产品一个关键的质量属性。
撞击法主要是利用惯性撞击的原理,按粒径大小分离药物颗粒,可对吸入制剂的体外沉积进行测定。此类装置主要有两级玻璃 撞 击 器(twin stage impactor,TSI)、Marple Miller 多级撞击器、Anderson 多级撞击器、多级液体采样器、新一代药用撞击器(next generation impactor,NGI) 以及电子新一代药用撞击器(the electrical next generation impactor,eNGI),目前除 eNGI 外,其他几种均已载入欧洲药典。
1. 新一代药用撞击器测定
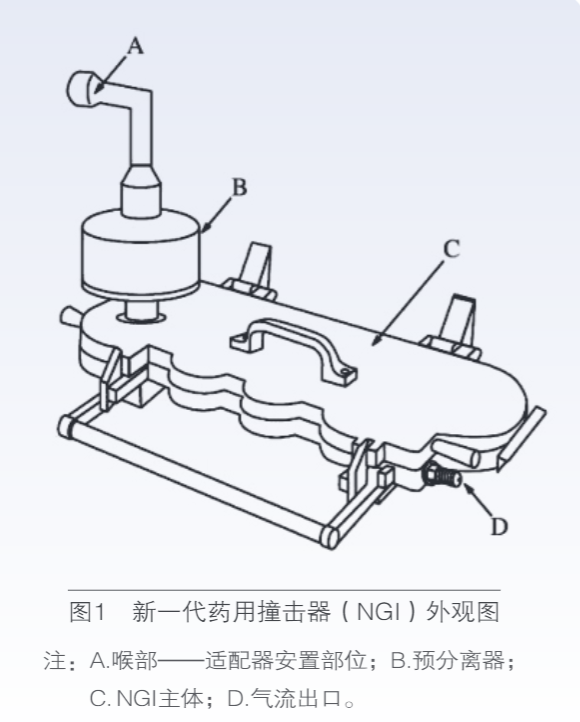
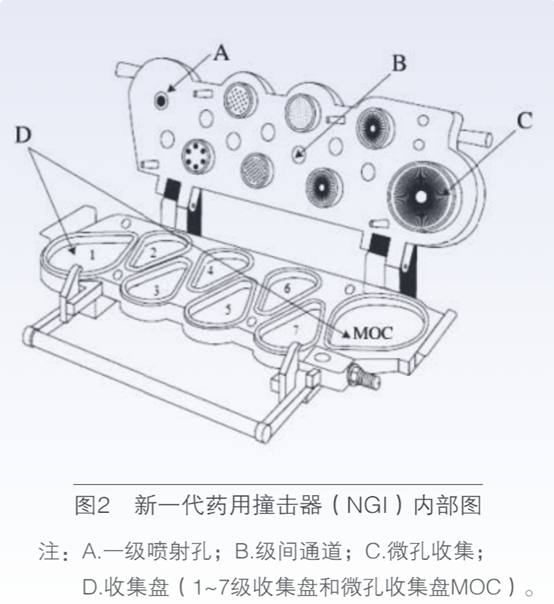
按照欧洲药典的方法进行测定,新一代药用撞击器(NGI)外观如图1所示,其内部结构如图2所示。先将收集盘用配好的涂层液进行涂层处理。
安装托盘,锁住杯体,进行气密性检查,气密性良好则进行仪器的安装,并在预分离器中加入约15mL蒸馏水。开启真空泵,将流量计连接于喉部,调节流速,固定流量,设置吸入时间和吸入次数。在吸入装置中置入一粒待测胶囊,按压吸入装置刺破胶囊,将吸入装置插入仪器喉部A处的橡胶适配器,按压吸入按钮进行测定,测试完成后取下吸入装置,置入另一胶囊进行吸入测定。用双蒸水分别清洗吸入装置、喉部(包含适配器)、预分离器及 8 个收集盘,将洗液分别收集定容,采用 HPLC 法测定。
2. 数据处理
收集各部位沉积的药物,定容后HPLC分 析 得 出 回 收 剂 量(recovered dose,RD),即装置、胶囊、适配器、模拟喉部、模拟颈部、收集盘的药物总量;传递剂量(delivered dose,DD),即适配器、模拟喉部、模拟颈部、收集盘收集的药物总量;累积药物总量定义空气动力学粒径小于一定值的累积药物量为FPD,以及体外沉积率(fine particle fraction,FPF),即 FPD 占DD 的百分率。药物损失量(total loss drug mass)为给药总量与回收剂量的差值,以累积分布百分率的对数对截断直径的对数作图,累积分布百分率达到50%时的粒径为质量中间空气动力学粒径(mass median aerodynamic diameter,MMAD);累积分布率分别为 84.13%、15.87% 时,对应的空气动力学直径之比的平方根为几何标准差(geometric standard deviation,GSD)。一般认为,GSD 越接近 1,吸入粉雾剂的粒度分布越窄。
NGI不仅能表征药物颗粒的粒度分布,亦能表征粒径小于 0.5μm 的小颗粒量,而且可以方便得到 MMAD 和 GSD 以及 FPF 的数值,可对吸入粉雾剂进行更全面的评价。但是,NGI也有自身的缺点:仪器精密,易造成MOC级喷射孔损坏,并需定期对喷射孔直径进行测定,以确定其截断粒径的准确性;需定期对上部垫圈进行更换,以保证其密封性等 ;高喷射速度,易造成粒子的回弹。不同的流速和涂层均会对沉积率的测定造成影响,因此,在用 NGI 测定粒径和沉积率时,应对其进行流速、涂层等方面的考察,建立良好的方法,使测定结果精确、可靠[2]。
二、粒子形态观察
除了粒度分布大小,粒子的表面形态也会影响制剂的稳定性和雾化性能。在呼吸给药系统中,药物粒子与载体的分布或黏附受到载体表面性质和粒子表面粗糙度的影响。对于可吸入药物粒子与载体的混合物,在混合或雾化时,药物与载体之间的黏附力影响两者的混合和分离,粒子表面粗糙度是影响黏附力的主要因素。Staniforth 等人认为,大多数情况下,更多的药物倾向于附着在粗糙的载体上。颗粒的表面粗糙度可以通过扫描电子显微镜(SEM)、光学显微镜、气体吸附法(BET)、激光轮廓技术、扫描探针显微镜(SPM)等技术来评价。
(一) 扫描电子显微镜和光学显微镜
扫描电子显微镜(Scanning Electron Microscope,SEM)和光学显微镜大多用来评价药物颗粒的表面形态和粗糙度,获得的信息是具有可视性和可描述的,但提供的信息有限,只能得到表面的定性信息。扫描电子显微镜是用细聚焦的电子轰击样品表面,通过电子与样品相互作用产生的二次电子、背散射电子或吸收电子等信号对样品或断口形貌进行观察和分析。
扫描电子显微镜具有制样简单、分辨率高、景深大等特点,能提供样品的形态和样品的几何尺寸等信息。采用扫描电子显微镜观察混合粉末表面的颗粒形状时,制备的样品需导电。对于非导电的样品,在电子束作用下会产生电荷堆积,影响入射电子束斑和样品发射的二次电子运动轨迹,使图像质量下降。因此,为了使测量样品具有导电性,在观察前要给样品喷上导电层。
扫描电子显微镜和光学显微镜的图像可以获得颗粒的形态参数,如宽度、长度、长宽比和圆度等,不能直观地提供粒子粗糙度的定量信息,是通过图像中表面阴影的色度和锐度间接地判断粗糙度,如图 3 可以比较两种乳糖载体的粗糙度[(a)较平滑;(b)较粗糙],但是,这种比较具有主观性,不能准确地计算量化。
(二) 比表面积测定
一些研究通过测量乳糖的比表面积将其和表面粗糙度联系起来。比表面积可以采用空气渗透法和气体吸附法两种方法测定,但只能通过计算比表面积间接地推测表面粗糙度,不能真正准确地获得表面性质。
空气渗透法是在规定的压力和体积下将粉末样品压实,空气强制通过填充的粉体层,得到的压差就是样品的比表面积,这种方法适用于无孔的粒子。在气体吸附法中,低温物理吸附氮气应用最为广泛,吸收的等温线是通过增加分压测量吸收的气体得到的,根据 BET 方程计算样品的比表面积。比表面积的计算与粒子的粒径有关,只有粒径分布相同或近似的样品基于比表面积评价表面粗糙度才有效。因此,此方法只是通过测比表面积间接地评价粗糙度,对于比表面积很小的粒子,准确性低,需要大量的样品进行测量[3]。
(三) 轮廓测定法
粒子的表面粗糙度也可以用轮廓仪来测量。传统轮廓仪的触针和传感器安装在拾取臂上,拾取臂以一定的速度使触针在表面上滑过。触针随着不规则表面垂直运动产生与表面局部高度呈比例的电信号,将这种电信号进行处理,转换成表面的轮廓。然而,轮廓仪使用触针会损坏样品表面,有较大凹凸的表面会被触针击碎,粗糙度的轮廓也会改变。非接触式激光轮廓仪使用低能量的激光束,光斑的大小通常为0.6μm~1μm,用双光束干涉法计算光斑到表面之间的相对距离。透明的粒子表面不能被准确地测量,因为激光无法反射。
(四)扫描探针显微镜
最 近, 扫 描 探 针 显 微 镜(Scanning Probe Microscope,SPM)越来越多地被用于粗糙度的评价,它可以获取粒子表面的三维图像,通过不同的参数来计算粗糙度。扫描探针显微镜测量金属尖端和导电表面之间的电流,用于探测粒子表面电子的密度,但只能用于导电的表面。
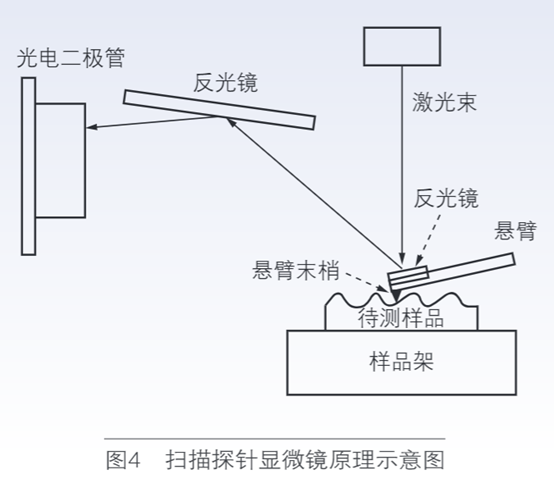
原子力显微技术绘制了离子表面和连接到悬臂尖端之间的表面力,用于非导电材料。然而,SPM 可以用于导电和非导电材料,并且能够测量从微观到纳米尺度粒子表面粗糙度,比其他方法有更好的分辨率[4]。样品表面的3D轮廓可以由SPM的接触和非接触两种模式直观地获得。SPM的原理基于一非常小的悬臂置于靠近样品表面的位置,测量悬臂和样品表面之间的原子力(见图 4)。
当悬臂扫描到样品表面时,若样品表面特性改变,由于悬臂梁和表面之间的作用力,悬臂梁会改变高度以保持两者之间的距离。用这种方式,悬臂梁的移动也直接反映了样品表面的特性。悬臂梁的改变由反射的激光束检测,通过电脑来记录。接触模式是利用上述办法检测悬臂梁和样品之间的斥力,但是,悬臂梁和样品之间的接触会导致悬臂梁和样品受到损坏。然而,动态模式不会使样品表面和悬臂接触,避免了接触的损坏。在动态模式中,利用悬臂梁尖端在悬臂的共振频率附近振动,当振动的悬臂接近样品表面时,由于悬臂和样品之间的原子力,悬臂的振动频率也会改变。共振频率的变化可以通过悬臂梁尖端的振幅变化来检测,光电二极管通过反射的激光来检测到这种振幅变化[5]。
在三维图像(见图5)上,利用各种参数和计算得到表面粗糙度的定量和定性的信息。
Seitavupio 等人通过平均粗糙度(Ra)、均方根粗糙度(Rrms)、峰谷比(Rp-v)等一系列高度参数,用SPM对片剂的表面粗糙度进行了定量化,与轮廓仪相比,SPM 有更小的悬臂梁尖端,可以更加准确地测量,有更高的分辨率,甚至可以达到纳米级。
三、粉体流动性
DPI原料药和辅料的流动特性不仅是DPI处方性能的关键,也是药物辅料混合、胶囊、设备填充等人工制造过程的关键。在DPI产品中,粉末的分散与两个过程有关:
粉末的流化与解聚,流动性差、内聚力大的粉末在吸入时会导致雾化性能较差。目前,有几种方法用于粉末流动性不同方面的测定,测量方法的选择应以所要测量的流变特性与粉末的制造工艺及应用的相关性为基础。
(一) 卡尔指数
与Hausner 比卡尔指数和 Hausner 比是描述粉末可压缩性和流动特性的两个指标。这两种指标都很好地说明了粉末的形状对粉体流动性的影响,并且对DPI辅料流动性的变化很敏感,例如向载体中加入细粉,即由于粒度分布而使流动性发生变化。这种方法的优点是成本较低,易于应用,但只是一种经验技术,测量结果可能会因为测量的精确度而有所差异。
其中,ρB、ρT分别是粉体的松密度和堆密度
(二) 粉末流变仪
粉末流变仪,Freeman FT4 提供了一系列粉体流变学测试,具有动态表征技术,可实现动态测试,其装置如图 6 所示,当粉末材料在运动状态时,对粉末材料的流动特性进行评估。
能够模拟不同的工艺环境,测量粉体在不同环境下的流动行为。可以直接测量粉体对于充气、固结、湿度和流动速率的反应,测量粉体密度、压缩性、渗透性等完整的松装性质。
动力学测量“桨叶”或“叶轮”螺旋旋转一定距离穿透粉层使粉末颗粒发生混合或分离。“桨叶”所需的扭矩反映了粉末的旋转阻力和垂直阻力,阻力越大粉末流动越不顺畅,则桨叶移动也越困难。桨叶移动时,FT4 粉末流变仪通过计算扭矩和阻力,对旋转阻力和纵向阻力进行测量,通常以流动能量表示。两种数值结合在一起,才能对粉体的整体流动阻力进行量化,从而反映粉末的流动性。旋转的角度、速度和方向,气流(通风)和施加的应力对粉末流动行为提供了详尽的描述。通过桨叶的旋转方向对粉体分为两种流动方式,约束流动和无约束流动决定了对粉体所施加压力的方向。
约束流动又被称为“强制流动”,指桨叶向下运动,粉体在螺旋饲料器上处于强制流动状态时,叶轮旋转下降粉末层1mm时,所测得的流动阻力,对得到的流动阻力值进行积分,计算出所做的功,即基本流动能量(Basic Flow Energy,BFE),是粉末被迫移动时的流动性指标。桨叶向上运动时,粉末的移动不受限制,也没有任何东西阻碍粉末的向上移动,粉体处于低压填充,低剪切力混合的无约束流动状态下,所测得的流动能量是比能量(Specific Energy,SE),该参数粉末无约束流动时的流动性指标[3]。
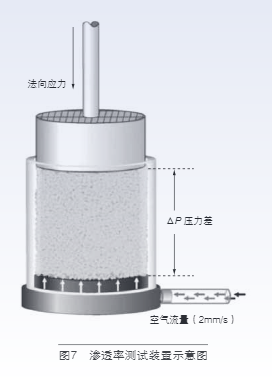
渗透性测试渗透性测试是观察粉末在空气中的行为,以及随着混合物中细小颗粒数量的增加而发生的渗透性变化。渗透率测试装置如图 7 所示,由一个 25mm×10mL 规格的硼硅酸盐容器,连接到曝气控制单元(ACU)的多孔曝气底座,24mm 排气活塞和 23.5mm 用于调节的桨叶组成。
ACU 使通过多孔底座的空气流量保持恒定在 2mm/s,同时排气活塞施加的正向应力以8mm/s增加,直至正向应力达到 15kPa。这样,可以获得每个施加的法向应力的渗透率值,用粉末床下降的压力作为一个比较不同粉末混合物的参数,相应的渗透率值可以用达西定律 :
3. 充气测试
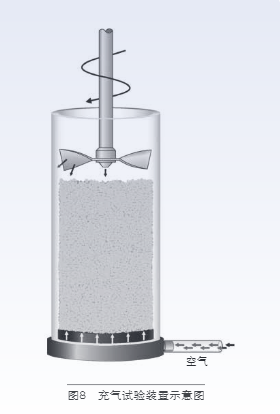
充气性质测试是用来考察粉体的内聚力强度、雾化或干粉吸入、流化态等行为。在粉体流变学测量过程中,DPI配方的雾化或吸入可以通过充气来模拟,引入空气是为了分散粉末粒子。Freeman FT4 粉末流变仪使用三个术语来描述气流对粉末流动性的影响:“充气能量”、“流化能量”和“动态流动指数”。充气能量是引入的空气流量的函数,是粉末充气后所需的流动能量,充气能量随着空气流量的增加而减少;当气流足以使粉末流化时,充气能量最小,被称为“流化能量”;动态流动指数 = 基本流动能 / 流化能量。流化能量可以作为预测粉末在吸入过程中分散性的指标[3,6]。充气测试装置由一个与 ACU 连接的多孔充气底座,孔直径为 25mm×35mL 硼硅酸盐的容器以及 23.5mm 桨叶组成,如图 8 所示。
将样品粉末装填在容器中,先对样品粉末进行预处理,叶轮再逆时针旋转向下压入粉末,记录下所需的流动能量,在 ACU 的调节下不断充气,随着充气量的增加,流动能量越来越小,当样品充分流化,此时所测量的能量为最小流化能量。在进行充气测试之前,已经进行了多次无空气通过的基本流动性能量(BFE)的测量,以确保粉末样品在充气测试过程中保持稳定,并且所测得的流动能不受其他因素的影响,如离析、固结等。
四、晶型测定药物
常见的固体形式有溶剂化物,亚稳定型、共晶型和无定型这些不同的存在形式影响着药物的稳定性、溶解度和生物利用度等,是重要的理化性质。据报道,近1/3的药物具有多态性,即以一种晶型以上的方式存在。在药物研发的最初阶段,确定药物的多晶型极为重要,不同的晶型存在不同的能量状态,也具有不同的稳定性、溶解度、生物利用度等物理、化学性质。
也有一部分药物是非晶型或无定型的,在大多数情况下,此类药物通过迅速干燥或冷却液体,例如喷雾干燥技术,使其分子在占据晶格位置之前失去流动性。结晶态的药物经过高能粉碎的技术,结晶度降低,产生无定型药物比结晶态药物的吉布斯自由能高,根据热力学定律,药物会从高能量状态过渡到低能量状态。所以,无定型药物热力学不稳定,重结晶后的颗粒表面性质也会发生变化,导致粉雾剂性质发生变化[3,7]。
在制剂和存放的过程中,可能会发生晶型转变,影响制剂的质量,而且不是所有的晶型都具有生物等效,因此,对于药物晶型的研究已经成为新药开发质量检测的重要部分。目前,对于药物的晶型检测技术有很多种,如 X 射线衍射(XRD)、差示扫描量热法(DSC)、热重分析(TGA)、红外光谱(IR)等。
(一)热分析技术热
分析技术是在程序控制温度下,测量温度变化时物质物理变化的一种分析技术,其广泛应用于物质的多晶型、物相转换、热分解、稳定性等方面的研究。热分析技术图8 充气试验装置示意图空气272021.04Research & Discussion
主 要 包 括 热 重 分 析(thermo gravimetric analyzer,TGA)、 差 示 扫 描 量 热 法(differential scanning calorimetry,DSC)、差热分析法(differential thermal analysis,DTA)、动态蒸汽吸附法(dynamic vapor sorption,DVS)。
1. 热重分析法
热重分析法(TGA)是在程序控制温度下,测量物质的质量随温度变化关系的一种技术,可以测量物质质量的变化及变化速率,主要用于测定晶体表面吸附的水含量[8]。
2. 差示扫描量热法
近年来,差示扫描量热法(DSC)是制药领域最广泛的热分析法,已经成为多晶型定量定性分析的常用方法。DSC 是对样品进行线性的加热或冷却,随后测量样品的一系列与热效应有关的温度和热量,如熔化、结晶、玻璃化转变或分解反应,在DSC图中可以获得转变温度,从而确定多态形式之间的对应关系。不同晶型在升温或冷却中的吸热、放热峰都有差异,峰的位置、数目、形状都与物质的性质有关,根据不同的曲线可以定性地表征和鉴定物质,而峰的面积与反应焓有关,可以用来定量计算参与反应的物质的量及测定热化学参数。与差热分析法(DTA)不同,DTA 是在程序控制温度下,测量供试品与参比物的温度差变化的一种技术,DSC 技术是对早期DTA 方法的发展。DSC 的优点是样品量小,约3mg~10mg,测量范围广,测量简单迅速,但DSC的图谱特征性不强,还需要辅助其他方法确定晶型。DSC 在使用时要注意升温速率、试样用量和装填情况等,在进行测量之前要掌握样品合适的测量参数[9]。
3. 动态蒸汽吸附法
动态蒸汽吸附法(DVS)采用高度灵敏的数字微天平,实时监测药物吸附水蒸汽前后的动态蒸汽重量变化,获得吸附/脱附曲线,是快速测量样品中水分增减的办法,可实现对多晶型体系中各种水合物形态的鉴定,其优点是实验设置简单[10]。
(二)粉末 X 射线衍射技术
粉末X射线衍射技术(PXRD)是药物多晶型鉴定的主要手段,主要用于表征多晶或粉状固体样品的晶体结构。不同固体具有不同的粉末衍射图谱,相同固体不同的晶型由于空间的对称排列规律不同,衍射图谱也会存在差异。粉末衍射的图谱所具有的指纹性与特征性表现在衍射峰位置与强度上,因此可以鉴别样品的存在状态。粉末 X 射线衍射技术的优点是样品量大于50mg,测试方法是非破坏性的,可以定性定量[11]。
五、发展与展望
吸入粉雾制剂在我国的起步较晚,技术力量薄弱,发展缓慢,仍处于起步阶段,随着国内医疗水平的发展和患者用药观念的变化,吸入制剂的市场正在扩大,也是国内外制药行业关注的焦点。各大制药公司开始投入力量进行粉雾剂的研发,同时各国药监部门对吸入剂的质量要求也变得越来越严格。
除了对干粉制剂的粉末进行上述物理、化学性质的研究,还要对 DPI 的处方以及装置和患者临床用药进行指导,这也是影响药物肺部递送的关键因素。患者依从性高、效果均一稳定、个性化、智能化的吸入装置将成为未来肺部药物递送系统发展的方向。
参考文献
[1] Elsayed Mustafa M. A. Microstructural characterization of carrier-based dry powder inhalation excipients:Insights and guidance[J].International journal of pharmaceutics,2019,568.
[2]杨资伟,杨阳,李晗,陈启明,梅兴国.两种撞击器测定自制吸入粉雾剂体外沉积性质的对比研究[J].国际药学研究杂志,2013,40(4):475-480.
[3] Tan Bernice Mei Jin,Chan Lai Wah,Heng Paul Wan Sia.Characterizing the Surface Roughness Length Scales of Lactose Carrier Particles in Dry Powder Inhalers[J].Molecular pharmaceutics,2018,15(4).
[4] Zhou Q. I. Surface properties of lactose carriers and their effect on drug delivery of dry powder inhaler[J].masters,2008.
[5] L.W.Chan,Q.Zhou,P.W.S.Heng.Comparison of surface roughness parameters obtained by scanning probe microscopy for carrier particles of dry powder inhalers[J].Journal of Drug Delivery Science and Technology,2007,17(3).
[6] M.Leturia,M.Benali,S.Lagarde,I.Ronga,K.Saleh.Characterization of flow properties of cohesive powders:A comparative study of traditional and new testing methods[J].Powder Technology,2014,253.
[7] Kotaro Iida,Youhei Hayakawa,Hirokazu Okamoto,Kazumi Danjo,Hans Luenberger.Effect of Surface Layering Time of Lactose Carrier Particles on Dry Powder Inhalation Properties of Salbutamol Sulfate[J].Chemical and Pharmaceutical Bulletin,2004,52(3).
[8]张蕾,雷勇胜,李晓娜,刘忠洪,蒋庆峰.药物多晶型的分析技术及应用[J].中国新药杂志,2013,22(21):2510-2515.
[9] Craig,Duncan & Reading,Mike(2006).Principles of Differential Scanning Calorimetry.10.1201/9781420014891.ch1.
[10] Chieng Norman,Rades Thomas,Aaltonen Jaakko.An overview of recent studies on the analysis of pharmaceutical polymorphs[J].Journal of pharmaceutical and biomedical analysis,2011,55(4).
[11]夏婉莹,郝英魁,唐辉,傅琳,蒋庆峰.粉末X射线衍射法在药物多晶型研究中的应用[J].中国新药杂志,2019,28(1):40-43.
作者简介
唐露(1992—),药学学士,初级药师,现就职于湖北昌明药业有限公司,研究方向为吸入制剂的新药研发。
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略


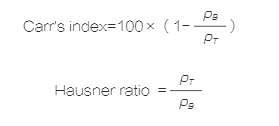















评论
加载更多