只需5分钟皮下注射!强生肺癌双抗新药新剂型在中国申报上市
公开资料显示,这是强生研发的EGFR/MET双特异性抗体埃万妥单抗(amivantamab)与重组人透明质酸酶的皮下给药固定组合。今年6月,强生已经向美国FDA递交这款皮下注射埃万妥单抗的生物制品许可申请,用于目前已批准或已提交的所有埃万妥单抗静脉制剂的适应症,涵盖不同类型的非小细胞肺癌(NSCLC)。根据强生此前的新闻稿,患者能够在5分钟完成该皮下制剂的注射。
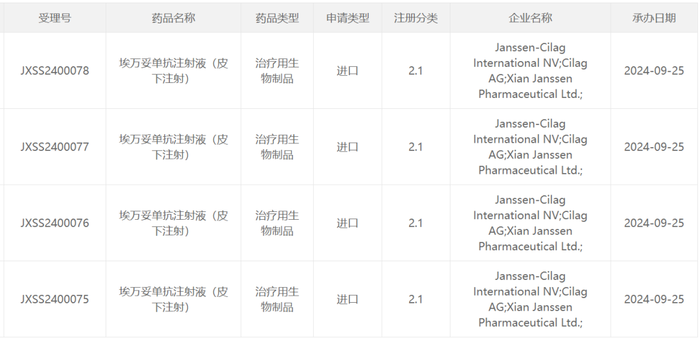
截图来源:CDE官网
埃万妥单抗是一款人源化EGFR/MET双特异性抗体。它具有多重抗癌的作用机制,不但能够阻断EGFR和MET介导的信号传导,还可以引导免疫细胞靶向携带激活性和耐药性EGFR/MET突变和扩增的肿瘤。该产品的静脉制剂最早于2021年5月获得FDA的加速批准,此后陆续获批多项适应症,包括:
EGFR外显子20插入突变、接受铂类化疗过程中或化疗后病情进展的局部晚期或转移性NSCLC成年患者;
联合第三代EGFR-TKI口服药物兰泽替尼片(lazertinib)一线治疗经FDA批准检测证实带有EGFR外显子19缺失或外显子21中L858R替代突变的局部晚期或转移性NSCLC成年患者;
联合标准化疗(卡铂和培美曲塞),用于治疗EGFR外显子19缺失或外显子21中L858R替代突变的局部晚期或转移性NSCLC成年患者。
在中国,埃万妥单抗的静脉注射剂型已有三项上市申请获得NMPA受理,包括与甲磺酸兰泽替尼片组成的联合疗法也已经向CDE递交上市申请。

埃万妥单抗注射液(皮下注射)是埃万妥单抗与重组人透明质酸酶的皮下给药固定组合。根据强生此前新闻稿,在PALOMA-3研究中,针对EGFR外显子19缺失或L858R突变的NSCLC患者,埃万妥单抗皮下制剂与静脉制剂具有相似的总缓解率。皮下制剂还显示出显著缩短的给药时间、输液相关反应减少了5倍,同时总生存期、无进展生存期和缓解持续时间更长。该研究详细试验结果发布于Journal of Clinical Oncology期刊上。此外,2期试验PALOMA-2的数据也支持埃万妥单抗注射液(皮下注射)以每两周和每三周的给药时间频率。
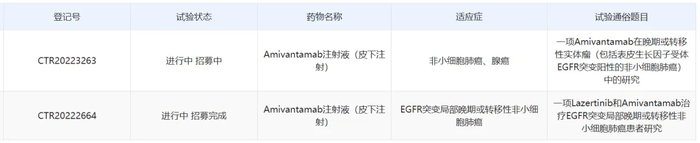
根据中国药物临床试验与信息公示平台官网,强生正在中国开展埃万妥单抗(皮下注射)两项国际多中心临床研究,包括一项2期研究,针对晚期或转移性实体瘤(包括EGFR突变型非小细胞肺癌)患者;以及一项3期研究,针对接受奥希替尼和化疗后出现疾病进展的EGFR突变晚期或转移性非小细胞肺癌患者,评估该产品联合兰泽替尼片的疗效和安全性。
本次这款双抗产品皮下注射剂型在中国申报上市,意味着其在中国的研发进程迎来重要进展。
医药观澜
邵丽竹
何发
热点文章
-
几种典型制药工艺流程图分析
2025-10-11
-
阿司匹林合成工艺及装置改进
2025-10-21
-
辐照辐照灭菌技术在制药行业中的应用灭菌技术在制药行业中的应用
2025-10-11
-
中药颗粒剂生产中的现代化工艺改造
2025-11-04
-
《药包材GMP(2025)》与药品GMP深度对比:核心差异、新增要点与实施指引
2025-11-25
-
2025年50家头部药企的竞争格局与核心趋势分析
2025-10-21
-
一文看懂新药研发到上市的全流程
2025-11-25
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多