评估合成路线,侧重于起始物质、中间体、试剂、催化剂、溶剂、副反应产物和降解产物等。对此,EMEA 建议“应基于扎实的科学评价,全面考虑参与合成的化学反应、原辅料中可能带入新原料药的杂质和可能的降解产物,确定最有可能在新原料药的合成、纯化和贮存期间出现的实际和潜在杂质。”
可能出现在API中的潜在基因毒性杂质一般可分为以下几类:
①未反应的具有警示结构的物料或中间体(如含氮杂环API 中未反应的硝基芳香化合物,由于不完全氢化作用或位置异构体无法环化)。
②与包含警示结构的物料、中间体或API 本身密切相关的物质(如在工艺中用盐酸处理后的含羟烷基的API 的氯烷基类似物)。
③通过溶剂和试剂两者之间的相互合成作用,或与原辅料或中间体的合成作用形成(如由于在磺酰氯的反应中,使用了异丙醇脱氧腺苷酸羟基中间体而形成了异丙醇甲苯磺酸盐)。此外,在API 开发阶段,风险评估还需考虑来源于生产期间或API 长期贮存期间的降解物。
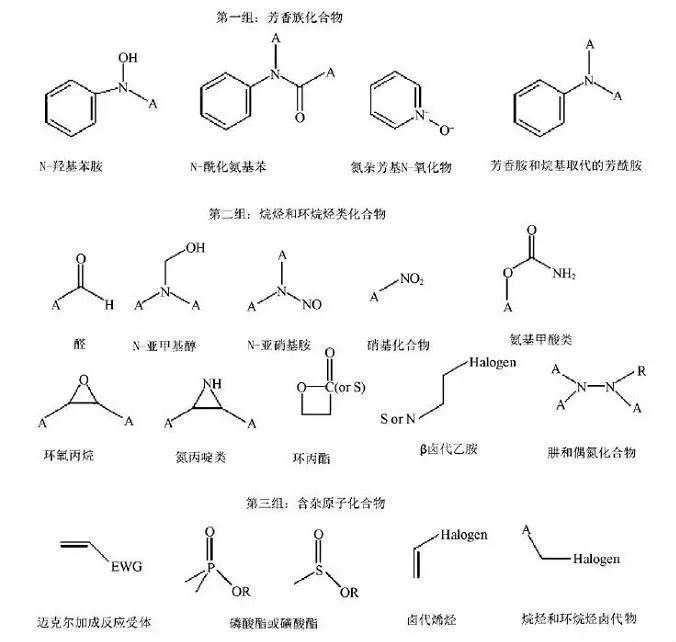
EMEA 和FDA 指南草案都认为使用结构评估是一种有效的方法,可通过它进行基因毒性潜在性的评估。常用的结构评估商业软件是DEREK和Mcase,这两个系统费用昂贵,小公司也可使用基于Ashby 和Tennant 警示的简单系统,详见图1。
一旦完成了结构评估,每个杂质应根据其基因毒性危害进行分类。Lutz Mueller 等确定的5 类分类方案已被广泛用于这个目的,见表2。
此外,SAR 评估程序也是有缺陷的,采用SAR评估程序并不能全面覆盖所有基因毒性杂质。因此需要根据安全性测试(Ames 测试),单独评估这些杂质。如果杂质没有基因毒性标记,但在工艺中作为亲电试剂使用,仍需通过数据库查询确定其是否具有基因毒性,比如美国医学图书馆提供的TOXNET 数据库,可通过共同的门户网站来访问一系列数据库,如有害物质数据库(HazardousSubstances Databank,HSDB)、化学致癌作用研究信息系统(Chemical Carcinogenesis ResearchInformation System,CCRIS)和集成风险信息系统(Integrated Risk Information System,IRIS)等,提供了许多常见化学品的安全性数据。另一个相关的系统是Berkeley 数据库。实际上,采用足够的数据库对化合物特定的成分进行基因毒性风险评估是经常的做法,而不是简单使用TTC 限度进行控制。
一旦确定具有潜在基因毒性的杂质,下一步就是考虑这些杂质带入原料药中的可能性。由于基因毒性杂质经常是高活性的,能够通过下游工艺去除,因此,可以结合杂质的理化性质,在下游工艺处理中采用适当的方式把它们去除。例如,生产工艺中经常遇到的酸性、碱性条件下可分解或去除杂质,或者下游工艺中所用的其他试剂可与基因毒性杂质反应,使其不易反应,从而“安全”。以下针对基因毒性杂质的不同性质,提供可行的工艺去除方法。
许多基因毒性杂质均具有高反应活性,例如酰卤化合物,因其极易反应,使得在反应结果中监测它们几乎无实际意义。而且,如果有任何残留,可以通过某些方法有效地去除,如水淬灭或对所得产物的简单水洗。
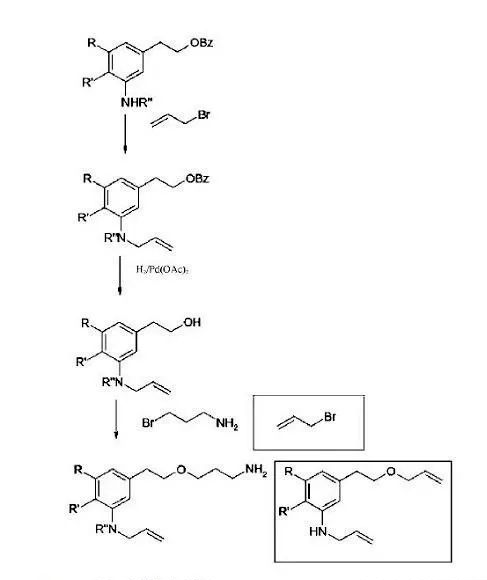
在工艺中,存在某些残留物可能残留在中间体中的可能性。对于这些化合物,在随后的工艺步骤中具有高概率的反应,例如,在合成早期考虑使用烷基卤,另一个烷化剂应在下游工艺中使用,则早期使用的烷基卤残留很可能消耗在后面阶段,见图2。该工艺中,第一阶段用到的烯丙基溴残留到第三阶段,如果仍然存在,将反应生成预期产物的烯丙基类似物。
基因毒性化合物的反应活性可按表6分类,该表只作为一个参考,具体情况应根据实际工艺的化学反应来评估。
许多高度亲电(往往是基因毒性)的试剂、中间体常常用于优化产量和提高产品质量的合成工艺中,并常常在溶液中完成反应步骤。这便意味着基因毒性反应物很可能高度溶于所选择的溶剂。因此,当工艺中将反应产物分离为固体时,基因毒性反应物被残留在反应母液中而除去,这可进一步通过用一种基因毒性试剂易溶而反应产物不溶的溶剂洗涤滤饼,而彻底去除基因毒性反应物。这种情况下,基因毒性试剂的溶解度应在置换溶剂中评估,以便确定合适的清除因子。
许多可能在典型的合成工艺中遇到的基因毒性物质是挥发性的,包括低分子量烷基卤、醛、氮/硫卤乙基芥。常用蒸馏方法来降低或完全去除存在的反应溶剂,因此也可有效地降低或消除残留的基因毒性杂质。这取决于基因毒性相对于溶剂沸点的挥发性。
芳香胺是含能电离基团的潜在基因毒性物质的最好例子。大部分API 和中间体均具有潜在的电离。这种情况下,关注基因毒性物质和基质间可能存在的的电离度差异,便能通过改变水相的pH 值并萃取有机相,来降低基因毒性杂质的水平。
硝基化合物还原至胺便是此类工艺的一个很好的例子。虽然它们具有一个共同的基因毒性代谢物中间体(一个正氮离子),但是可能发现讨论中的硝基化合物具有基因毒性,而其胺类似物则可能没有。在这种情况下,需要去除硝基前体物,特别是如果相关的硝基化合物在下游工艺中不活泼,使得它可能以原形完成该工艺。
对于过量硝基化合物的去除,可以通过使用酸性水层的双相系统,通过液液萃取来实现。任何非电离的硝基化合物将残留在有机相中,而可电离的胺将残留在水层中。弃去有机层,胺则在碱化后在新有机溶剂层中简单地反萃取。
在合成常见的止痛药对乙酰氨基酚中,倒数第二阶段涉及将4-硝基酚还原至相应的胺,反应混合物用甲苯萃取,碱化,再萃取胺。
从通过硅酸床的简单过滤,到制备型液相色谱法,色谱法为API 或中间体中基因毒性杂质的去除提供了多种选择。
制备型液相色谱法一般采用正相模式,即采用极性固定相(一般为硅酸)和非极性流动性(有机溶剂系统)。这与分析型液相色谱法不同,因为大部分分析色谱法都是在反相模式中进行的。制备型液相色谱法采用正相模式是出于分离化合物的需要——使用易被除去的挥发性溶剂。也可以使用反相模式,但是除去基于水性溶剂系统的困难限制了适用范围。
Bandichhor 等报告了利扎曲坦的纯化,利扎曲坦是一种5 羟色胺-HT 受体激动剂,其合成工艺中生成的基因毒性二聚合物杂质不能通过普通的工艺去除,通过分步结晶和重结晶工序,不能达到0.01%的限度。因此,使用适当的pH 值和离子强度改性来开发反相法,增加利扎曲坦和基因毒性二聚合物之间的选择性。基因毒性二聚合物强烈地保留在柱子上,经过优化的负载率达到最大生产率,而没有任何可察觉的基因毒性二聚合物带入到产品中。作者报告了基因毒性二聚合物水平从约40 000 ppm 减少到40~80 ppm( 产率>95%)。
重结晶是去除API 或中间体杂质,包括基因毒性杂质的最有效方法之一。采用该方法需要选择一种适合的溶剂,使API 或中间体在高温情况下高度溶解,而冷却时几乎不溶。高温条件下通过过滤,去除不易溶于热溶剂的杂质,而较易溶于冷溶剂的杂质保留在冷却后的溶液中,通过过滤分离。
除以上技术外,还可通过其他手段去除基因毒性杂质,如活性炭和树脂。活性炭结合重结晶工艺,可非常有效地去除有色杂质。而树脂去除法类似于萃取和分离技术,使基因毒性杂质吸附在树脂上,而所需产品保留在溶液中,从而通过过滤除去杂质。
应用加标、清除法进一步风险评估除了述理论风险评估外,还需要通过加标清除法定量工艺对基因毒性杂质的实际去除能力。加标(spiking)指的是以固定的数量加入需要研究的基因毒性物质;清除(purging)指的是下游工艺去除目标杂质的能力。
一种新型的抗肌瘤产品,盐酸帕唑帕尼的5 个潜在基因毒性杂质的分析控制策略见图3(基因毒性杂质用盒括标识)。
讨论中的杂质中的每一个以高水平(某些情况下高达5%)加标至工艺中。然后使用杂质预定命运图以证明下游产品中水平的连续降低。例如,第1阶段产品含670 ppm 化合物ii,第2阶段产品23 ppm,而第3 阶段产品中间级API 和最终API含不到1.7 ppm(化合物ii)。这使他们集中于起始物料或中间体的上游控制,并避免需要在制剂中进行控制。这种方法的吸引力是它允许控制限度
设定在较高水平,并保证下游的清除将降低相关物质的水平至可接受水平。
它也允许控制策略基于不太复杂和灵敏的分析方法,这些方法更与常规质量控制环境有关。


















评论
加载更多