多糖链长度和结合方式对多糖结合疫苗免疫源性的综合影响
抗菌糖结合疫苗的开发和使用显著减少了潜在致命的儿童和成人疾病的发生,例如菌血症、细菌性脑膜炎和肺炎。在这些疫苗中,细菌多糖与载体蛋白的共价连接通过触发 T 细胞依赖性 B 细胞反应来增强糖抗原的免疫原性,从而产生高亲和力的抗体和持久的保护。已获批的糖结合疫苗含有长链细菌多糖、中等大小的寡糖或短合成多糖。在这里,我们讨论影响疫苗中多糖链长度的因素,并回顾讨论多糖链长度对疫苗功效影响的现有文献。此外,我们评估了针对两种细菌病原体(b 型流感嗜血杆菌和 C 型脑膜炎奈瑟菌)的不同链长度的获批糖结合疫苗制剂的现有临床数据,了解多糖链长度与其功效的可能相关性。我们发现与载体蛋白交联的长链多糖和与载体末端连接的中等大小的寡糖都实现了高免疫原性和功效。然而,含有长的、不受束缚的天然多糖链的末端连接糖结合物可能会通过 B 细胞的 T 细胞独立激活而诱导低反应性,而交联的中等大小的寡糖可能会遭受非最佳糖表位可及性的影响。
细菌多糖分子是多功能化合物,包括脂多糖及其 O 抗原、荚膜多糖和胞外多糖。它们作为细菌病原体的毒力因子发挥着重要作用,并通过至少三种方式保护细菌免受宿主免疫反应的影响。首先,表面多糖保护细菌结构免受先天免疫系统替代补体途径的破坏性活动。其次,荚膜多糖也会阻碍经典的补体途径,因为抗体无法轻易到达荚膜下细菌表面蛋白,从而阻碍随后的补体沉积。第三,对细菌多糖的适应性免疫仍然低效,因为糖结构与抗原呈递细胞的主要组织相容性结合物 (MHC) 的结合很差,这导致 T 辅助细胞依赖性抗体反应被最小化。后者可能解释了为什么许多宿主依赖性细菌在进化过程中形成了表面碳水化合物结构。
细菌多糖还有助于微生物定植特定生态位、抵抗抗生素和对抗噬菌体的能力。它们在许多细菌病原体中无所不在,长期以来引起了人们对这些化合物用于疫苗开发的兴趣。细菌多糖的多糖链形成可被 B 细胞受体 (BCR) 识别的表位或抗原决定簇。这些表位本质上可以是线性的或构象的,并且可以由最小范围的相同单糖(在同聚多糖链中)或各种不同的单糖(包括侧链)(在杂聚多糖链中,图1)组成。到了 20 世纪 70 年代和 80 年代,细菌荚膜多糖疫苗成为常规疫苗接种的一部分,并且已经针对由脑膜炎奈瑟菌、b 型流感嗜血杆菌 (Hib)、伤寒沙门氏菌和肺炎链球菌引起的疾病建立了基于纯化多糖的成人疫苗。这些普通(即未结合的)多糖疫苗的免疫原性取决于长链多糖交联 B 细胞上表面免疫球蛋白受体的能力,从而产生具有典型 T 细胞非依赖性特征的抗体反应。
图 1:细菌多糖抗原决定簇(表位)的主要类型。
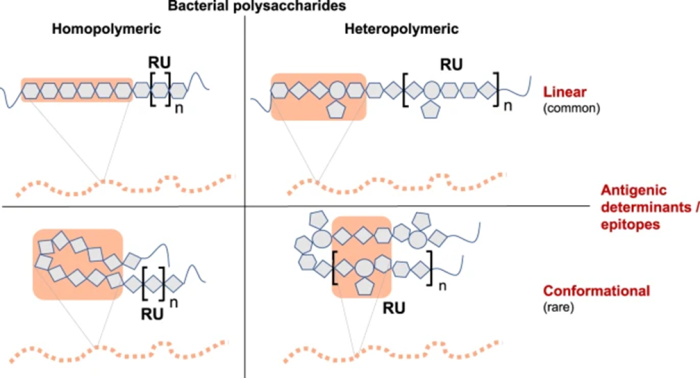
在同聚多糖中,相同的单糖残基重复形成聚合物。在杂聚(或复合)多糖中,重复单元(RU,在方括号中)由不同的单糖残基组成,并且可能包含支化侧链。线性表位中抗原性所需的最小单位由大约 6-7 个连续的单糖组成。线性表位可以包括多糖链的末端单糖残基。构象表位由空间上非常接近但分散在其一级序列中的残基形成。这些需要足够长的残基序列来构建或模拟与抗体相互作用所需的空间构象。例如,脑膜炎奈瑟菌 B 组荚膜多糖抗原的同聚物构象表位包含 10 个残基,但只有内部 6 个残基与其同源抗体相互作用。超过已识别抗原表位长度的多糖片段通常用作多糖结合疫苗中的免疫原。
细菌多糖本身通常仅诱导相对短暂的不依赖于 T 细胞的免疫反应,并且很大程度上无法激活记忆 B 细胞 和长寿命浆细胞的成熟。因此,它们主要诱导低亲和力抗体反应,并且不能有效引发长期可增强的免疫记忆。由于其不依赖于 T 细胞的性质,普通多糖疫苗(例如针对 Hib 的疫苗)不会诱导抗体反应,因此对 2 岁以下婴儿无效。幸运的是,多糖与载体蛋白的结合可以将这些化合物转化为 T 细胞依赖性抗原,从而诱导高亲和力抗体、抗体同种型转换和持久记忆免疫反应,使它们对婴儿有效。多糖与载体蛋白的结合允许结合物与糖特异性 B 细胞结合、结合物的内化以及 MHC 将载体蛋白衍生的肽表位呈递给 T 辅助细胞。这最终导致同源 B 细胞的克隆激活,并分化为产生抗体的浆细胞,同种型转变为 IgG 和亲和力成熟,并分化为记忆 B 细胞。
目前所有获批的多糖结合疫苗都含有五种载体蛋白之一:包括破伤风类毒素 (TT)、白喉类毒素 (DT)、白喉毒素的基因修饰交叉反应物 CRM197、脑膜炎球菌外膜蛋白结合物 OMPC 或流感嗜血杆菌蛋白 D HiD23。然而,人们也在积极探索各种替代载体蛋白,例如铜绿假单胞菌外毒素 A 的修饰版本24,25 和肺炎链球菌 ABC 转运蛋白 PiuA。
在获批疫苗使用的五种载体中,CRM197和TT是迄今为止使用最多的载体。DT 通常效力较低,可能是由于化学脱毒过程中表位失活, OMPC 和 HiD 都很少使用。载体与多糖分子共价结合,要么在多糖末端的糖模体激活后形成端联构型,要么在随机激活多糖链后形成交联物质(图 2)。
图 2:四种可能的多糖激活类别。
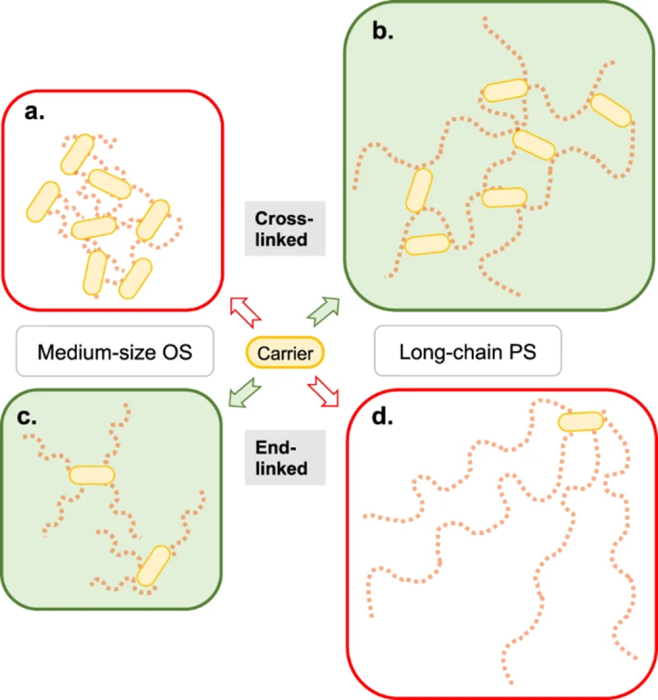
显示了所得糖结合物的基本结构。多糖链被描绘为红色方块串,其中每个方块表示一个表位(见图 1)。多糖的随机激活会产生交联的中等大小寡糖 (OS) 糖结合物 (a) 或交联的长链多糖 (多糖) 结合物 (b)。多糖末端的激活产生末端连接的中等大小的 OS 糖结合物 (c) 或末端连接的长链多糖结合物 (d)。很少进行多糖链两端的激活可能会产生具有低至中等交联水平的疫苗。在目前的实践中,b 和 c 可以产生更好优化的糖结合物疫苗。
糖结合物的特定理化性质会影响疫苗的功效,而关键参数,例如用于结合的多糖的分子大小和交联程度,可能对疫苗的免疫原性产生深远的影响。例如,每个载体蛋白的附着位点数量需要足够高,以确保有效结合,限制残留游离多糖分子的水平。然而,载体蛋白的衍生化程度需要仔细优化,以避免蛋白质序列内关键 MHC 表位受到不必要的破坏,从而消除其 T 细胞刺激活性。这些关键参数的选择以及载体蛋白的选择以及活化和结合化学反应受到疫苗生产过程中纯化步骤的实用性的影响,其中结合与未结合多糖的粘度和分子量比可能会影响最终产品的纯度和产量。因此,已采用不同的工艺化学和结合方法来制备这些结合物。这些化学过程包括引导蛋白质-多糖连接位点及其每个分子数量的激活程序,以及在两个糖结合物成分之间引入间隔分子。
疫苗生产中获得的微生物多糖的主要质量属性之一是每个多糖链的重复单元的数量,称为聚合度或链长度。该链长很大程度上受生产工艺的影响。通常,在激活和与特定载体蛋白化学连接之前,多糖的尺寸会从非常大的分子 (> 500 kDa) 减小到约 100–300 kDa 的多糖异质混合物。多糖分子尺寸的减小提高了疫苗生产中后续的结合效率。
普通细菌多糖的免疫原性水平与其大小相关,因此也与其链长度相关。因此,大多糖尺寸的测定成为保证普通多糖疫苗免疫原性的关键质量测量,这可能是因为需要交联 BCR 以引发不依赖于 T 细胞的抗体反应。但这种关联对于多糖结合疫苗来说也成立吗?与普通多糖疫苗不同,糖结合物诱导抗体机制并不依赖于 BCR 的交联。相反,糖结合物被抗原呈递细胞内化,导致载体蛋白衍生肽触发 T 辅助细胞反应。尽管存在这种差异,对多糖链长度的依赖性是否仍然存在?为了澄清这个问题,对有关链长差异对多糖结合疫苗功效的影响的现有文献进行了以下调查。
原文:C.Anish, M.Beurret, J.Poolman, Combined effects of glycan chain length and linkage type on the immunogenicity of glycoconjugate vaccines. NPJ Vaccine, 2021.
撰稿人 | 开朗的豌豆射手 生物工艺与技术
责任编辑 | 胡静
审核人 | 何发
邵丽竹
何发
热点文章
-
几种典型制药工艺流程图分析
2025-10-11
-
阿司匹林合成工艺及装置改进
2025-10-21
-
辐照辐照灭菌技术在制药行业中的应用灭菌技术在制药行业中的应用
2025-10-11
-
中药颗粒剂生产中的现代化工艺改造
2025-11-04
-
《药包材GMP(2025)》与药品GMP深度对比:核心差异、新增要点与实施指引
2025-11-25
-
2025年50家头部药企的竞争格局与核心趋势分析
2025-10-21
-
一文看懂新药研发到上市的全流程
2025-11-25
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多