施维雅|利用高通量AI驱动的平台改变药物发现:Patrimony平台5年经验回顾

背景
人工智能能够分析包括化学结构、多组学、临床前和临床数据在内的庞大而多样化的数据集,进而推动药物发现方法发生变革。
鉴于一些初步的成功,制药行业现在正在通过实施工业化平台,广泛采用人工智能和机器学习来支持药物发现。这些计算平台旨在利用内部和公共数据源为靶点识别、治疗方式选择和后续药物设计提供信息。与传统的发现方法相比,这种基于模型的策略可以最大限度地减少对大量试错方法的需求,从而节省宝贵的时间和资源。
知识图谱及其在药物发现和精准医学中的应用
Patrimony的核心是知识图谱(KG),这是一种用于集成和解释大量多模态数据的经典工具。
KG是用于表征实体(节点)之间关系(链接)的结构。在生物医学领域,KG的结构将多种类型的节点(如基因、药物或疾病)与连接节点的边缘(如蛋白质之间的物理或功能相互作用)组装在一起,用于表征从众多数据集中积累的关于医学和生物实体之间复杂相互作用的知识。
Patrimony在疾病模型、靶点优先排序和药物再利用中的应用
为了表征受干扰的生物系统在具体疾病中的复杂性,Patrimony被设计为整合各种类型的相互作用,包括蛋白质-蛋白质、基因-分子功能和药物-靶点。Patrimony集成了内部和外部数据库,包括 Drugbank(药物-靶点),DisGeNET(基因-表型)和反应组(基因-生物过程),以生成将疾病与基因和药物联系起来的综合图(图1)。
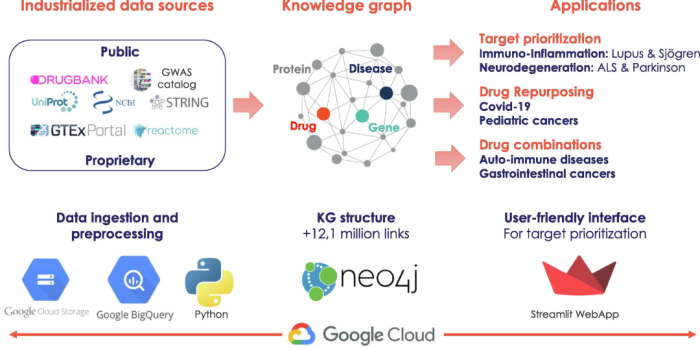
图1 Patrimony的主要应用和底层结构概述
在Patrimony中,数据被部署在Google云平台(GCP),使用自动化管道定期从原始数据源中提取数据。在Neo4j(https://www.neo4j.com; KG工具)中,数据被进一步处理成节点和链接,以构建作为Patrimony骨架的图形(图1)。
Patrimony最早用于确定两种自身免疫性疾病(原发性斯约格伦综合征和系统性红斑狼疮)的优先靶点。根据对疾病因果关系的推断,以及对相关性、安全性和可药用性的预测,利用Patrimony确定了两个原始治疗靶点,从而启动了新药研发项目。
Patrimony在神经退行性疾病中的应用
施维雅对Patrimony平台进行了调整,以应用于肌萎缩性脊髓侧索硬化症(ALS)和帕金森病(PD)这两种神经退行性疾病的靶点优先排序。
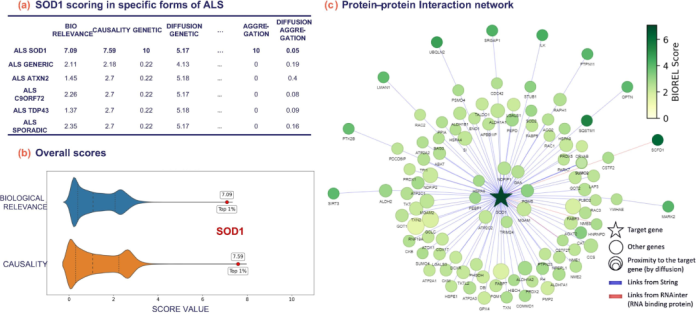
图 2. 肌萎缩性脊髓侧索硬化症(ALS)中SOD1的选定靶点优先级输出
与平台产业化相关的关键成功因素和挑战
产业化的目标,是创建一个高效、可重复和可扩展的工作流程,用于分析和管理数据,同时为最终用户生成可解释的输出结果。
考虑到这些目标,获取高质量数据和算法的透明度被认为是确保计算模型准确性的关键因素。
数据质量
在Patrimony中,内部或外部的主要数据源可重复用于其他计算工具的并行开发,从而促进整个研发(R&D)价值链的互操作性。
算法的透明度
在这方面,Patrimony平台产业化的另一个成功因素是建立一个用户友好型界面,让没有编码经验的科学家也能访问结果。Patrimony利用 Streamlit构建的界面(图 1、图 2),提供了浏览不同疾病相关性评分的灵活性,同时还允许通过安全登录流程访问底层数据源。
面临的多重挑战
在为神经系统疾病开发Patrimony时的一个教训是,要使该平台适用于各种治疗领域,必须具备工具的多功能性。因此,保持工具的持续进化至关重要,这样才有可能添加新的数据源,并以试验和学习的方式调整分析方法。这种演变在工业化环境中很难适应,因为工业化环境基于标准化的工具和方法,并有确保数据管理和良好编码实践的程序。
另一个挑战是基于人工智能的模型往往缺乏验证,因此需要通过临床前湿法实验室实验和/或人体临床研究来证实计算模型的预测输出。同时,施维雅还利用不同的数据源和分析方法,将预测性计算模型的输出结果与正交的计算模型进行交叉验证,以得出趋同的结果。
经验:尽早让人类专家参与进来
Patrimony的开发时间表、扩展前景
Patrimony是一个多功能平台,可轻松应用于所有感兴趣的治疗领域。
取得了多项重要成果
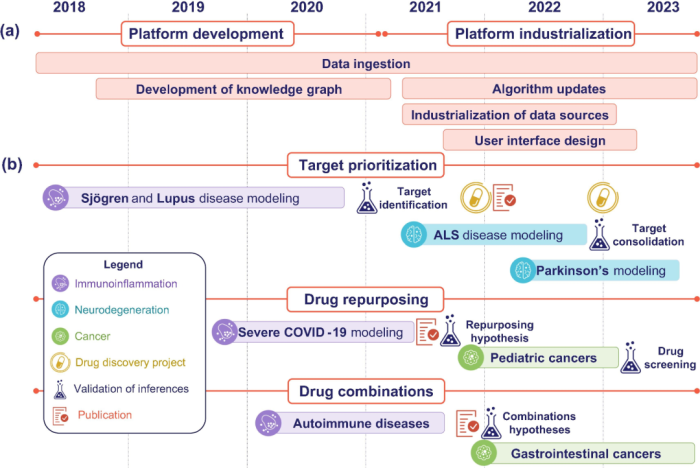
图3 Patrimony开发和产业化期间的时间表和成就
Patrimony的另一项重要成果是展示了计算建模在深入了解相关疾病方面的能力。这些疾病模型为公司专有,具有显著的竞争优势,因为可以通过有效查询这些疾病模型来设计创新的治疗方案,特别是在全面了解疾病病理生理学的基础上选择更相关的治疗靶点。
未来发展的关键点
首先是在工业化环境中保持不断发展的能力,这需要整合新的数据源,改进分析方法,开发新的应用,同时确保数据质量和标准化流程(图 4)。
这就要提到大型语言模型(LLMs)。应用大型语言模型可以进一步挖掘KG的组成部分,因为它们具有自然语言处理能力。LLMs正被用于支持药物发现,以解释海量的科学信息,从而实现对基于非结构化文本数据的组学数据的补充,其产出包括靶点识别、因果疾病建模和候选药物安全性评估等。
其次是开发或搭建可互操作的工业工具或其他计算平台,将Patrimony等平台进一步嵌入基于人工智能的端到端研发价值链支持中,从而提高临床前候选药物的成功概率,并缩短研发时间(图 4)。
施维雅正在将Patrimon与另一个KG结合起来,以挖掘来自多个来源的大量异构药理学和生物学数据。这个KG支持根据不同治疗模式(如小分子、反义寡核苷酸和生物制剂)与特定靶点的相互作用能力来确定它们的优先次序,AlphaFold预测的蛋白质结构可为这一工作提供便利。
可补充Patrimony功能的其他模型包括:可评估靶点或候选药物安全性的模型,通过对大型化学空间进行虚拟筛选来确定候选药物的模型,通过多任务并行预测候选药物来优化hit的模型,以及通过使用虚拟患者、数字孪生或因果疾病模型来预测药物疗效的模型(图 4)。
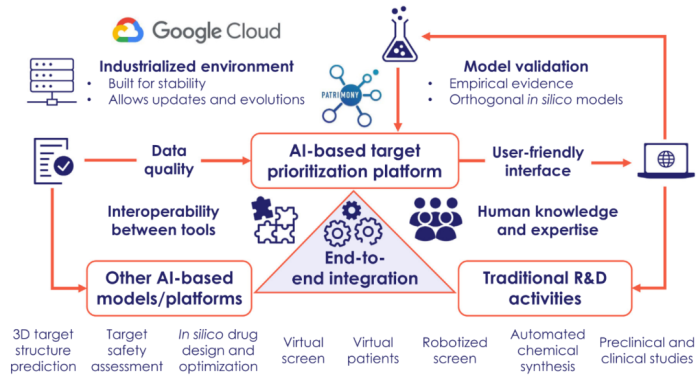
图4. Patrimony和其他基于AI的平台与传统研发活动的端到端整合
进一步发展Patrimony,需要将其他基于人工智能的平台与传统研发活动进行端到端整合,以支持靶点安全性评估、计算药物设计、虚拟患者中的优化和评估。包括高通量自动化化学合成、机器人湿实验室筛选以及确证性临床前和临床研究。
第三个要点是,计算平台和人工智能的变革力量在于将计算预测建模与传统的制药研发活动充分结合起来(图 4)。
例如,建模活动可与自动化化学合成、机器人湿实验室筛选以及确证性临床前和临床研究相结合,以提高药物发现的效率和规模。通过采用混合现实(mixed-reality)方法,将预测性虚拟模型的输出与现实世界的实证研究无缝结合,可以彻底改变人工智能、药物发现和开发的能力。
开发人类智能和人工智能的融合将是一项关键挑战,需要进行必要的文化适应和培训,以帮助人类专家利用这些计算方法的优势,并在平台中获取他们的知识,使他们成为制药业正在进行的这场深刻变革的积极参与者。
参考资料
撰稿人 | 智药邦
责任编辑 | 胡静
审核人 | 何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多