多家药企「冲刺」基药目录
01
多家药企做好准备
“冲刺”2000亿市场
本该3年一调的国家基药目录,自2018版发布后一直未有更新。此前,业内推测新版基药目录将在今年6月更新,但赛柏蓝在5月9日于山东青岛举办的第86届全国药品交易会上了解到,有专家指出,6月发布新版基药目录的可能性不大。
“征求意见稿和目录之间一般间隔两个月,即使5月出征求意见稿,最早也要7月(才会发布目录)”。
进入基药目录的品种在销售方面一般能得到正向拉动,根据赛柏蓝在今年药交会现场的观察,医保、独家、基药,仍然是工业企业招商的核心卖点。
在多方信源都认为基药目录将在2023年进行调整的前提下,一批企业在加快推进准备工作。
例如,今年4月末,一品红在接受机构调研时表示,目前正在等待有关部门启动基本药物目录申报,芩香等多个产品循证医学证据研究充分,有较强竞争力,并且前期做了大量准备工作,预计应该会有一个好的结果。
包括一品红在内,今年已有贵州百灵、葵花药业、桂林三金、佛慈制药、盘龙药业等多家药企在投资者关系活动中传递出对进入基药目录的积极态度,有企业提出“借助(进入基药目录)这个正向拉动,为今年全年销售任务的完成增添保障”。
对于药企而言,品种进入基药目录往往也意味着广覆盖。
据业内相关统计,2018年版基药目录中新增的187个品种对应市场规模约1600亿元,按照2018年和2012年基药目录调整中调入、调出的品种数量推算,新版基药目录覆盖的品种总数或将超过900个,其所涉市场规模也将超过2000亿元。
长期以来,因不同地方医生开药、患者用药存在较大差异,基药的“986”使用比例要求,各级医疗机构完成得一直不太理想。
国家发布的多份文件,都对基药目录的使用提出了明确的要求。
4月10日,国家卫健委发布《关于2021年度全国二级公立医院绩效考核国家监测分析情况的通报》提到,基本药物主体地位不明显,二级公立医院基本药物采购品种数占比45.73%,较2020年下降1.06个百分比。
国家卫健委医政医管局在《关于印发国家二级公立医院绩效考核操作手册(2022版)的通知》中提出,基药在二级公立医院的定位要上升到主导地位。
基药的重要性不言而喻,对于企业而言,药品进入基药目录可以帮助其快速进院,不少医院还会单独召开基药药事会,引进基药品种;同时,可以帮助药品销量提高,在“986”的要求下,二三级公立医院的基本药物配比还会不断提高等。
02
突出主体地位
基药品种猜想
一直以来,基本药物遴选按照“突出基本、防治必需、保障供应、优先使用、保证质量、降低负担”的功能定位,坚持中西药并重、临床首选的原则,参照国际经验合理确定。
接下来,基药目录将如何调整?
2012版基药目录发布时,其覆盖病种范围就在2009版囊括常见病、多发病的基础上,拓展至重大疾病(儿童白血病、终末期肾病、血友病)、妇女儿童用药,其中可用于儿童的品种近200种,儿童专用剂型、规格达到70余个。
2021年发布的《国家基本药物目录管理办法(修订草案)》公开征求意见稿又增加了儿童药品目录,这无疑将利好大批布局儿药的企业。
另一方面,2018年版的基药目录在以临床主要病种为基础的同时,重点聚焦癌症、儿童、慢性病等病种,新增品种包括抗肿瘤用药12种、临床急需儿童用药22种,以及国内唯一一个全口服、泛基因型、单一片剂丙肝治疗新药。
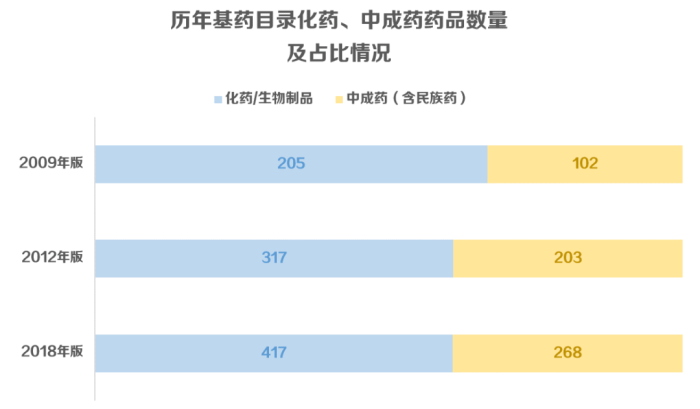
此外,今年3月国家卫健委在《对十三届全国人大五次会议第1996号建议的答复》中,再次提到“坚持中西药并重”的原则,历年三版基药目录中成药占比逐次从33%左右提升到39%,新版基药目录中成药占比或将在此基础上再次升高。
在基本药物市场准入的路径及趋势方面,上述专家将其分为三类:
一是“自动准入”,障碍较小,如2021版WHO基本药物目录中药品,三批《鼓励研发申报儿童药品清单》中的药品(名单见文末附1),临床价值高的新冠治疗药品;
二是“半自动准入”,专家投票比较重要,包括医保甲类药品、独家中成药、国采药品;
三是“被动准入”,专家投票极其重要,如国谈药品、医保目录乙类药品、眼科药品。
对于企业而言,基药目录准入和医保目录准入类似,企业高层、中层、一线人员要在证据产生和传播中协同,才能发挥证据的助推作用。
《药品临床综合评价管理指南(2021年版试行)》指出,药品临床综合评价是以临床价值为导向,综合真实世界数据、药品供应保障各环节信息来评价药品的安全性、有效性、经济性、创新性、适宜性、可及性。
上述6个维度可以为基本药物遴选提供证据,接下来,想要产品进基药目录,企业可以自己或找第三方做药品经济、临床评价的证据评价等。
END
内容来源: 责任编辑:胡静 审核人:何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多