一波三折!首款口服粪便微生物疗法获得FDA批准

SER-109是该公司的研发重点之一,它由多种厚壁菌门菌种的纯化细菌孢子组成。这些微生物在调节艰难梭菌生命周期和CDI疾病发生方面具有重要作用。在1b期临床试验中,高达86.7%的患者达到试验主要终点。2015年,美国FDA授予这一疗法突破性疗法认定,意味着它与已有CDI疗法相比,具有为患者提供显著获益的潜力。
然而,2016年Seres宣布SER-109在2期临床试验的中期分析中未达到主要终点,在接受治疗8周之后,患者与对照组相比,CDI复发风险并未显著降低。这一结果为SER-109的开发前景蒙上了一层阴影。
对临床试验数据的进一步分析显示,对CDI患者的误诊和用药剂量不足可能是导致试验结果不如预期的原因。接下来是对疗法漫长的进一步优化和启动新一轮的临床试验。在这个过程中,Seres公司经历了公司重组,在2019年不得不裁员30%,将资源集中用于推动少数几个后期临床开发项目上。幸运的是,研究人员始终对SER-109的潜力充满信心,将其视为继续研发的重点项目之一。
Seres公司的坚持在2020年终于收获回报,在关键性3期临床试验ECOSPOR III中,SER-109达到试验的主要终点,接受治疗8周后,SER-109组患者的复发率为12.4%,而安慰剂患者为39.8%。与安慰剂组相比,SER-109治疗组的疾病复发相对风险为0.32(95% CI,0.18,0.58)。这项临床试验的结果在著名医学期刊《新英格兰医学杂志》和《美国医学会杂志》上发表。去年10月,SER-109的生物制品许可申请获得美国FDA授予的优先审评资格。
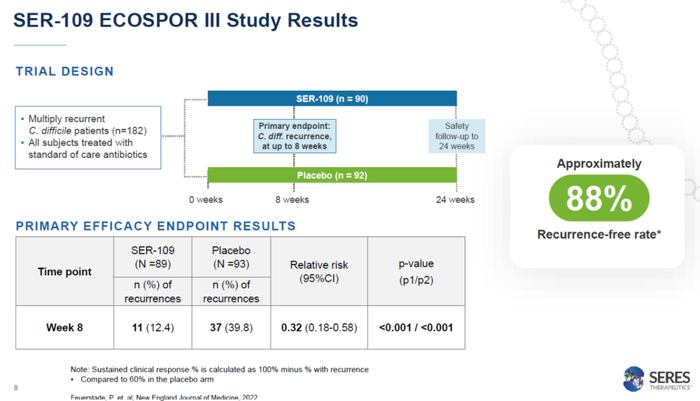
▲SER-109的3期临床试验结果(图片来源:Seres公司官网)
Flagship Pioneering的创始人兼首席执行官Noubar Afeyan博士在今年年初发表的公开信中表示,创新技术平台的突破需要时间。核聚变研究在经过几十年的挫折之后,在去年年底获得突破。基于mRNA的新抗原癌症疫苗去年首次在随机对照临床试验中显著降低黑色素瘤复发或死亡风险,而Moderna的mRNA技术平台也经历了近10年的优化。Seres公司从创建至今,其口服肠道微生物组平台也经历了十余年的优化。如今,SER-109不但为解决未竟医疗需求提供了新选择,也有望开启微生物疗法的新时代。
诚然,将微生物疗法推广到治疗其它疾病仍然有许多路要走,前途也充满了各种挑战,近日,Seres公司的另一款微生物组疗法SER-287在治疗溃疡性结肠炎的临床试验中并未达到预期效果。然而,Noubar Afeyan博士在公开信中坚定地表示,面对挑战的坚韧不拔是创新者必须具备的品质。这些突破的实现提醒我们,将目光专注于远在地平线上的终极目标将带来无限的可能性!
内容来源:药明康德
责任编辑:胡静 审核人:何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多