渤健超10亿美元引进!帕金森病潜在“first-in-class”疗法在中国启动临床
中国药物临床试验登记与信息公示平台显示,渤健(Biogen)启动了一项国际多中心(含中国)2b期临床研究,以评估创新疗法BIIB122的安全性及其是否能减缓30至80岁早期金森病受试者疾病恶化。公开资料显示,BIIB122(又称DNL151)是一款潜在“first-in-class”的LRRK2小分子抑制剂,目前正在海外开展治疗帕金森病的3期临床试验。2020年,渤健与Denali Therapeutics达成一项超10亿美元的合作,从而获得合作开发和共同商业化BIIB122的权益。
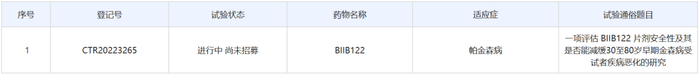
截图来源:中国药物临床试验登记与信息公示平台
在与帕金森病相关的基因中,LRRK2基因被认为是个关键因子。研究发现,患者携带的LRRK2基因突变与细胞培养环境中神经元的病理蛋白激酶活性相关,这引起了研发人员研发LRRK2激酶抑制剂的兴趣。虽然携带LRKK2基因突变的患者只占帕金森病患者总数的一小部分,但是最近研究发现,在从患者身上获取的多巴胺神经元和小胶质细胞中,野生型LRKK2蛋白激酶的活性也有所升高。因此,以LRRK2为靶点的疗法被认为在帕金森病中具有一定治疗潜力。
公开资料显示,BIIB122正是Denali公司开发的一款小分子LRRK2激酶抑制剂。该公司的研究表明,抑制LRRK2活性可恢复溶酶体的功能,这不但对携带LRRK2基因突变的帕金森病患者有效,还可能对不携带LRRK2基因突变的患者也产生疗效。
2020年8月,渤健和Denali公司宣布达成一项协议,双方将在美国和中国合作开发和共同商业化DNL151,用于治疗帕金森病。渤健将负责该产品在所有其他市场的商业化。根据协议,渤健将向Denali公司支付5.6亿美元的前期付款,并对后者进行4.65亿美元的股权投资。根据LRRK2项目开发情况,Denali公司还有资格获得高达11.25亿美元的潜在里程碑付款。

根据中国药物临床试验登记与信息公示平台,此次渤健启动的是一项2b期、国际多中心、随机、双盲、安慰剂对照研究,主要终点指标是治疗期间(最长144周)MDS-UPDRS第II和III部分评分总和至明确恶化的时间。该试验计划在全球109家研究中心开展,计划在国际入组640人,在中国入组9人。该研究的中国部分由北京医院主任医师陈海波医生担任主要研究者。
此前,BIIB122已在早期临床研究中取得积极结果。在健康志愿者中开展的1期研究(N=184)和在帕金森病患者中开展的1b期研究(N=36)结果显示,通过pS935 LRRK2和pT73 Rab10测量,BIIB122治疗参与了靶点调控和下游信号通路,并且实现了尿液中溶酶体脂质BMP(溶酶体功能的生物标志物)水平的剂量依赖性减少。
Denali公司曾在新闻稿中指出,早期研究结果不仅表明LRRK2是一个潜在改善帕金森病的新靶点,也支持BIIB122作为一种减缓帕金森病进展的潜在“first-in-class”口服疗法。

图片来源:123RF
帕金森病(PD)是一种进行性的神经退行性疾病,通常发生在50~70岁的老年人身上。该病由于产生神经递质多巴胺的脑细胞逐渐丧失引起,大脑中多巴胺的下降导致广泛的运动和非运动症状。上世纪70年代以来,该病主要的治疗方法为左旋多巴。然而随着时间的推移,左旋多巴可能导致不自主、不受控制的运动。到目前为止,帕金森病仍然无法完全治愈,因此开发出有效治愈帕金森病的疗法是科学家的当务之急。
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多