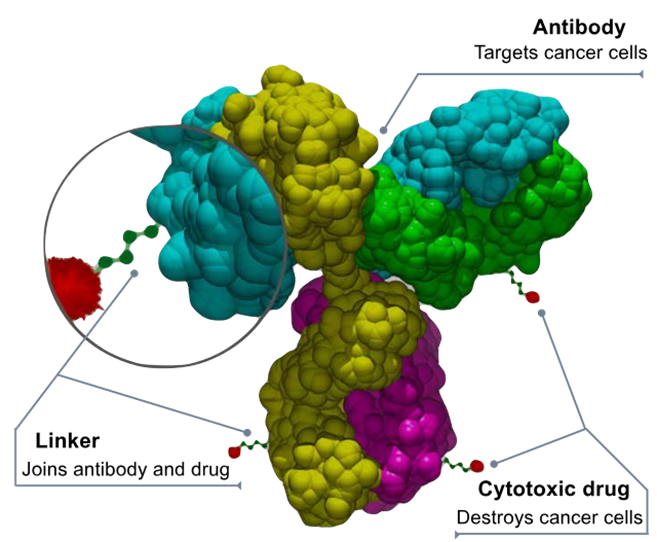
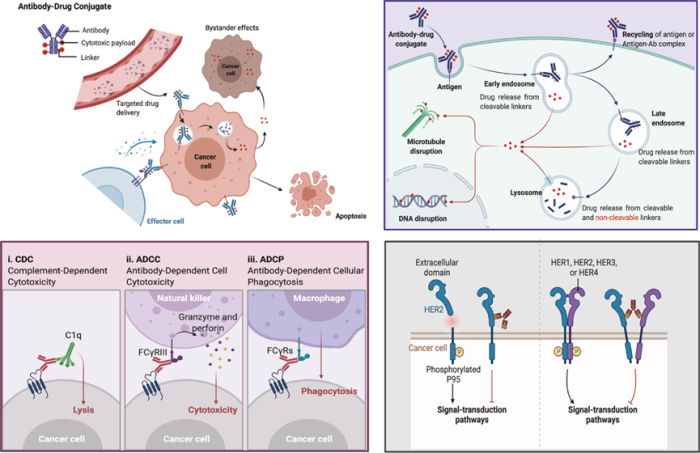
抗体-药物偶联物由抗体、连接子和毒性小分子组成,兼具抗体的高特异性和毒素分子的强效杀伤能力,能够精准靶向并杀死肿瘤细胞,已成为临床肿瘤治疗的重要组成部分,也是目前创新药物研发的热点。
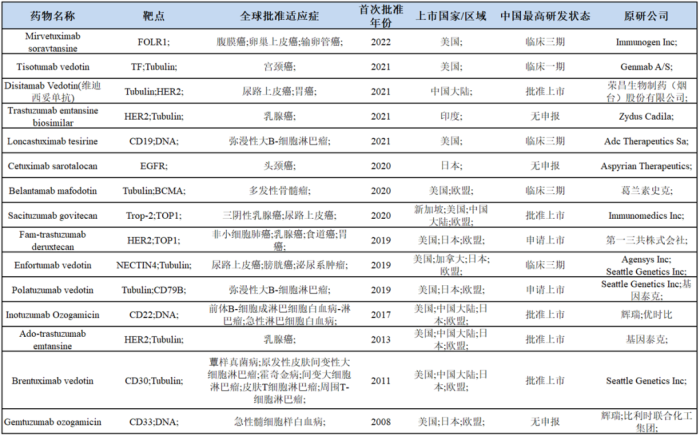
截至2022年12月18日,全球共有15款ADC药物获批,FDA批准了其中的12款,适应症包括实体瘤和血液瘤。国内则有5款ADC获批,分别是Seagen的Brentuximab vedotin、基因泰克的Ado-trastuzumab emtansine、辉瑞的Inotuzumab Ozogamicin、Immunomedics的Sacituzumab govitecan和荣昌生物的维迪西妥单抗,另有第一三共的Enhertu和罗氏的Polivy提交NDA。
“魔法子弹”ADC可为患者带来较大临床获益,甚至改变肿瘤治疗范式。
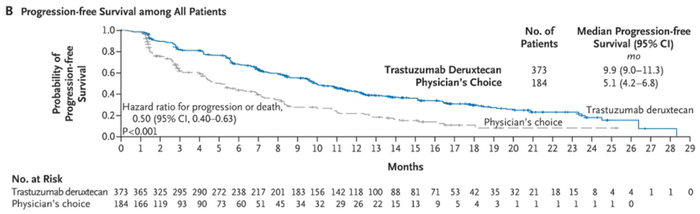
由Seagen开发的靶向CD30的Adcetris已成为难治性霍奇金淋巴瘤和外周T细胞淋巴瘤的一线疗法,改善了患者的治疗结局;第一三共/阿斯利康的DS-8201则革新了整个HER2+乳腺癌的治疗格局,对HER2-乳腺癌人群同样具有极佳疗效,在今年ASCO上公布的DESTINY-Breast04试验中,DS-8201相比化疗,让HER2低表达乳腺癌患者的中位无进展生存期从5.4个月延长到10.1个月,中位总生存期从17.5个月延长到23.9个月,实现了HER2靶向药物在HER2低表达患者上的疗效突破。2022年,8月5日,FDA批准DS-8201用于不可切除或转移性的HER2低表达乳腺癌,改写了乳腺癌的分类标准。
2022年8月11日,FDA又加速批准DS-8201用于HER2突变的非小细胞肺癌,成为首个用于肺癌的HER2靶向疗法。
然而,抗体-连接子-毒素分子的多重组合,就如同是一把双刃剑,在给ADC药物带来强大疗效的同时,也给它带来了毒副作用发生率、严重程度均高于一般单抗和小分子的缺点。
在FDA批准的12款ADC中,仅2021年批准的靶向CD19的Loncastuximab tesirine和2019年批准的靶向CD79的Polatuzumab vedotin未被添加黑框警告,其余10款ADC均被添加黑框警告(FDA对某种处方药潜在危险或可能致命的风险的总结,在药品说明书醒目位置使用加黑加粗的边框加以突出),黑框警告概率远远高于普通的小分子及单抗,涉及到的毒副作用包括严重的肝毒性、眼毒性、严重的皮肤反应、中性粒细胞减少、进行性多灶性白质脑病及间质性肺病(ILD)等。
1)根据一项囊括169项临床试验共22492名患者的meta分析[1],使用ADC药物进行治疗时,所有级别不良反应的总发生率为91.2%,
≥ 3
级不良反应的发生率为46.1%,常见不良反应与化疗药物报导的类似,如淋巴细胞减少症(53.0%)、恶心(44.1%)、中性粒细胞减少症(43.7%)、视力模糊(40.5%)和周围神经病变(39.6%),主要为剂量限制性的脱靶毒性。这169项研究中有153项报告了ADC治疗导致的患者死亡,总体发生率为1.3%,死亡的直接原因主要为肺炎、败血症和呼吸衰竭。
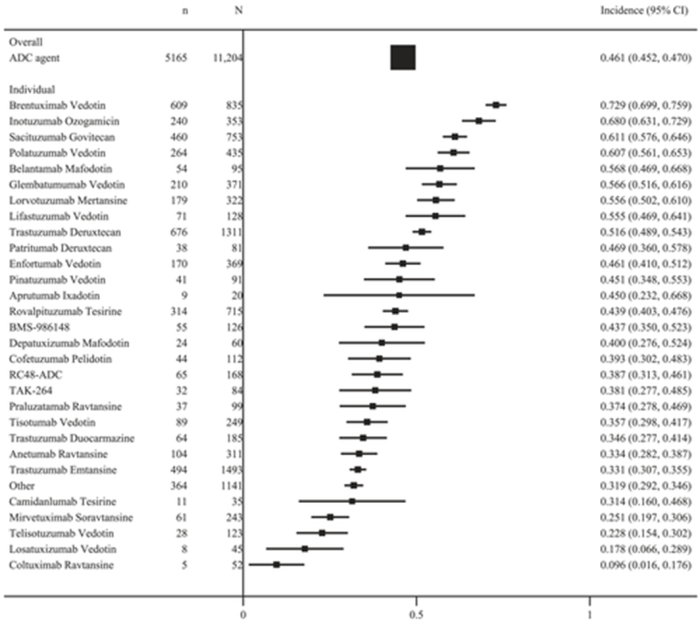 图注:ADC方案中≥3级治疗相关不良事件的总体发生率[1]
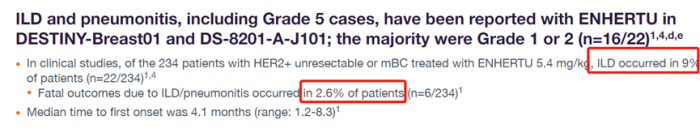
2)对于不同的ADC药物来说,其不良反应谱和发生率也有差异。DESTINY-Breast 01试验结果显示Enhertu的不良反应主要为deruxtecan相关的副作用,如恶心(79%)、白细胞计数减少(70%)、中性粒细胞计数减少(62%)、天冬氨酸转氨酶升高(41%)、血小板计数降低(37%)等,其中被黑框警告的间质性肺病发生率为9%,因间质性肺病导致的死亡发生率则达到了2.6%[5]。
图注:ADC方案中≥3级治疗相关不良事件的总体发生率[1]
2)对于不同的ADC药物来说,其不良反应谱和发生率也有差异。DESTINY-Breast 01试验结果显示Enhertu的不良反应主要为deruxtecan相关的副作用,如恶心(79%)、白细胞计数减少(70%)、中性粒细胞计数减少(62%)、天冬氨酸转氨酶升高(41%)、血小板计数降低(37%)等,其中被黑框警告的间质性肺病发生率为9%,因间质性肺病导致的死亡发生率则达到了2.6%[5]。

3)最近获批的
Mirvetuximab Soravtansine
则因眼毒性被添加黑框警告,其可能引起包括视觉障碍、角膜病变、干眼症和葡萄膜炎在内的严重眼部副作用。根据2022 ASCO大会上公布的安全性数据[7],Mirvetuximab Soravtansine最常见的不良反应包括视力模糊(63%)、疲劳(58%)、角膜病变(43%)和干眼症(35%)等。这和GSK开发的Belantamab mafodotin类似,其主要不良反应也为眼毒性,原因可能是二者的有效载荷易在角膜上皮细胞聚集。

图注:Mirvetuximab Soravtansine则因眼毒性被添加黑框警告[7]
ADC的毒素小分子和抗体部分均可影响正常细胞,从而导致不良反应。其不良反应可以分为在靶和脱靶毒性,在靶毒性是由ADC杀伤表达靶抗原的正常组织产生,脱靶毒性则是指ADC在不表达靶抗原的组织中产生的杀伤。根据临床观测,由毒素小分子引起的脱靶毒性是ADC不良反应的主要来源。
在靶毒性:
抗体部分介导的ADCC、CDC效应均可在表达靶抗原的正常细胞上发生,并导致不良反应,比如继发性的肾损伤。此外,抗体部分也可阻断正常细胞靶抗原的信号传导,比如HER2靶向的ADC可作用于表达HER2的肺上皮细胞、心肌细胞,通过抗体阻断HER2通路或是小分子毒素直接杀伤,引起肺损伤、肝毒性、LVEF降低等不良反应。
脱靶毒性:
毒素小分子在血液循环中的脱落、对正常细胞的旁杀效应以及正常细胞对ADC的内吞/摄取均可导致脱靶毒性,使正常细胞遭受毒素小分子损伤。首当其冲的便是血液循环中的淋巴细胞、粒细胞、血小板等,其次还包括容易蓄积亲脂性小分子的肝、药物排泄经过的肾,此外还包括对肺、神经、皮肤等组织的杀伤,从而引起临床上观察到的与化疗药物类似的不良反应。
肝毒性:
用药前和用药期间进行肝功能检查,并在发生肝功能异常时及时进行干预。
眼毒性:
可预防性使用无防腐剂人工泪液和类固醇滴眼液。1级副反应无需采取措施;2级则暂停给药,改善至1级/基线时再按原剂量恢复给药;为3级则暂停给药,恢复至1级/基线水平剂量降低后恢复给药;4级则停止用药。
血液学毒性:
应用ADC药物前进行全血细胞计数检查,在治疗期间定期监测血细胞计数,同时考虑预防性用药进行二级预防。
间质性肺病:
对于无症状(1级)ILD,考虑使用类固醇皮质激素治疗,可继续ADC治疗;2级ILD则暂停用药,口服或静脉给予糖皮质激素,直到缓解至0到1级;3级及以上考虑永久停药,部分患者考虑经验性给予抗生素,请呼吸专科医生会诊等;如果症状持续恶化,建议多学科会诊,并积极干预。
心脏毒性:
在应用DS-8201和T-DM1之前,对患者全面评估,以充分纠正心血管病等危险因素;如LVEF绝对值<50%(下降≥16%),或在正常范围但治疗过程中LVEF下降幅度≥10%,暂停ADC药物治疗,并给予血管紧张素转换酶抑制剂等药物,待LVEF恢复正常后再进行ADC治疗;如LVEF降低不可恢复或严重降低,或发生有症状的充血性心力衰竭,应永久停药。
ADC药物通过将毒素小分子与抗体连接,提高了小分子的靶向性,造福了诸多肿瘤患者。但由于有效载荷毒性明显提升、连接子循环不稳定等原因,目前的ADC药物尚未表现出较化疗小分子或单抗更佳的安全性。
因此,一方面,我们需在临床应用ADC时做好副反应监测和风险管理,及时应对出现的不良反应;另一方面,我们更需要从ADC分子本身着手,不断优化其抗体、连接子及毒素小分子,改善PK/PD性质,提高递送效率,从而实现弱毒性下的强药效。
[1] Zhu Y, Liu K, Wang K, Zhu H. Treatment-related adverse events of antibody-drug conjugates in clinical trials: A systematic review and meta-analysis. Cancer. 2022 Nov 21.
[2] Carrie Wynn, Ritesh Patel, Shou-Ching Tang et al. Increased systemic toxicities from antibody-drug conjugates (ADCs) with cleavable versus non-cleavable linkers: A meta-analysis of commercially available ADCs. Journal of Clinical Oncology. 2022 40:16_suppl, 3032-3032
[3] Ma, F, Xu, B. Expert consensus on the clinical application of antibody-drug conjugates in the treatment of malignant tumors (2021 edition). Cancer Innovation. 2022; 1: 3– 24.
[4] Lievano, F.A., Scarazzini, L.J., Tyczynski, J.E.et al. Risk Minimization of Antibody–Drug Conjugates in Oncology: A Review. Drug Saf 44, 733–742 (2021).
[5] https://www.enhertuhcp.com/en/breast/efficacy/destiny-breast-01
[6] Eaton JS, Miller PE, Mannis MJ et al. Ocular Adverse Events Associated with Antibody-Drug Conjugates in Human Clinical Trials. J Ocul Pharmacol Ther. 2015 Dec;31(10):589-604.
[7] https://www.immunogen.com
来源:BiG生物创新社





 图注:ADC方案中≥3级治疗相关不良事件的总体发生率[1]
图注:ADC方案中≥3级治疗相关不良事件的总体发生率[1]

















评论
加载更多