除菌级过滤器的选择和应用
我国国家药品监督管理局(NMPA)在2018年也专门针对除菌过滤技术起草了相关的应用指南,内容囊括了除菌过滤的设计、验证、操作等细节。本文将从筛选和应用等角度,为您详细介绍除菌过滤的相关知识。
除菌级过滤器筛选时需要考虑的要素
细菌截留水平
这是最关键的选择要点,每平方厘米的滤膜应至少可以截留107CFU挑战细菌(通常采用模式细菌Brevundimonas diminuta),且完整性测试数据需与细菌截留测试相关联。
载量和通量
单位面积滤膜对实际待过滤料液的处理量和流速,应尽量高。
非特异性吸附
药物活性成分在过滤工艺前后,回收率不得受到明显影响。
可提取物水平
过滤工艺中,应尽量降低过滤器中的成分进入到实际料液中。
化学兼容性
应考虑待过滤料液和过滤器的兼容性,尤其是对于过酸或者过碱的料液,比如层析工艺中可能用到的再生和清洗缓冲液。
灭菌方式
过滤器是否有推荐的灭菌方式,比如在线蒸汽灭菌、高压蒸汽灭菌、伽马辐照灭菌等,且灭菌方式应该经过验证。
除菌级过滤器的应用
缓冲液过滤(Buffer)
该步骤通常不定义为严格的除菌过滤工艺,目的仅仅是去除缓冲液中的不溶微粒,或者降低缓冲液中的微生物负荷。
在下面的案例中,研究员在实验室以600g/L蔗糖溶液作为样品,对乐纯生物单层0.2μm PES膜片进行了测试。实验采用14.5psi的恒定压力,共测试了110分钟,PES膜片的过滤载量和流速衰减如下图所示:
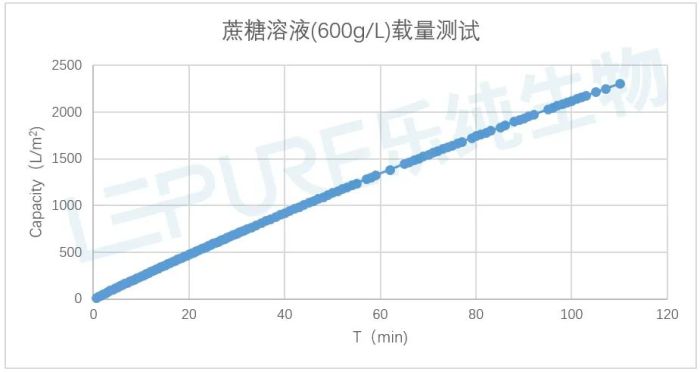
图1:蔗糖溶液过滤载量随时间的变化曲线
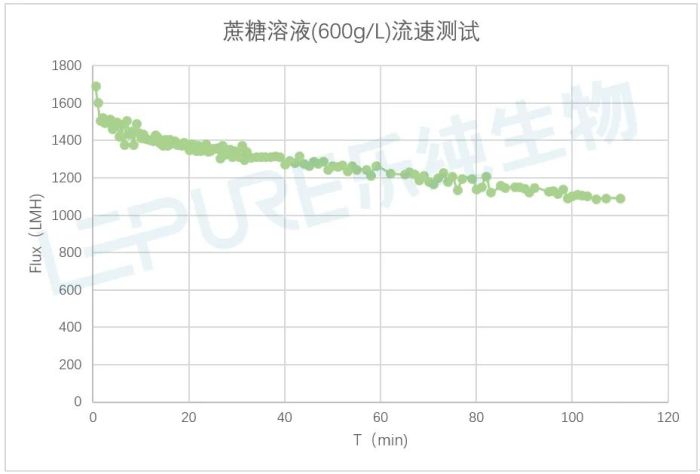
图2:蔗糖溶液过滤流速的衰减曲线
中间品过滤(Intermediate)
该步骤通常也不定义为严格的除菌过滤工艺,目的是去除中间品中的不溶微粒,保护层析柱和层析介质,或者降低中间品中的微生物负荷。
在一个案例中,研究员使用乐纯生物双层PES(0.45+0.2μm)膜片对捕获后的单抗料液中间品进行了测试,料液浓度约15-20g/L,测试前经过了长时间储存,并略显乳白色的胶束。测试在14.5psi的恒定压力下进行了8分钟,测试曲线如下所示:
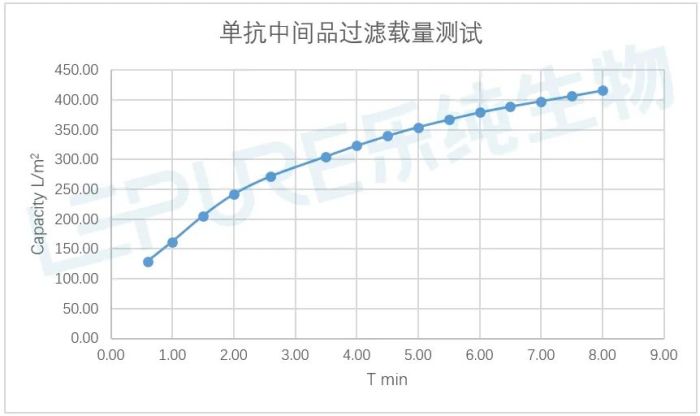
图3:单抗中间品过滤载量测试
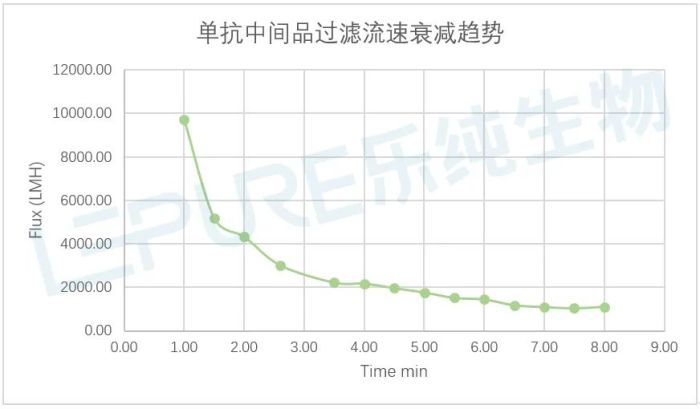
图4:单抗中间品过滤流速衰减测试
终端产品(Drug product)
严格的除菌过滤工艺,通常需要用实际料液以缩小模型的方式在相关验证实验室进行,并需要定义最差条件。
在一项测试中,研究员使用乐纯生物单层PES膜片,对大肠杆菌表达的某种重组蛋白酶进行了终端除菌过滤测试,料液浓度约0.2g/L,测试前恢复到室温,测试曲线如下所示:
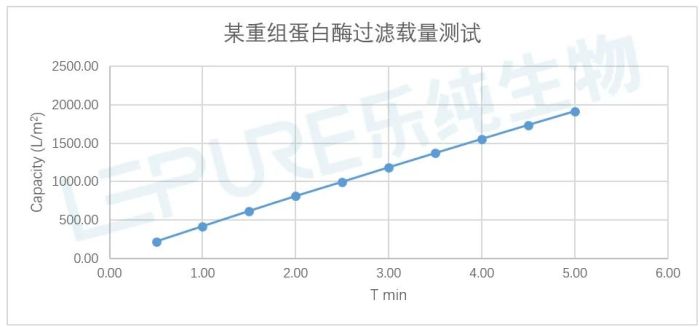
图5:某重组蛋白过滤载量测试
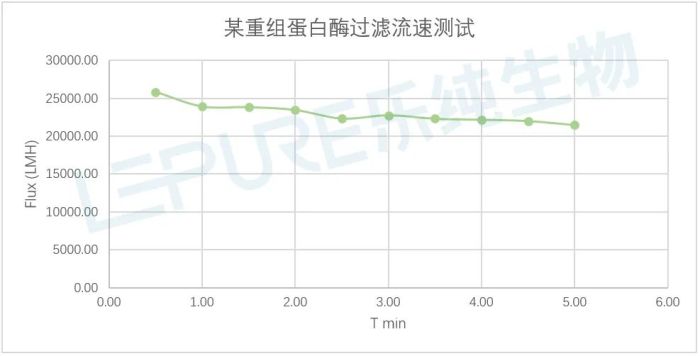
图6:某重组蛋白过滤流速衰减趋势

邵丽竹
何发
热点文章
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
微生物发酵技术在植物活性成分提取中的应用研究进展
2026-03-06
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多