制药人一定要了解的医药包装赋码与检测解决方案!

在过去的2021年中,仅北美就有多家著名的制药巨头(数据来源于www.fda.gov)批量召回其在外销售的产品,其中包括产品信息缺失,规格标识错误,用量标识错误,信息无法读取,数据无法追溯等等一系列问题。
但是怎样才能在不影响产线效率的情况下,确保产品赋码的正确性,减少意外损失的成本?有一个原则我们可以参考:一个问题发现的越早,其产生的影响就越小。同时,还有几个方面至少应该纳入考虑:
1. 产品包装本身的制式规格。仅生产一种和多种尺寸的包装产品可能会面临不一样的技术选择。有时,其间差别还会非常大,从赋码技术的角度来看,墨水赋码如果采用高解析那么喷印距离要求会很近,如果采用激光技术,由于打印面的变化是否还需要变焦功能,亦或是传输系统能够兼容各类规格的调节。
2. 产品包装需标识的信息内容。这和药品包装的设计息息相关,是否仅在包装上打印三期或是药品追溯码,一维的条码或是需要包含二维码的GS1 GTIN编码等等。这些信息的排版设计是怎样的,字符的大小安排,二维码的编码规则使用以及矩阵大小是如何考虑的(虽然信息相同但采用不同编码规则会影响二维码的尺寸大小)。赋码信息的合规要求是怎样的?是否出口国外并考虑各国不同的规则要求FDA、FMD、KNIH、SDC、DGFT、ANVISA、ITS?
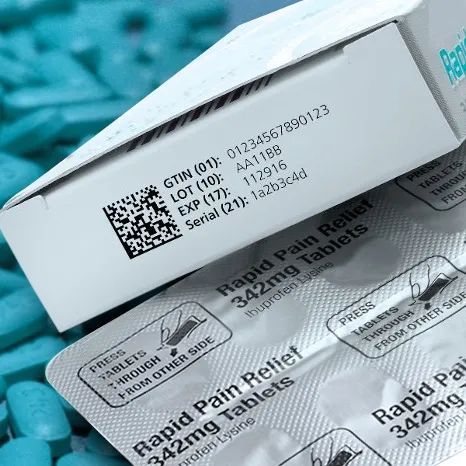
3. 产品包装的材质使用。即便是纸质外盒,覆膜与未覆膜也将会直接影响到赋码技术的效果。未覆膜的纸盒由于具有良好的渗透性,可以考虑以酒精或是水为基底的墨水喷印,而覆膜的纸盒就需要考虑快干类型的溶剂型基底墨水来操作。亦或是由激光灼烧的技术来应用,但是对于不同的材质在灼烧后产生对比度的效果,其影响可能很大。这对于后续的校验段将会增加识别的难度。并且不同赋码技术伴随着不同的打印速度,又关联着不同的赋码质量是否能够满足客户的需求都应考虑清楚。
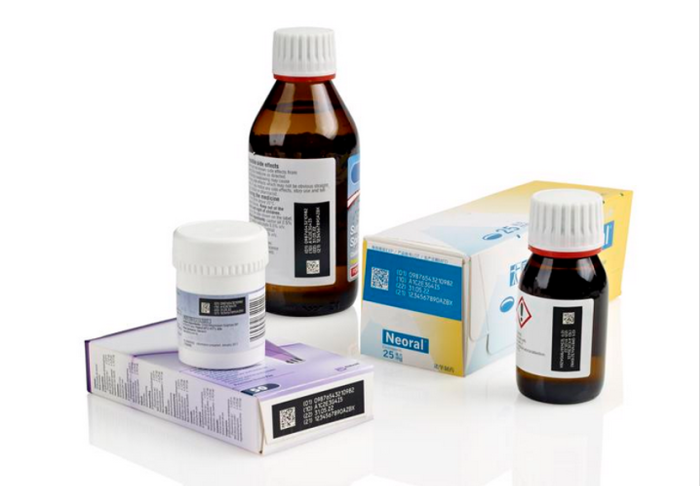
4. 视觉验证/检测的要求。潜在的故障和问题总是存在的,而对于出现问题后能够第一时间发现,是制药包装赋码检验的关键节点,越早发现的问题,其处理的复杂度甚至是损失将会极大的减少。那么,在医药产品包装赋码工艺之后,紧跟视觉检验的重要性不言而喻。但是问题来了,对于视觉检验,我们到底检验哪些情况?有无赋码?缺失部分赋码?条码/二维码是否能够被识读?这些只是最基本的。接下来,我们考虑二维码能够被识读,但是它的等级如何?如果并入后续工段或运输中可能磨损/衰减(墨水光照褪色速度)的情况考虑,光能够识读可能还不够,是否同时也需赋码等级检测的要求?还没完,是否考虑除了条码/二维码以外,所有字符的内容校验是否能够被读取?读取后和计划应当正确赋码的内容是否一致?这是我们想要达到的结果,但是技术层面的实现还需要考虑不同打码设备的特点,划线式的激光,高解析的热发泡,点阵式的连续喷墨,类印刷品质的热转印等等。他们会产生不同的图像特点和字符边缘类型,甚至是当出现赋码故障时呈现不同的“毛病”现象。这对于视觉校验工艺段的来说,涉及到不同情况时的识别图像学习过程,需要一定的人员技术经验和时间来完善。
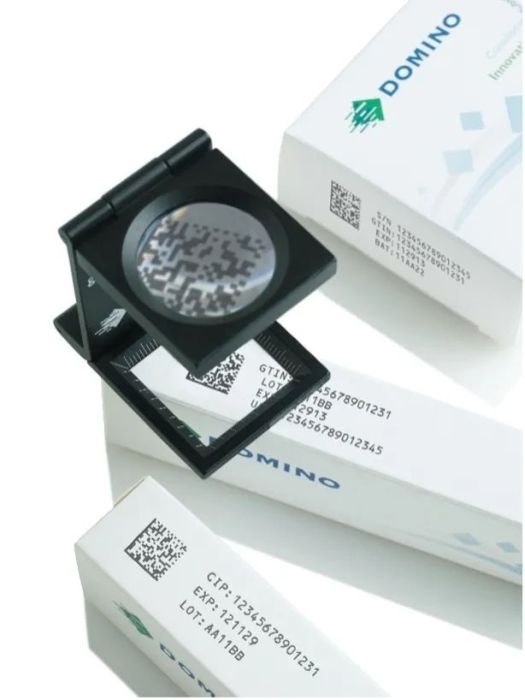
5. 数据关联的考虑。简单的解释来说,从赋码到视觉检测,数据的输入和输出关联到整个系统的考虑是怎样的。如果是一物一码的标识要求,是否当前包装层级的数据还需要做关联处理,从单品至中包到外箱堆托盘,这一系列的数据关联都需要考虑,并且从一开始的小包装赋码检测开始就要保证极高的正确性。
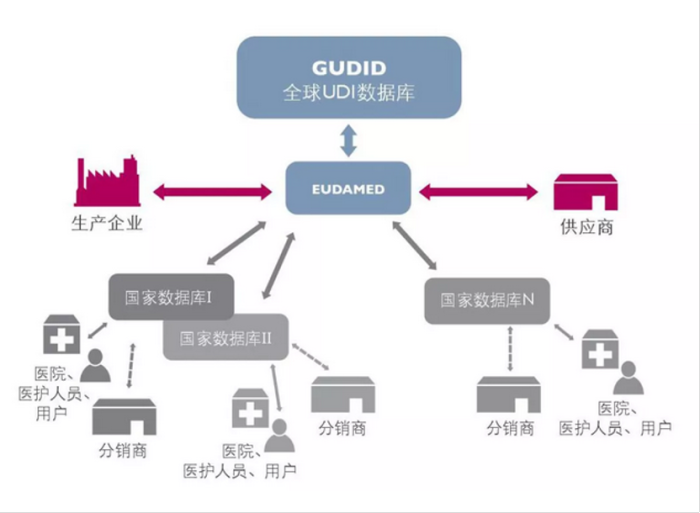
6. 不良品的操作流程。没有100%的OEE(全局综合生产效率),总会有各类问题导致损耗和不良品的出现。在包装赋码的环节,当出现此类情况时,我们能够及时发现之外,第一时间能够做出处理非常关键。如果后续还有更多层级的关联,一旦队列混乱那就麻烦了。现场的操作人员将一头雾水,拼命翻找不良品甚至不惜废掉一大段产品。准确的,快速的,正确对应的剔除应当纳入考虑,同时赋码不良品的数据反馈,视觉检测的图像存储或上载都应当完善。
7.合规认证。不同于其他产品,药品制造有着极其严格的合规性要求,从设备操作到数字签名,从赋码油墨的成分到GMP生产,每一项的纰漏都可能会影响药企产品的整体合规性。所使用的赋码检测功能,是否具备/满足21 CFR part11,ePedigree?所使用的标识墨水产品,是否也符合GMP生产标准?也需要仔细考虑。


多米诺医药包装赋码与检测解决方案充分考虑了以上7点内容,可以帮助企业确保产品赋码的正确性,大大降低产线成本。多米诺在医药产品可追溯性,GMP合规性和打击伪造药品等方面具有40多年解决方案的经验,一直秉承“Do More”的理念,用户可以完全信任其提供的整个赋码标识过程。可以说,他们是“标”与“识”的专家,能够为用户提供一站式解决方案,包括:

多米诺外盒赋码视觉检测一站式解决方案
多米诺打印视觉工作站(CV Station),用于盒式包装的序列化信息,包括各类条码、二维码、批号、产品标识号(GS1\GTIN)和有效期、图案logo等内容的打印,并同时包含视觉检验系统可满足MRC和ORC等功能及不良品剔除方案。
无需在耗费额外的精力协调各设备厂家集成,这是一套成熟且高效的外盒赋码解决方案。通过了解生产线预留工位的情况后,我们会定制匹配线体尺寸的打印视觉工作站,并无缝整合至您规划的线体工位。

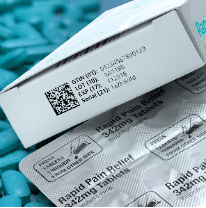
一维码、二维码、批号、有效期和产品标识号(如: GS1 GTIN)
符合ISO/IEC 15415条码等级检测
每分钟可达400盒生产速度
自动保存序列号及批号数据


根据您的产线情况制定适配的工艺参数
可达60米/分钟的产线速度
同步上下夹持输送带设计,稳定精确
渗透或非渗透包装材质均可兼容
高速气动剔除不良品


药品赋码内容检查
MRC和ORC识别检测
不良品检测图像保存或上载
在线条码等级检测(ABCDF)(可选)
21 CFR Part 11合规
文章来源:多米诺
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多