2021年新冠业务赢家排名出炉,辉瑞遥遥领先
随着企业财报的公布,2021年新冠业务(疫苗+治疗/预防药物)的赢家也浮出水面,详见下表。
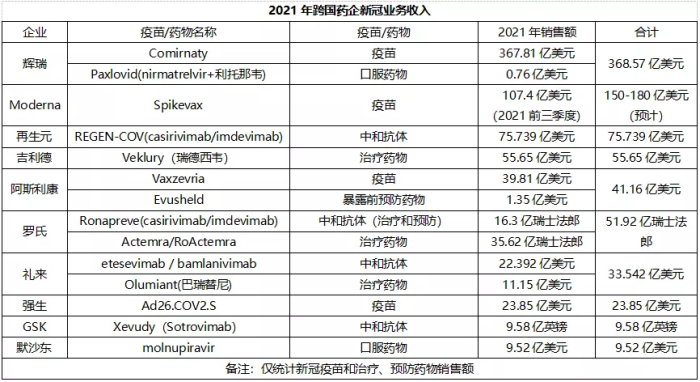


辉瑞同时拥有新冠疫苗和口服治疗药物,其新冠疫苗Comirnaty最早于2020年12月获FDA紧急使用授权用于16岁及以上人群预防新冠病毒感染,目前2针免疫程序已获FDA紧急使用授权被扩大用于5-11岁的儿童,而且其加强针也已获得紧急使用授权。此外,去年12月公布的初步实验数据显示,接种3剂Comirnaty疫苗能有效对抗Omicron变种病毒。口服新冠药物Paxlovid于2021年12月获FDA紧急使用授权,用于治疗直接SARS-CoV-2病毒检测呈阳性、体重至少40公斤、有高风险发展为严重COVID-19(包括住院或死亡)的轻度至中度COVID-19成人和儿科(≥12岁,体重≥40公斤)患者。而且,Paxlovid有望对抗奥密克戎变异株。
在公布2021年财报时,辉瑞预测2022年这两款产品有望带来540亿美元收入,其中Comirnaty 2022年营收预期约为320亿美元,Paxlovid 2022年营收的初步预期约为220亿美元。


Spikevax(mRNA-1273)是一款使用mRNA编码新冠病毒刺突蛋白的新冠疫苗,获FDA紧急使用授权用于18岁及以上人群预防新冠病毒感染,其加强针已获FDA紧急使用授权用于16岁以上人群。2022年1月被FDA批准用于预防18岁及以上人群感染新冠病毒。
目前,Spikevax 2021年前三季度销售额为107.4亿美元,全年销售额还未公布。Moderna公司预计有望其2021年销售额有望达到150-180亿美元。不过仅前三季度销售额就已妥妥决定Moderna公司的排位。


REGEN-COV是一款抗体鸡尾酒疗法,由再生元发明并与罗氏合作开发,罗氏主要负责美国以外地区的开发和供应。其有效成分casirivimab和imdevimab两种单抗分别针对新型冠状病毒(SARS-CoV-2)棘突蛋白(S蛋白)受体结合区域的2个独立的、不重叠的位点,具有协同作用,可降低病毒变异逃逸的风险,并保护人群免受S蛋白发生突变的病毒变体的侵害。2021年7月,REGEN-COV在日本获得全球首个监管批准(完全批准,商品名:Ronapreve),通过静脉输注,用于治疗轻中度COVID-19患者。
在美国,REGEN-COV于2020年11月获FDA紧急使用授权,用于治疗最近确诊为轻度至中度COVID-19的高危人群。2021年7月,该药又获FDA更新紧急使用授权,用于有高风险发展为严重COVID-19的人群进行暴露后预防性治疗。此外,该药用于治疗COVID-19非住院患者,以及用于某些个体预防COVID-19的BLA正在美国接受优先审评,PDUFA日期为2022年4月13日。此外,该药还将递交用于治疗COVID-19住院患者的BLA。
2021年,REGEN-COV销售额为75.739亿美元,而且在美国以外市场的销售额,即罗氏Ronapreve的销售额,达16.3亿瑞士法郎。


Veklury (remdesivir) 是吉利德研发的一种核苷酸类似物,2020年5月获FDA紧急使用授权用于治疗重症COVID-19住院患者,随后又获FDA紧急使用授权用于治疗中度COVID-19患者、12岁以下的住院儿科COVID-19患者(体重至少为3.5kg),以及有高风险发生疾病进展的12岁及以下非住院儿童患者。而且,Veklury还被FDA批准用于治疗12 岁以上(体重≥ 40 kg)需要住院的 COVID-19 成人和儿科患者。
不过,2021年Veklury市场表现并不亮眼,仅有55.65亿美元。而且2021年第四季度销售额已较2020年同期出现下滑(19.38 vs 13.57 亿美元)。


阿斯利康同样拥有2款新冠产品,其新冠疫苗Vaxzevria(前称AZD1222)由牛津大学及其剥离的公司Vaccitech共同发明,使用基于普通感冒病毒(腺病毒)的弱化版本的复制缺陷型黑猩猩病毒载体,该病毒在黑猩猩中引起感染,并包含SARS-CoV-2病毒刺突蛋白的遗传物质。接种后会产生表面刺突蛋白,激发免疫系统攻击SARS-CoV-2病毒。2021年1月,AZD1222获EC有条件上市许可,用于18岁及以上人群主动免疫,以预防由新型冠状病毒(SARS-CoV-2)引起的新型冠状病毒肺炎(COVID-19)。Evusheld是两种长效单克隆抗体tixagevimab和cilgavimab的组合,是美国唯一授权用于暴露前预防新冠肺炎的抗体疗法,也是唯一通过肌肉注射的新冠肺炎抗体,2021年12月获FDA紧急使用授权用于新冠肺炎暴露前预防。
2021年,Vaxzevria和Evusheld的销售额分别为39.81亿美元和1.35亿美元。


罗氏拥有两款新冠治疗药物,不过Actemra/RoActemra 35.62亿瑞士法郎的销售额并不完全来自COVID-9患者,该药还被批准用于治疗系统性硬化症相关间质性肺病(SSc-ILD)、类风湿性关节炎(RA)、多关节型幼年特发性关节炎(pJIA)、全身型幼年特发性关节炎(sJIA)、巨细胞动脉炎(GCA)、细胞因子释放综合征(CRS)、Castleman病等,其2019年、2020年销售额分别为23.11亿瑞士法郎、28.58亿瑞士法郎。另外一款新冠药物Ronapreve其实就是再生元的REGEN-COV,其2021年在美国以外市场的销售额为16.3亿瑞士法郎。


礼来也有2款新冠治疗药物,其中中和抗体etesevimab/bamlanivimab于2021年2月获FDA紧急使用授权用于治疗伴有进展为重度COVID-19和/或住院风险的12岁及以上轻中度COVID-19患者,2021年9月获得FDA紧急使用授权用于12岁及以上高风险人群的暴露后预防,2021年12月获得FDA紧急使用授权用于出生至12岁以下的轻中度COVID-19治疗及暴露后预防,成为全球首个且唯一获得EUA覆盖12岁以下人群的中和抗体疗法。Olumiant是一种每日口服一次的选择性、可逆性JAK1和JAK2抑制剂,2021年11月获FDA紧急使用授权,联合Veklury用于疑似或经实验室确认为新型冠状病毒肺炎、需要补氧/有创机械通气/体外膜肺氧合(ECMO)、年龄≥2岁的住院成人和儿科患者。不过该药还被批准用于治疗类风湿性关节炎、特应性皮炎。
2021年etesevimab/bamlanivima中和抗体疗法销售额达22.392亿美元。笔者预计未来礼来在新冠领域的市场占比将继续扩大,其与AbCellera合作开发的单抗Bebtelovimab对Omicron变种和其他已知的SARS-COV-2变种保持着全面和有效的中和活性,目前已获FDA紧急使用授权用于用于治疗轻度至中度新冠病毒肺炎成人患者和 12 岁及以上儿童患者。而且,Olumiant用于治疗新冠肺炎患者的是NDA也已被FDA受理。


Ad26.COV2.S单剂新冠疫苗是使用腺病毒26型(Ad26)载体表达新冠病毒的独特“刺突”蛋白,对Ad26的改造使其无法在人体内复制而致病,2021年3月获FDA紧急使用授权用于18岁及以上人群预防新冠病毒感染,且其加强针也已获得FDA紧急使用授权。2021年Ad26.COV2.S销售额达23.85亿美元。


Xevudy(Sotrovimab)是葛兰素史克(GSK)与Vir Biotechnology公司合作开发的一款中和抗体,具有双重作用,可同时阻断病毒进入健康细胞、清除受感染细胞,2021年5月获FDA紧急使用授权用于治疗有高风险的轻度至中度COVID-19成人和儿科患者(12岁及以上,体重至少40公斤),2021年12月被EC批准用于早期治疗COVID-19。
2021年Xevudy销售额达9.58亿英镑,GSK预计其2022年的销售额约为14亿英镑。


molnupiravir是默沙东与Ridgeback合作开发的一款高效核糖核苷类似物,2021年11月获英国药品和保健品管理局(MHRA)批准,用于治疗具有发展为中症和重症COVID-19风险的轻、中度COVID-19成人患者,成为全球首个获批上市的口服小分子新冠药物。2021年12月,该药获FDA紧急使用授权用于治疗 SARS-CoV-2 病毒直接检测结果呈阳性的成人轻中度冠状病毒病 (COVID-19),并且有发展为严重 COVID-19 的高风险,包括住院或死亡,以及 FDA 授权的 COVID-19 替代治疗方案无法获得或临床上不合适的人。
2021年Molnupiravir销售额为9.52亿美元,预计2022年将达到50-60亿美元。
其实,2021年礼来、罗氏新冠业务的排名并不确定。随着新冠病毒的变异,以及多款在研药物,2022年新冠业务的市场格局更充满不确定性。
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多