原料药领域反垄断指南发布 进一步明确市场竞争规则
 行业 · 政策动态
行业 · 政策动态
1.国家药监局发布《全国药品监管系统法治宣传教育第八个五年规划(2021—2025年)》。《规划》明确了指导思想、主要目标和工作原则,提出突出学习宣传习近平法治思想、突出宣传宪法、突出宣传民法典、深入宣传与推动高质量发展和社会治理现代化密切相关的法律法规、深入宣传药品监管法律法规、深入宣传党内法规6项重点内容,并确定12项主要任务。
2.国家药监局发布公告,决定成立医用高通量测序标准化技术归口单位,76名专家组成第一届医用高通量测序标准化技术归口单位专家组。
3.国家药监局对《药品经营和使用质量监督管理办法(征求意见稿)》公开征求意见。征求意见稿是在2019年9月发布的《药品经营监督管理办法(征求意见稿)》的基础上修改完善而形成,与2019年征求意见稿相比,本次征求意见稿更加强调各相关方责任落实,进一步细化药品使用环节质量管理要求。
4.国家药监局就《医疗器械质量管理体系年度自查报告编写指南(征求意见稿)》和《医疗器械委托生产质量协议编制指南(征求意见稿)》公开征求意见,征求意见截止时间均为2021年11月30日。
5.国家药监局发布第四十八批仿制药参比制剂目录,共新增57个参比制剂,另外6个为增加持证商、增加商品名、药品通用名称及英文名称更新等。
6.国家药监局发布公告,注销小儿酚氨咖敏颗粒、氨非咖片、复方氨基比林茶碱片、氨林酚咖胶囊、氨咖敏片、丁苯羟酸乳膏、小儿复方阿司匹林片、氨非咖敏片8个品种的药品注册证书,停止上述8个品种在我国的生产、销售、使用。
7.国家中医药管理局网站发布《关于规范医疗机构中药配方颗粒临床使用的通知》,《通知》明确要求省级中医药主管部门在配合省级药品监督管理部门制定中药配方颗粒管理细则时,要进一步细化中药配方颗粒临床合理规范使用措施,确保中药饮片的主体地位。
8.国家卫健委药政司就《国家基本药物目录管理办法(修订草案)》公开征求意见。此次《修订草案》是在2015年2月发布的《国家基本药物目录管理办法》的基础上修订完善形成的,共19条。此次《修订草案》在基药目录范围中新纳入了儿童用药,这也是儿童用药目录首次被单独提出。
9.国家药监局医疗器械技术审评中心发布通告,公布修订后的各类医疗器械注册申请电子申报目录文件夹结构。新版注册申请电子申报目录文件夹结构自2022年1月1日起施行。
产品研发 · 上市信息
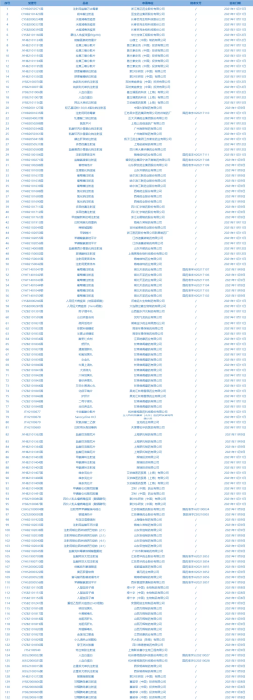
1.国家药监局发布3期药品批准证明文件待领信息,共包括132个受理号,涉及浙江海正药业股份有限公司等企业。(截至11月18日)
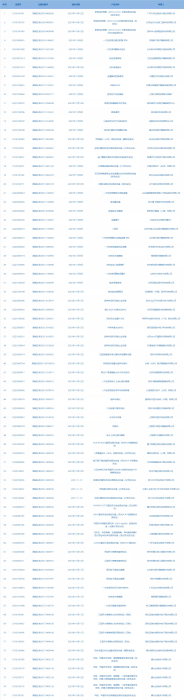
2.国家药监局发布4期医疗器械批准证明文件(准产)待领信息,共包括77个受理号,涉及广州万孚生物技术股份有限公司等企业。(截至11月18日)
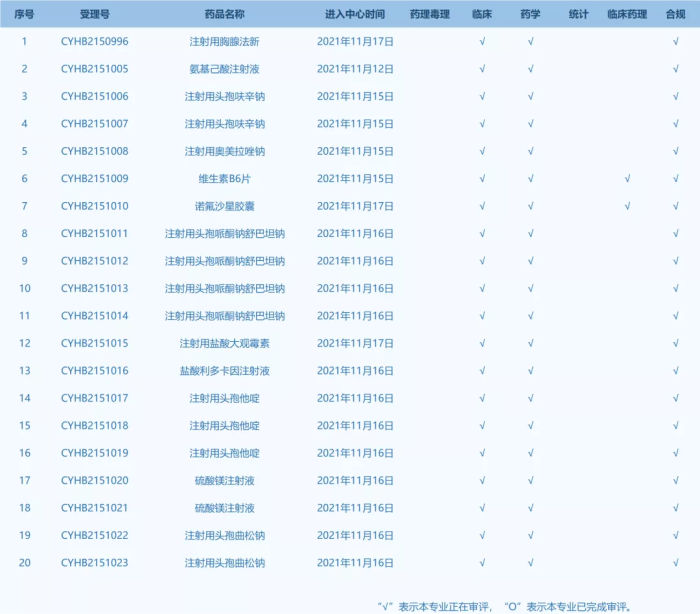
3.CDE网站公示20个仿制药一致性评价任务,涉及注射用胸腺法新等药品。(截至11月18日)
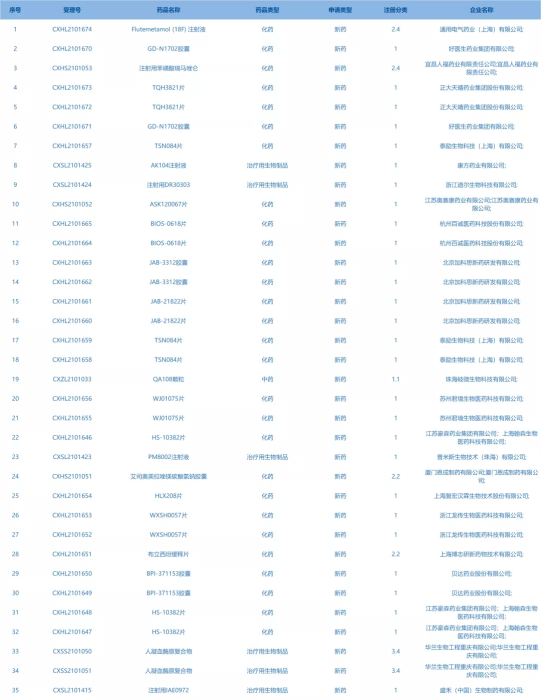
4.CDE承办受理35个新药上市申请,包括GD-N1702胶囊等药品。(截至11月18日)
医药企业观察
1.科济药业宣布,公司针对CLDN18.2的自体CAR-T候选产品CT041,已被欧洲药品管理局(EMA)授予优先药物(PRIME)资格,用于治疗胃癌/胃食管结合部癌。
2.君实生物宣布,由公司自主研发的抗PD-1单抗药物特瑞普利单抗用于治疗食管癌(EC)获得美国FDA授予孤儿药资格。这是特瑞普利单抗获得的第四个孤儿药资格,此前特瑞普利单抗治疗黏膜黑色素瘤、鼻咽癌及软组织肉瘤已分别获得FDA孤儿药资格。
3.澳宗生物宣布,美国FDA已授予其在研创新药TTYP01片孤儿药资格,用于治疗肌萎缩侧索硬化症(ALS)。
4.丽珠集团控股子公司丽珠单抗与美国Bright Peak Therapeutics签订研究合作和授权许可协议,丽珠单抗将具有自主知识产权的注射用重组人源化抗PD-1单克隆抗体(LZM009)有偿非独家许可给BPTx用于开发新型PD-1靶向免疫细胞因子(PD-1 ICs)。
5.因明生物与华润医药达成战略合作。根据合作协议,双方将积极推进因明生物新型肉毒素产品和眼科药物的商业化合作,探索因明生物产品管线的产业化合作,以及推进对因明生物的股权投资合作。
6.健民集团与汉康医药签订《技术开发合同》,委托其进行JMEY-WD15项目的技术开发,技术委托开发服务费用300万元;与杭州百诚医药签订《技术开发合同》,受让其自主研发的JMJT-DK16项目并委托其继续开发,技术委托开发服务费用750万元(含转让费)。
7.捷思英达宣布完成B轮融资。本轮融资由泰格医药、百度风投共同领投,前海贝增、久友资本跟投,老股东聚明创投和倚锋资本持续加码。
8.科镁联生物宣布完成1860万美元Pre-A轮融资。本轮融资由博远资本领投,联想之星、汇鼎投资及其他投资者参投。本轮募集资金将用于推进中美两国研发中心的建设,公司管线中主要品种的IND申报,以及加速公司的技术开发。
药械集中采购
1.山东省药品和医用耗材联合采购办公室就《关于国家组织药品集中带量采购协议期满山东省接续采购(202112)的公告(征求意见稿)》公开征求意见,明确将开展第一批国采25个品种以及第三批协议期满的22个品种续约工作。
2.广东省药品交易中心发布《关于开展广东联盟阿莫西林等45个药品集团带量采购价格申报品规申报工作的通知》,在之前公布13省45个品种联盟集采实施方案的基础上,公布了最为重要的三个附件:A、B、C采购单分组情况以及全国带量最低价。
3.湖南省公共资源交易中心发布《关于做好2021年抗菌药物专项集采中选结果执行前准备工作的通知》,将63个品规纳入“抗菌药物—续约药品”目录;41个品规纳入“抗菌药物—过渡期药品”目录;国家集采抗菌药物(湖南)中选供应品种30个药品纳入“抗菌药物—国采药品”目录。
4.陕西省公共资源交易中心发布《陕西省药品集中带量采购公告》,将对熊去氧胆酸等20个品种进行带量采购,同时公布了这20个品种的首年约定采购量计算基数及相应比例采购量。
来源/中国食品药品网
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多