中药粉末直接压片技术的前沿拓展:辅料改性及粒子设计与连续制造的整合
直接压片(DC)技术因其流程精简、能耗低等优势,已在化学药片剂连续化制造中成功应用。然而,中药粉末因其成分复杂、流动性差、可压性差及吸湿性强等特性,其 DC 面临显著挑战,严重制约了该技术及连续制造模式在中药领域的产业化推广。该研究聚焦于中药粉末的 DC 适用性这一问题,系统综述了通过单一辅料改性、功能性辅料共处理开发以及粒子设计(如多孔粒子、复合粒子构建)等具体策略,以改善其压片性能的最新研究进展。探讨其与连续制造流程整合的关键技术与适配性要求,以期为推动中药片剂高效、稳定的连续化直压技术开发与应用提供切实的理论依据和技术思路。
中药制剂作为中医药理论实践的物化载体,其生产模式的现代化转型始终是中药产业升级的核心命题。传统的间歇式生产方式存在生产效率低、质量稳定性差等诸多弊端,难以满足现代医药产业快速发展的需求。随着制药领域相关技术的不断发展,连续制造已成为未来发展的必然趋势。在这种背景下,中药粉末直接压片技术(DC-TCMP)作为一种创新的生产模式,受到了广泛关注。通过将中药粉末与功能性辅料配伍后不经制颗粒而直接压制成片,可以实现“一步成片”的集约化生产。
中药粉末包含单味或多味中药经粉碎的原生药粉末,经提取的提取物粉末,以及上述 2 种的混合粉末。不同于化药粉体可控的晶型与流变特性,中药物料多、物性复杂且浸膏占比大,导致其粉末的流动性和压实性普遍低于化学药粉体,易造成压片过程中片重差异过大、粘冲等现象,不能满足传统批次生产模式下对物料稳定性的要求。此外,相同的中药配方在不同的片剂制备工艺中对工艺的影响也不尽相同。
因此,迫切需要寻找新技术来克服中药粉末的压片困难,如优化辅料体系、创新粉末直压技术以及改进生产工艺,以实现 DC-TCMP 的高效和稳定生产。连续直接压片(CDC)是直接压片(DC)的连续化过程,其工序简单、生产效率高、能耗低,利于质量控制,但是其对物料的流动性和可压性要求高。DC-TCMP 技术的突破不仅能够改善粉末的压实特性,还能为中药片剂的连续化生产提供新的可能性,为中药片剂的现代化生产提供技术支持。
本文综述了辅料工程技术、粒子设计技术和在线过程分析技术,探讨其在中药制药连续化生产中的可行性,为实现中药粉末 CDC 提供思路。
Part.01
DC-TCMP 技术
1
DC 概述
压片机是实现 DC 的关键设备,通常使用单冲或多冲压片机进行操作。现代压片机配备先进的控制系统和压力调节机制,可以精确调控压片过程中的压力、速度和温度,从而确保每一片药物的均匀性和质量,见图 1。DC 工艺与原辅料性质密切相关,其中粒径、堆密度、表面吸附性、可压性和流动性等性质均对压片工艺产生重要影响。
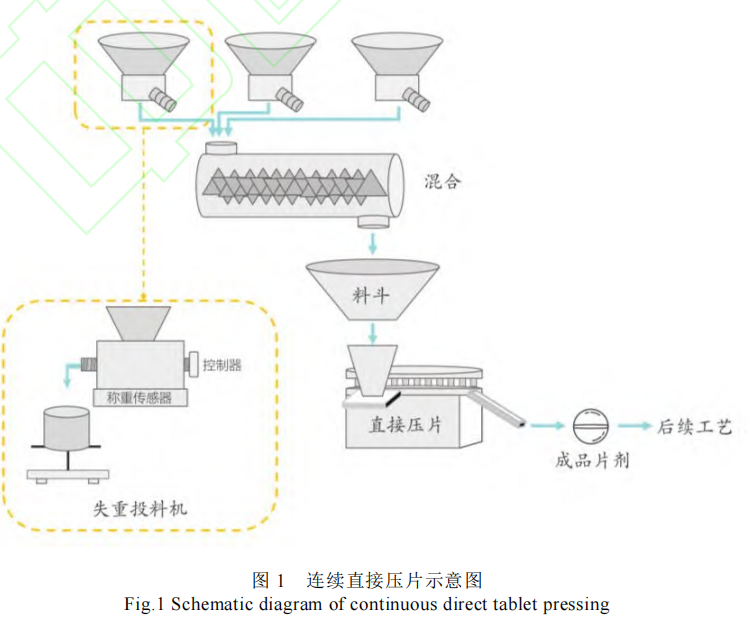
2
DC-TCMP 的难点与限制
当前,DC-TCMP 存在以下难点:①对物料粉体性质要求高:因未经历制粒过程,需物料具有良好的流动性、填充性和压缩成型性,否则在直压过程中可能会出现可压性差、硬度低、崩解不合格等现象[2];②中药复方粉末自身易分层:因其相容性问题易发生迁移分层,同时其强吸湿性导致粉末流动性急剧下降;③中药粉末与辅料易分层:二者的粒子大小及密度差异会在干混时产生静电,导致物料分层,出现质量差异和成分分布不均的情况[3]。此外,DC-TCMP 依赖高性能辅料,要求辅料除有良好的可压性和流动性外,还需有适宜的松密度和较大的药物容纳量[4]。因此,开发高性能辅料与寻找新技术以改善中药粉末直压特性已成为推进 DC-TCMP 产业化应用的关键突破口[5]。
Part.02
DC-TCMP 的创新与突破
1
辅料工程技术的创新
单一改性辅料的研究与应用
DC-TCMP 对辅料性能要求严苛,需具备高流动性、强压缩成型性、低吸湿性及高稀释潜力等特性[6]。传统辅料(如未改性淀粉、普通乳糖)因无法有效抑制中药粉末的高黏附性、难分散性纤维束及吸湿潮解,常导致压片粘冲、裂片或崩解延迟。单一改性辅料通过物理/化学手段(如喷雾干燥、基团修饰)针对性优化关键性能,成为解决中药直压难题的基础方案。其功能单一但使用灵活,可根据不同药物粉末特性进行定向选择。常用单一直压辅料有:喷雾干燥乳糖、预胶化淀粉、改性微晶纤维素、喷雾干燥钙盐、喷雾干燥的糖和多元醇等,见表 1。

其中,喷雾干燥乳糖作为 1956 年引入的首款直压辅料,具有粒径均匀、堆密度大、流动性与可压性优异、抗吸湿能力强等特点[11],能有效改善本身黏性较大的中药粉末的流动性与可压性。此外,它抗吸湿能力强,可应对吸湿性强的中药粉末[12]。其所制得的片剂硬度高、脆碎度低,但高温储存易显色变化。改性淀粉则是通过羧甲基化、交联等工艺提升崩解性与压缩性,如 Starch 1500®通过部分预胶化处理,凭借直链与支链淀粉的氢键作用优化内聚性,兼具自润滑特性与成本优势。对于流动性较差的中药粉末,改性淀粉能提升其崩解性和流动性,使片剂更易崩解和成型[13]。
微晶纤维素(MCC)是另一种广泛使用的喷雾干燥赋形剂。其通过喷雾干燥或颗粒化处理后具有极高的稀释潜力与干黏合性,可以通过塑性形变容纳更多中药成分而不易裂片[14]。余雅婷等[15]系统探讨了 MCC 对疏风解毒复方提取物直压性能的影响。发现随着 MCC 添加比例的增加,压缩比(CR)、屈服应力(Py)逐渐降低,单位有效功(Esp)逐渐升高,意味着 MCC 的加入有效提升了该复方粉的压缩与成型能力。此外,对于含挥发油类的特殊药材,通过活性组分预处理再联合其他常用直压辅料,有望实现油性成分片剂化。如 ARRAIS A 等[16]将百里香挥发油包合到 β-环糊精中并制备成片剂。
尽管单一改性辅料在特定性能优化上表现突出,但中药粉末成分复杂,单一辅料的功能单一性导致其综合性能受限,难以同时满足理化与机械性质的全面需求,共处理辅料在这方面具有更优异的表现。
共处理辅料的开发
共处理辅料通过塑性与脆性辅料在亚微米级的复合实现功能协同[17],其经特定的物理加工(如喷雾干燥、热熔、共结晶、冷冻干燥等)改性后,可赋予超越物理混合的优化性能[18],改变粉体自身的流动性、可压性和吸附性,从而提高片剂的硬度、脆碎度和崩解性能。
20 世纪 80 年代末,制药工业第一次引入了共处理的 MCC 和碳酸钙,标志着共处理辅料发展的开端。随后多种类型的共处理辅料相继上市,见表 2。例如基于淀粉的 DC 预混型辅料 StarLac®、Advantose FS®95、StarCap®1500 等[19]。共处理辅料相较于物理混合辅料具有显著优势:其一,多组分分布均匀,可避免加工过程中的成分离析;其二,通过颗粒团聚、球化及表面平滑等工艺改良,显著提升物料流动性;其三,不同组分间的协同作用能够赋予辅料多样化的功能特性[20]。

中药粉末因其物性问题,常出现流动性差、易吸潮结块、可压性差等缺陷,直接影响填充或压片工艺的稳定性。共处理辅料的均匀分布状态和协同作用,能够有效改善高纤维、高黏性中药粉末的流动性,减少吸湿结块现象。如乳糖基共处理辅料 Ludipress(由α-乳糖一水合物与聚维酮、交聚维酮共处理制成)兼具优良流动性、低吸湿性和高压缩性,已成功应用于 DC 和胶囊填充[21]。同时共处理辅料在提升中药制剂可压性崩解性能方面也具备应用潜力[22]。王松涛等[23]以栀子和垂盆草提取物为模型药物,通过喷雾干燥技术制备了乳糖-糊化淀粉、乳糖-不糊化淀粉 2 种共处理辅料,发现乳糖-糊化淀粉表现出更好的可压性和更大的载药量,有望成为新型中药直压辅料。WANG S 等[24]开发的乳糖-HPMC-PVPP 共处理辅料使雪莲提取物片剂抗张强度与普通物理混合辅料所制片剂相比提升200%;刘辉等[25]使用直压型共处理辅料 Parteck® ODT 制备了银杏叶提取物口崩片,崩解时间较物理混合缩短 25%,且可容纳 40%的银杏叶提取物。这些研究证实,共处理辅料经分子级复合改性,能优化中药粉末流动性、可压性与崩解性能,为中药制剂开发提供关键支撑。此外,除了已经上市的共处理辅料,仍有许多新型共处理辅料还在研发当中,见表 3。
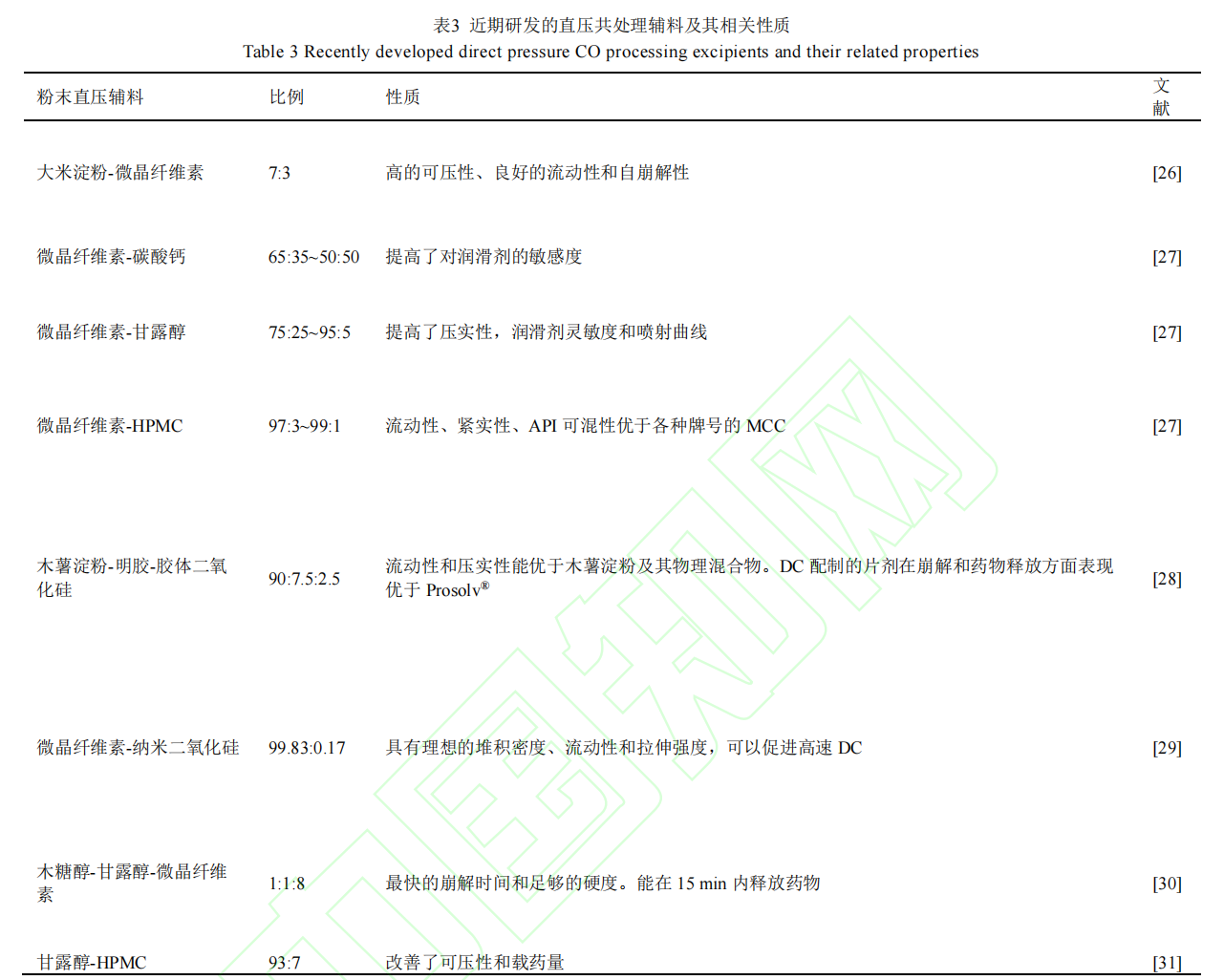
2
粒子设计技术的创新
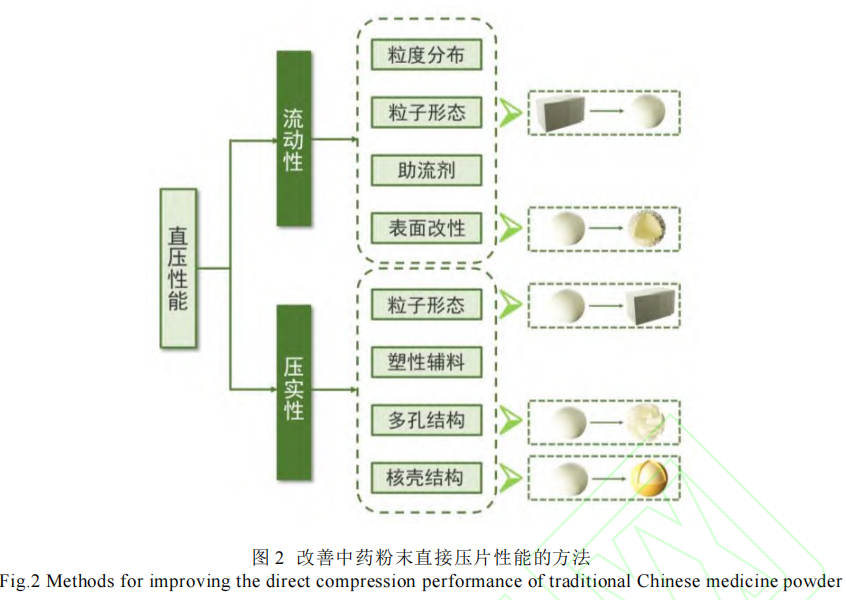
对于 DC-TCMP 而言,粒子设计技术不仅能够减少大量赋形剂的需要,而且还能通过调节粒子形态、结构和大小等颗粒的基本性质来显著提高颗粒的功能性质,满足多样化制剂需求,见图 2[37]。以下重点介绍核壳粒子、多孔粒子及多孔核壳粒子的设计与功能。
核壳粒子的设计与功能
核壳粒子是指由核心和外壳组成的复合结构颗粒,其表面性质多与外壳材料表面性质直接相关。通过壳层材料的选择可以满足成片需要的压缩力和强度,改善颗粒表面的流动性和崩解性,同时还能避免核心与环境中的水分或氧气接触[38]。由于中药粉末在流动性、可压性等直接影响直压工艺的关键物理性质上通常逊于常规的化学药物,因此,通过制备中药核壳型复合粒子改善中药粉末的直压特性是一次重要的尝试[39]。制备核壳复合粒子的常用共处理方法包括干磨、磁辅助冲击包衣、共喷雾干燥和流化床包衣,见图 3。干磨和磁辅助冲击涂覆主要集中在通过涂覆二氧化硅来改善材料的流动性[40]。陈志泽等[41]通过引入药用辅料硬脂酸镁与蒲公英、老龙皮饮片细粉进行超微粉碎制备“核-壳”复合粒子改善滋阴益胃胶囊内容物细粉粉体学性质,确定最佳硬脂酸镁用量为 2%,复合时间为3 min,复合胶囊内容物粉体学性质得到一定改善。
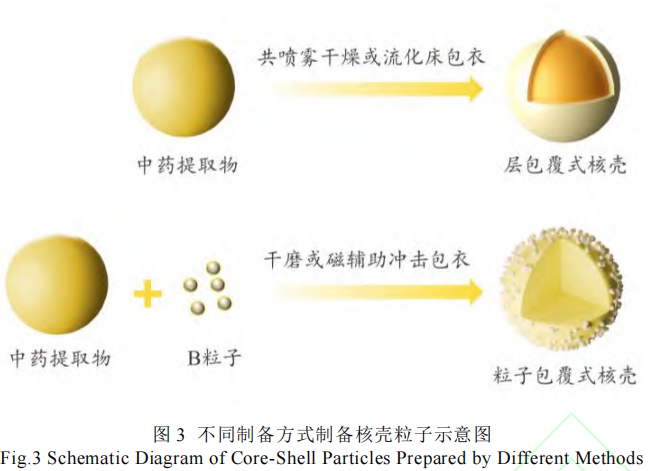
经二氧化硅涂覆的核壳粒子[42],可以提高粉体的流动性,同时降低复合粒子粉的吸湿性。陈丽华等[43]以疏水性气相纳米二氧化硅制备发酵虫草菌粉复合粒子,经振动式超微粉碎成功形成包覆结构,降低了发酵虫草菌粉与空气的接触面积,改善了吸湿性和流动性。ZHANG Y 等[44]通过湿共处理法采用纳米二氧化硅(NS)改性黄芪浸膏粉(ZR)的结构和表面性质,发现与微晶纤维素(MCC)相比,NS 可以更显著地改变 ZR 的纹理和表面特征。通过制备核壳粒子增强粉末压缩的有效粒子工程方法是用塑性变形材料(例如聚合物)对颗粒进行表面涂覆[45]。已经表明,用塑性变形材料包衣的颗粒表面可以使粉末的可压片性优于其他不可压缩的弹性粉末[46-47]。如用塑性聚合物羟丙基纤维素包衣对中药复合粒子进行表面改性[48]。LI Z 等[49]以干姜醇提物、葛根醇提物、茯苓醇提物、灵芝水提物、栀子水提物、陈皮粉碎物、穿心莲粉碎物、茯苓粉碎物为模型药物,制备了含羟丙甲纤维素的核壳复合颗粒和含聚乙烯吡咯烷酮的不同核壳复合颗粒并比较两者性能差异。结果发现,虽然两者性能不同,但都比原模型药物性能有较好的提升。
多孔粒子的设计与功能
多孔粒子是指具有大量微孔或纳米孔的特殊结构颗粒。凭借其独特的高比表面积与可控孔隙结构,为中药片剂提供了突破崩解迟缓、低塑性变形及溶出瓶颈的创新路径。相较于核壳结构,多孔结构通过物理容纳改善粉体的压缩特性,利用高孔隙率及高比表面积促进水分渗透与崩解,加速药物溶出。以金荞麦提取物为例[50-51],传统片剂面临溶出慢和可压性差的挑战,而将其与碳酸氢铵共喷雾干燥制成多孔粉体后,不仅溶出速率得到显著提升(较市售片剂提升 1~11 倍),其压缩性能也明显改善,更在与微晶纤维素或乳糖以适宜比例(如 75:25)配伍后,实现了片剂在 2~5 min 的快速完全崩解,这揭示了多孔粒子通过优化自身结构与协同传统辅料后可整体提升制剂性能。
常用的多孔粒子制备方法主要包括模板剂法、致孔剂法、利用自身基质成孔和化学合成法[52]。模板剂如蔗糖、柠檬酸、D-果糖等,致孔剂如碳酸氢铵、碳酸氢钠、樟脑、薄荷醇等,均可用于制备具有特定孔隙结构的多孔材料[53]。朱伟峰等[54]使用 PVP K30 作为模板剂制备了多孔乳糖,显著改善了姜黄素的溶出行为。李哲等[55]则通过对比表明,对于改善难溶性药物(如麦芽糊精)的溶出,模板剂法往往展现出更优的递送效果,这提示方法选择需基于药物特性与目标释放行为进行理性设计。除常规制备方式外,还可使用多孔材料(如多孔二氧化硅、多孔淀粉、多孔乳糖等)负载药物。针对中药中易挥发、氧化的挥发油成分稳定性差、包封率低的普遍难题,FANG Y 等[56]使用多孔材料(三维纳米网络多孔淀粉)高效吸附并固定丁香精油,将包封率提升至 86.7%且显著增强其热稳定性,从而实现了挥发油成分的固体粉末化,极大拓展了其在固体制剂中的应用前景[57]。
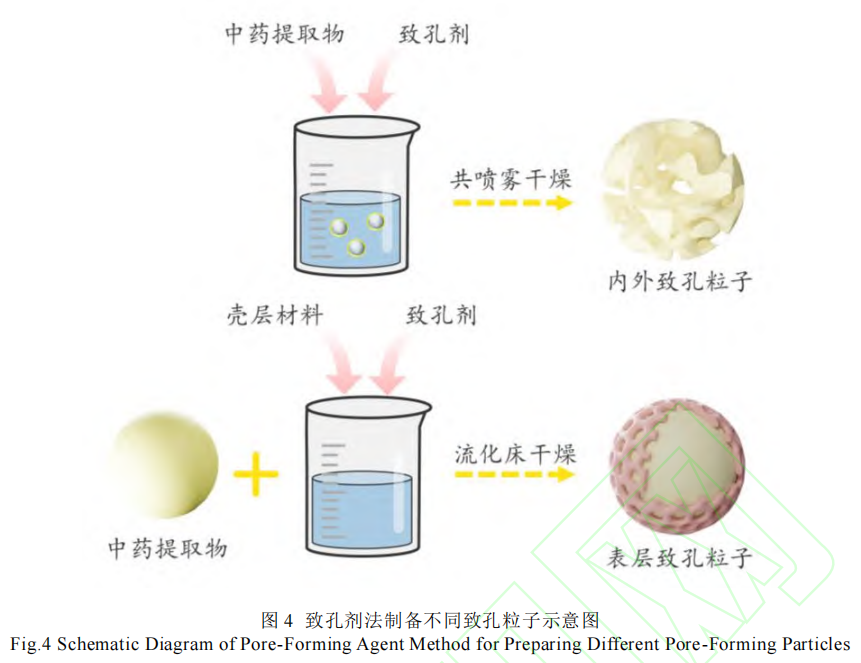
多孔粒子的形态分为全多孔颗粒和表面多孔颗粒,见图 4。全多孔颗粒因其内部和表面的孔洞,能显著改善药物的溶出和压片性能。而表面多孔颗粒则主要改善与表层相关的性质,如初期溶出速率和压缩成型性[58]。在中药粉末直压中,多孔粒子技术的应用需结合中药粉体的物性特点进行优化设计,以实现最佳的药物释放和成型效果。
多孔核壳粒子的创新与应用
虽然核壳粒子可以改善中药粉末的流动性和压实性,但它也具有延长片剂的崩解时限的缺点。而多孔结构恰好可以增加药物提取粉末的压实性,缩短片剂的崩解时限。多孔核壳粒子是粒子设计技术的创新成果,结合了核壳结构和多孔结构的优势,是 DC-TCMP 领域的前沿研究方向。
在中药粉末功能性包覆过程中引入改性剂和致孔剂。致孔剂受热分解后,会在粒子内部或表面形成孔洞,由此制备出的疏松多孔复合粒子,不仅能加快片剂崩解,其多孔结构还提供了更大压实空间,有效改善药物压缩成型性,可同时满足流动性、压缩性和崩解性的多重需求[59]。罗毓等[60]以共聚维酮和碳酸氢铵分别为改性剂和致孔剂制备不同比例的干姜醇提物改性复合粉体,相比于碳酸氢铵或共聚维酮单独制备的复合粒子,碳酸氢铵-共聚维酮共喷雾制备的复合粒子所压制片剂的抗张强度进一步提升,崩解时间缩短。LI Z 等[61]以聚乙烯吡咯烷酮(PVP K30)和羟丙基甲基纤维素(HPMC E3)为壳层材料,碳酸氢钠(NaHCO3)和碳酸氢铵(NH4HCO3)为致孔剂,采用共喷雾干燥制备了不同结构的改性颗粒改善了六味地黄粉的流动性和可压性。在制备过程中,由于常用壳材 HPMC E3和 PVP K30 的表面张力较小,干燥后,HPMC E3 和 PVP K30 迁移到改性粒子表面形成壳层。致孔剂在高温作用下分解产生气体,使内部气压升高。当压力达到极限时,将形成孔隙,从而形成多孔粒子或多孔核壳粒子结构。药物成分在致孔剂分解产生的气体压力下被挤压到壳层下形成芯层,见图 5。
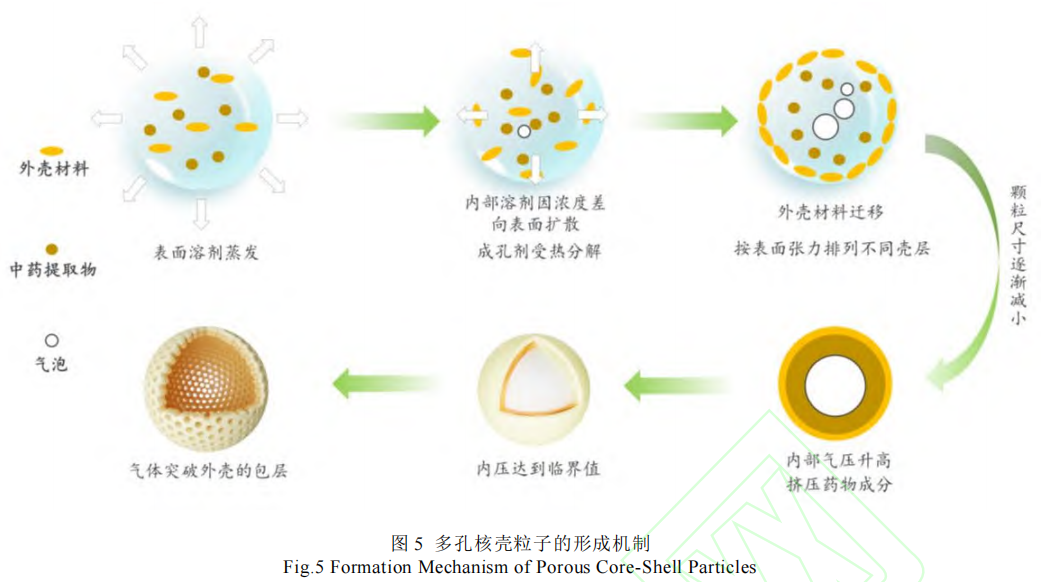
LI Z 等[62]制备了小儿喜食配方粉-多孔核壳复合粒子(XEXS-PCPS)并摸索了改性剂与致孔剂的最优比例,发现当 NH4HCO3和 PVP K30 的比例为 4.76%和 9.42%时与 4 种直压级辅料混合压片,粉体具有良好的直压特性和适用性。
中药多孔核壳粒子改善了中药粉末固有流动性差、可压性不足的特点,显著提升其对粉末直压工艺的适配性。该技术融合核壳结构的机械稳定性与多孔载体的功能调控优势,在核壳与多孔材料研究基础上实现创新突破,为中药固体制剂从传统湿法制粒向现代化压片工艺转型提供了新策略。
Part.03
DC-TCMP 与连续制造的结合
CDC 技术以工艺简洁、避免湿热损伤等优势,成为固体制剂工艺升级的重要方向。在化学药领域,基于“质量源于设计”(QbD)理念与过程分析技术(PAT),已建立起较为成熟的连续制造体系[63]。该体系在实时在线监控与模型化控制为核心的质量控制方面的成功实践,为中药连续制造提供了可参考的方法范式。
然而,中药物料具有组分复杂、黏性高、吸湿性强以及批间波动显著等特殊性,这给连续生产过程中的物料输送稳定性和混合均一性带来了挑战。因此,在中药领域推广 CDC 技术,不能简单沿用化学药的模式,而必须发展针对性的粉体改性技术以提升直压适用性,构建适应中药复杂体系的在线质量控制策略,并开发匹配中药物料特性的连续化专用设备,从而为建立稳健的中药连续制造体系奠定基础[64-66]。
1
中药 CDC 面临的挑战
CDC 工艺在化学药领域已凸显高效生产与质量可控的核心优势[67]。该技术基于“一进一出”的连续化设计原理,构建了从喂料、混合到压片的一体化流程,将传统批次生产的周期缩短为数十分钟内[68]。其集成生产线主要由配料站、连续混合单元、旋转压片机等核心设备构成,通过剪切与对流协同混合机制实现物料快速均质化,同时集成多冲头同步压实功能与实时质量检测模块,形成高效协同的生产链路[69-70]。在过程控制层面,CDC 工艺依托模型预测控制或人工智能算法动态调控工艺参数,构建起闭环质量控制体系,进一步保障生产稳定性与产品均一性。
尽管 CDC 工艺在制药行业的高效性、成本优势及质量提升潜力已得到广泛认可,但将其应用于成分复杂的中药粉末体系,仍面临独特的物料属性制约与工艺建模难题。不同于化药粉末成分单一,中药粉末(尤其全粉末)因含纤维、淀粉及油脂等多元组分,普遍存在堆密度不均、粒径分布宽、表面特性不均一等问题。这类物料的强内聚性与不良流动性,易在连续生产的失重喂料与连续混合环节诱发物料流动不稳定、含量均匀度波动等问题,成为限制 CDC 工艺稳定运行的核心瓶颈[71]。同时,中药粉末中的高黏性成分易导致粘冲问题,多糖类成分如红枣多糖则会显著影响压缩成型行为[72]。
此外,化学药粒子与辅料粒子通过相互粘连即可构建成型结构,而中药粒子需在外加机械力作用下发生塑性形变,进而与少量辅料粒子形成“内生桥”以实现成型[73]。在设备层面,我国目前的中药制剂设备整体缺乏创新,对中药工艺质量规律理解尚不充分,典型问题之一便是针对中药浸膏类物料的检测探头易出现污染问题,难以匹配中药复杂体系的连续化生产需求[74]。
为提升中药粉末对连续化生产的适配性,当前研究主要聚焦于两大技术路径:其一,通过物料前处理与粒子工程设计直接改善粉末性能,例如采用纳米二氧化硅共处理技术或设计多孔核壳复合粒子,能有效优化中药粉末的流动性与可压性,为 DC 提供物料基础[75];其二,鉴于中药体系的“黑箱”特性,利用离散元法(DEM)等先进数值模拟技术,对粉末在喂料、混合及压片过程中的微观行为进行仿真,已成为优化设备参数与工艺条件、降低开发风险的关键工具[76-77]。石辰风等[78]采用 DEM 对生甘草、独活、微晶纤维素和乙基纤维素 4 种粉末的休止角进行模拟,筛选出对休止角模拟测定影响显著的接触参数,建立了接触参数与模拟休止角之间的回归模型,证实了通过宏观物性参数间接标定中药颗粒体系 DEM 微观力学参数的可行性。
尽管中药体系的连续制造挑战显著,但已有研究提出了涵盖“操作、装备、工艺、质控”4 个连续性的中药连续制造成熟度评估模型[79-80]。未来可行的应用路径或采取分步策略:初期可在单方制剂等组分相对简单的体系上实施 CDC,随后通过深化工艺建模、开发专属在线监测工具,逐步向复杂复方制剂拓展,最终推动中药制药生产模式的智能化升级。
2
中药压片过程 PAT 应用探索
传统的控制策略大多依赖于成品测试的离线分析,而在线过程分析技术可以对生产过程进行在线分析和控制,依据生产过程中的周期性检测、CQAs 控制、原材料和中间产品的质量控制,大幅提高生产自动化水平,降低成本和减少人为错误,从而确保最终产品质量达到认可标准,见图 6[81-82]。常用于制药工艺的 PAT 工具有近红外光谱、拉曼光谱、高光谱成像、太赫兹脉冲成像、质谱法、声共振光谱、空间滤波测速法、聚焦光束反射测量、X 射线荧光、光学相干断层扫描等。
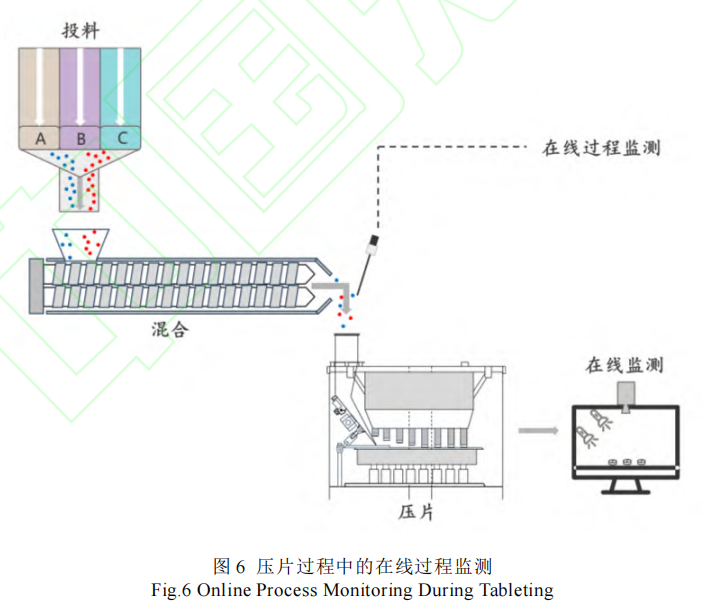
其中,傅里叶变换近红外光谱(FT-NIR)是制药生产中最为常用的分析技术[83],见表 4。张坤峰等[86]系统构建了中药浸膏粉及常用辅料的近红外光谱数据库,探索了 NIR 数据对原辅料物理性质及最终 DC 片剂性能的预测能力。刘秋安等[87]则通过 NIRS 技术结合对比分类和回归树算法,成功建立起一种快速无损检测天舒片崩解时间的新方法。
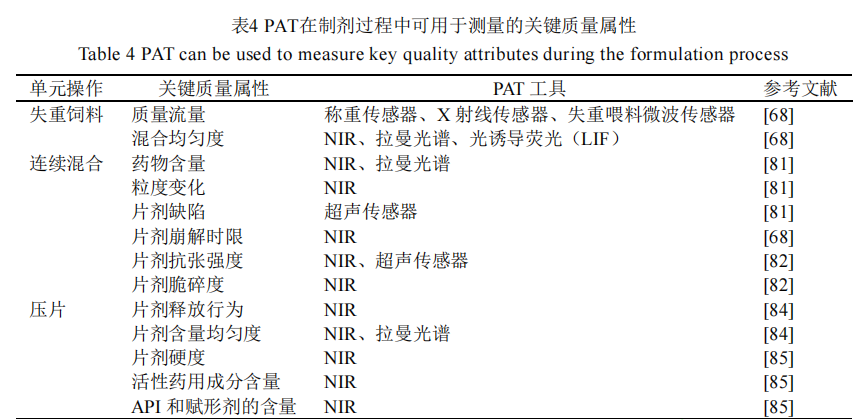
尽管 PAT 在中药生产的部分环节中已有初步尝试,但中药粉末固有的成分复杂性与物料波动性,却直接对主流光谱类 PAT 技术的应用构成了挑战[88]。中药多活性成分共存常导致近红外、拉曼等光谱吸收峰严重重叠,背景干扰极大,难以直接关联单一成分。同时,中药物性受原料产地、采收季节及前处理工艺波动的影响显著[89],这种“批间差异”会导致建立稳定、普适的定量模型极为困难。尽管挑战显著,通过针对性的策略,PAT 在中药体系中的应用具有可行性。张磊等[90]提出中药质量标志物(Q-marker),将药效物质与中药生物属性、组方配伍理论相融合,强化了中药有效性-物质基础-质量控制指标的关联,为复杂体系的质量控制提供了清晰、可检测的关键指标。此外,单纯依靠全谱分析往往效果不佳,采用高效的变量筛选与建模算法,是抗光谱干扰的关键。安思宇等[91]采用变量组合集群分析联合迭代保留信息变量-最小二乘法测定红参总皂苷,Rc 为 0.928,误差显著降低。证明了采用针对性的化学计量学策略,可有效从干扰严重的中药复杂光谱中提取关键信息。
2
研究与产业化进展
虽然用于制药片剂生产的几个单元操作本质上是连续的,但集成的从粉末到片剂连续生产线相对较新。GEA Pharma systems 首次引入了连续压片多功能平台(ConsiGma™),ConsiGma™系统专为插入式流程,先进先出生产(避免回混)而设计,提供一致的质量并允许对关键质量属性进行在线控制[92]。同时市场上有几种集成的连续压片生产线(例如 Glatt,Lödige,L.B.Bohle)。辉瑞公司和 GEA集团合作开发设计出了一种便携化、连续化、微型、模块化的连续制造平台,该平台集成了 6 种失重式进料器、一台立式混合器与一种旋转压片机,并在压片机饲粉器内配备了近红外系统,压片前可以实时监控含量均匀度并对片剂分流转移不合格的片剂,压片后,对片剂进行除尘,以批生产的方式包衣,离线检测终产品的溶出度、硬度、片重等性质,按需生产药物,Daurismo®和 Cibinqo®均采用这种平台进行制备[93-95]。
目前化学原料药 CDC 的工艺开发最为完善,已有多个采用该技术的产品成功上市。而近年来中药制剂领域也取得显著进展[96],部分中药生产工段及关键单元操作已实现了自动化生产。北京同仁堂已安装了一个全封闭的自动化中药粉碎、混合、计量分装系统,节约了人力和场地,提升了物料收率,使生产更加环保[92]。闫凯境等[97]提供的中药滴丸智能生产线,由输送管道连接的喂料装置、化料装置、均质装置、滴制装置以及脱油装置组成的连续性液体凝固装备集成,可实现连续性生产作业,能够保证滴丸产量的同时减小设备整机的占地面积。随着相关技术的进一步发展,中药制剂有望通过系统借鉴化学原料药连续化生产的成熟经验,突破传统生产模式的局限性,加速实现中药现代化战略目标。
Part.04
结语
DC-TCMP 技术是实现中药固体制剂高效、绿色生产的重要方向,本综述围绕该技术的产业化应用瓶颈展开系统分析与梳理。研究明确,中药粉末的多组分复杂性、差流动性、低可压性及批间不均一性,是阻碍 DC 工艺落地与连续化制造的核心挑战;针对这一核心问题,综述系统梳理并论证了三大关键改进策略:单一改性辅料应用、功能性共处理辅料开发以及中药活性成分的粒子设计。通过调控中药粉末的流动性、压缩成形性、混合均匀度及挥发油类成分稳定性,为 DC 工艺奠定合格的物料基础;而从辅料改性向中药活性成分自身粒子设计的重心转移,进一步为高载药量中药片剂的成型提供了创新思路。
需要强调的是,DC-TCMP 从间歇生产模式向连续制造模式的转型,是一项涉及物料属性、装备适配与质量控制的系统工程。该转型的核心前提是通过共处理、粒子设计等多种策略的协同应用,实现中药粉末直压适用性的综合提升;而其落地则需同步开发适配的连续化生产装备与在线质量监测技术,三者缺一不可。唯有构建“物料优化—装备适配—质控协同”的一体化技术体系,才能形成稳健可控的 DC-TCMP 工艺,推动中药固体制剂生产的现代化升级。未来研究可进一步聚焦于中药粉末的直压性能改善、多组分中药粉末的性质预测模型构建,以及连续制造过程的数字化质控体系开发,为该技术的产业化应用提供更坚实的理论与实践支撑。
参考文献
[1] 高岩. 粉末直接压片工艺在中药片剂生产中的应用[J]. 中国科技投资,2018(17):308.
[2] ZHANG Y, LI J, GAO Y, et al. Improvements on multiple direct compaction properties of three powders prepared from Puerariae L obatae Radix using surface and texture modification: Comparison of microcrystalline cellulose and two nano -silicas[J]. Int J Pharm, 2022, 622: 121837.
[3] 陈荣震,商明红,唐云. 浅谈直压工艺中的分层问题[J]. 山东化工,2022,51(5):161.
[4] 黄朝霞. 粉末直接压片工艺的进展[J]. 现代食品与药品杂志,2007,17(5):31.
[5] 李金枝,冯金瑞,何恬,等. 粉末直接压片技术及其辅料的应用与研究现状[J]. 中国新药杂志,2015,24(21):2467.
[6] 毕勇,李祥祥. 共处理辅料及其在制剂中的应用研究[J]. 安徽科技,2019(9):48.
[7] KORHONEN O, RAATIKAINEN P, HARJUNEN P, et al. Starch acetates-multifunctional direct compression excipients[J]. Pharm Res, 2000, 17(9): 1138.
[8] AL-ZOUBI N, GHARAIBEH S, ALJABERI A, et al. Spray drying for direct compression of pharmaceuticals[J]. Processes, 2021, 9(2): 267.
[9] LIN L, LIN X, SHEN L, et al. Mannitol in direct compression: Production, functionality, critical material attributes and co -processed excipients[J]. Int J Pharm, 2025: 125595.
[10] ZHAO H, ZHAO L, LIN X, et al. An update on microcrystalline cellulose in direct compression: Functionality, critical material attributes, and co-processed excipients[J]. Carbohydr Polym, 2022, 278: 118968.
[11] ATASSI F, ALMAYA A, ABURUB A. Effect of storage conditions on compaction behavior of two grades of spray-dried lactose[J]. Pharm Dev Technol, 2008, 13(4): 277.
[12] 刘佳佳,潘林梅,朱华旭,等. 基于多维检测和低场核磁共振技术探讨中药复方骨痹颗粒浸膏粉体吸湿性特征及其改性机制
[J]. 中草药,2018,49(11):2540.
[13] 任晓文,王维,丁一,等. 预混辅料直接压片的性质考察[J]. 现代药物与临床,2012,27(2):107.
[14] JIVRAJ M, MARTINI L G, THOMSON C M. An overview of the different excipients useful for the direct compression of tablets[J]. Pharm Sci Technol Today, 2000, 3(2): 58.
[15] 余雅婷,赵立杰,徐君杰,等. 微晶纤维素对疏风解毒配方提取物粉末直压性能影响的研究[J]. 中草药,2019,50(17):4041.
[16] ARRAIS A, BONA E, TODESCHINI V, et al. Thymus vulgaris essential oil in beta-cyclodextrin for solid-state pharmaceutical applications[J]. Pharmaceutics, 2023, 15(3): 914.
[17] 王淼,陈英,伍伟聪,等. 预混与共处理药用辅料的发展与质量管理现状[J]. 中国医药工业杂志,2022,53(4):578.
[18] BHATIA V, DHINGRA A, CHOPRA B, et al. Co-processed excipients: Recent advances and future perspective[J]. J Drug Deliv Sci and Technol, 2022, 71: 103316.
[19] SAHA S, SHAHIWALA A F. Multifunctional coprocessed excipients for improved tabletting performance[J]. Expert Opin Drug Del, 2009, 6(2): 197.
[20] LI J, ZHAO L, LIN X, et al. Co-spray Drying with HPMC as a Platform to Improve Direct Compaction Properties of Various Tablet Fillers[J]. AAPS PharmSciTech, 2017, 18(8): 3105.
[21] 林瑶. 热熔挤出技术在制备速释安宫牛黄片中的应用[D]. 咸阳:陕西中医药大学,2011.
[22] 缪妍,胡丽琴,张珂,等. 药用辅料在中药制剂中的应用研究进展[J]. 中国药科大学学报,2024,55(6):734.
[23] 王松涛,张静,林晓,等. 一种基于乳糖与糊化淀粉的新型共处理辅料研究[J]. 中国中药杂志,2014,39(22):4329.
[24] WANG S, LI J, LIN X, et al. Novel coprocessed excipients composed of lactose, HPMC, and PVPP for tableting and its application[J]. Int J Pharm, 2015, 486(1-2): 370.
[25] 刘辉,都胜男,邹萍,等. 口腔崩解片直压预混辅料 Parteck(R) ODT 的粉体学性能评价[J]. 中国药学杂志,2014,49(18):1625.
[26] LIMWONG V, SUTANTHAVIBUL N, KULVANICH P. Spherical composite particles of rice starch and microcrystalline cellulose: a new coprocessed excipient for direct compression[J]. AAPS PharmSciTech, 2004, 5: 40.
[27] 冉飞,张定堃,慈志敏,等. 高功能化复合辅料的研究现况[J]. 中国药学杂志,2020,55(10):794.
[28] APEJI Y E, OYI A R, ISAH A B, et al. Development and optimization of a starch-based co-processed excipient for direct compression using mixture design[J]. AAPS PharmSciTech, 2018, 19: 866.
[29] CHEN L, HE Z, KUNNATH K, et al. Fine grade engineered microcrystalline cellulose excipients for direct compaction: Assessing suitability of different dry coating processes[J]. Eur J Pharm Sci, 2020, 151: 105408.
[30] LOKE Y H, CHEW Y L, JANAKIRAMAN A K, et al. Development of a novel direct compressible co-processed excipient and its application for formulation of Mirtazapine orally disintegrating tablets[J]. Drug Dev Ind Pharm, 2024, 50(1): 36.
[31] 李金枝,阮洪生,林晓. 共处理辅料甘露醇-HPMC 生产工艺放大及在中药中的应用[J]. 中国中药杂志,2018,43(10):2067.
[32] 邹俊波,封亮,张小飞,等. 粒子设计技术在中药粉体领域的实践应用研究[J]. 中国中药杂志,2021,46(23):6011.
[33] 朱卫丰,陈富财,刘文君,等. 基于粒子设计原理的中药粉体改性研究进展[J]. 药学学报,2022,57(06):1781.
[34] 杨艳君,李婧琳,王媚,等. 粉体改性技术在中药制剂中的应用研究:以参苓白术散为例[J]. 中草药,2020,51(15):3884.
[35] 周晓,封亮,张小飞,等. 基于溶剂挥发法的羚珠散粒子设计技术应用研究[J]. 中国中药杂志,2021,46(23):6028.
[36] 郭立玮,付廷明,李玲娟. 面向中药复杂体系的吸入给药复合粒子优化设计原理与方法[J]. 中草药,2011,42(11):2165.
[37] LI Z, LIN X, SHEN L, et al. Composite particles based on particle engineering for direct compaction[J]. Int J Pharm, 2017, 519(1-2): 272.
[38] LI J, WU F, LIN X, et al. Novel application of hydroxypropyl methylcellulose to improving direct compaction properties of tablet fillers by co-spray drying[J]. RSC Advances, 2015, 5(85): 69289.
[39] LI Z, WU F, ZHAO L J, et al. Evaluation of fundamental and functional properties of natural plant product powders for direct compaction based on multivariate statistical analysis[J]. Adv Powder Technol, 2018, 29(11): 2881.
[40] 王小平,韩丽,任桂林,等. 基于机械粉碎法的穿心莲内酯复合粒子制备及其溶出度研究[J]. 中国中药杂志,2014,39(4):657.
[41] 陈志泽,杨荣平,史亚军,等. 粉体改性技术提升滋阴益胃胶囊内容物均一性的应用研究[J]. 中国中药杂志,2021,46(23):6053.
[42] 曾荣贵,蒋且英,廖正根,等. 表面包覆改性技术改善中药浸膏粉体流动性及吸湿性研究[J]. 中国中药杂志,2016,41(12):2245.
[43] 陈丽华,史畑女,吴瑶,等. 基于中药粒子设计技术改善发酵虫草菌粉吸湿性的研究[J]. 中国中药杂志,2019,44(8):1558.
[44] ZHANG Y, LI Y P, WU F, et al. Texture and surface feature-mediated striking improvements on multiple direct compaction properties of Zingiberis Rhizoma extracted powder by coprocessing with nano-silica[J]. Int J Pharm, 2021, 603: 120703.
[45] CHATTORAJ S, SUN C C. Crystal and particle engineering strategies for improving powder compression and flow properties to enable continuous tablet manufacturing by direct compression[J]. J Pharm Sci, 2018, 107(4): 968.
[46] OSEI-YEBOAH F, SUN C C. Tabletability modulation through surface engineering[J]. J Pharm Sci, 2015, 104(8): 2645.
[47] SHI L, SUN C C. Transforming powder mechanical properties by core/shell structure: compressible sand[J]. J Pharm Sci, 2010, 99(11): 4458.
[48] 李哲,张梦珊,周苗苗,等. 羟丙基甲基纤维素在中药粉体表面改性直压工艺中的应用[J]. 中成药,2021,43(10):2755.
[49] LI Z, WU F, HONG Y L, et al. The fundamental and functional property differences between HPMC and PVP co-processed herbal particles prepared by fluid bed coating[J]. AAPS PharmSciTech, 2020, 21: 1.
[50] 李金枝,罗毓,阮洪生,等. 金荞麦多孔粉体的压片性能改善及机制研究[J]. 中国中药杂志,2020,45(22):5518.
[51] 李金枝,罗毓,阮洪生,等. 金荞麦改性粉体直接压片的应用性研究[J]. 人参研究,2024(3):16.
[52] ZHOU M, SHEN L, LIN X, et al. Design and pharmaceutical applications of porous particles[J]. RSC advances, 2017, 7(63): 39490.
[53] LI Z, LUO X, LI Q, et al. The fabrication, drug loading, and release behavior of Porous Mannitol[J]. Molecules, 2024, 29(3): 715.
[54] ZHU W F, ZHU L, LI Z, et al. The novel use of PVP K30 as templating agent in production of porous lactose[J]. Pharmaceutics, 2021, 13(6): 814.
[55] 李哲,罗晓岁,朱卫丰,等. 模板剂法与致孔剂法对多孔麦芽糊精结构及药物递送影响研究[J]. 药学学报,2024,59(8):2381.
[56] FANG Y, FU J, LIU P, et al. Morphology and characteristics of 3D nanonetwork porous starch-based nanomaterial via a simple sacrifice template approach for clove essential oil encapsulation[J]. Ind Crop Prod, 2020, 143: 111939.
[57] 苏晓渝,李彪,陈水燕,等. 多孔材料吸附技术改善中药挥发油稳定性的研究与应用[J]. 药学学报,2022,57(11):3301.
[58] NGUYEN T T, SAIPUL B N S N, RAHMATIKA A M, et al. Rapid indomethacin release from porous pectin particles as a colon -targeted drug delivery system[J]. ACS Applied Bio Materials, 2023, 6(7): 2725.
[59] 罗毓,吴飞,沈岚,等. 流化包裹与致孔对中药提取物片剂制备性质的改善[J]. 药学学报,2020,55(11):2728.
[60] 罗毓,李金枝,阮洪生,等. 表面改性与致孔对干姜醇提物压片关键性能改善的研究[J]. 中草药,2023,54(10):3141.
[61] LI Z, PENG W, ZHU L, et al. Study on improving the performance of traditional medicine extracts with high drug loading based on co -spray drying technology[J]. AAPS PharmSciTech, 2023, 24(8): 247.
[62] LI Z, XIAO Y, ZHU L, et al. Optimization and application of porous core-shell particles for direct compaction[J]. J Chin Pharm Sci, 2024, 33(5): 412.
[63] IERAPETRITOU M, MUZZIO F, REKLAITIS G. Perspectives on the continuous manufacturing of powder ‐ based pharmaceutical processes[J]. AIChE J, 2016, 62(6): 1846.
[64] KAMYAR R, PLA D L, HUSAIN A, et al. Soft sensor for real-time estimation of tablet potency in continuous direct compression manufacturing operation[J]. Int J Pharm, 2021, 602: 120624.
[65] DAI S, XU B, ZHANG Z, et al. A compression behavior classification system of pharmaceutical powders for accelerating direct compression tablet formulation design[J]. Int J Pharm, 2019, 572: 118742.
[66] DAI S, XU B, SHI G, et al. SeDeM expert system for directly compressed tablet formulation: A review and new perspectives[J]. Powder Technol, 2019, 342: 517.
[67] HUANG Z, GALBRAITH S C, CHA B, et al. Effects of process parameters on tablet critical quality attributes in continuous direct compression: a case study of integrating data-driven statistical models and mechanistic compaction models[J]. Pharm Dev Tech nol, 2020, 25(10): 1204.
[68] VANHOORNE V, VERVAET C. Recent progress in continuous manufacturing of oral solid dosage forms[J]. Int J Pharm, 2020, 579: 119194.
[69] SINGH R, SAHAY A, KARRY K M, et al. Implementation of an advanced hybrid MPC-PID control system using PAT tools into a direct compaction continuous pharmaceutical tablet manufacturing pilot plant[J]. Int J Pharm, 2014, 473(1 -2): 38.
[70] JANSSEN P H M, FATHOLLAHI S, BEKAERT B, et al. Impact of material properties and process parameters on tablet quality in acontinuous direct compression line[J]. Powder Technol, 2023, 424: 118520.
[71] JONES-SALKEY O, CHU Z, INGRAM A, et al. Reviewing the impact of powder cohesion on continuous direct compression (CDC) performance[J]. Pharmaceutics, 2023, 15(6): 1587.
[72] 唐远萍,谢艾迪,赵怡,等. 红枣多糖的提取工艺优化及其压片糖果的制备[J]. 中国调味品,2025,50(1):127.
[73] 李哲,孙彩云,萧子健,等. “内生桥”驱动的高载药量中药粉末直压成型机制研究进展[J]. 中草药,2025,56(18):6493.
[74] 王子千,王学成,钟志坚,等. 中药口服固体制剂连续制造技术应用现状、趋势与挑战[J]. 中国中药杂志,2023,48(16):4536.
[75] 杨彤彤,赵水瑜,李金枝,等. 微粉硅胶的用量与加入方法对陈皮生粉的直压性能改善研究[J]. 中草药,2025,56(7):2319.
[76] 吴一峰,王子千,万鑫浩,等. 离散元法(DEM)在中药固体制剂制造过程中的应用[J]. 中国中药杂志,2024,49(12):3152.
[77] 崔荣才. 压片机与粉末直压工艺的优化适配探讨[J]. 流程工业,2025(8):68.
[78] 石辰风,杨茂蕊,唐正馨,等. 中药浸膏粉离散元模拟参数标定方法研究[J]. 中草药,2020,51(24):6205.
[79] 梁子辰,唐雪芳,杨平,等. 中药连续制造研究进展和成熟度评估[J]. 中国中药杂志,2023,48(12):3162.
[80] 牟娜,李香玉,黄哲. 中药应用连续制造技术的现状研究及对策建议[J]. 中成药,2024,46(9):3194.
[81] KIM E J, KIM J H, KIM M S, et al. Process analytical technology tools for monitoring pharmaceutical unit operations: a control strategy for continuous process verification[J]. Pharmaceutics, 2021, 13(6): 919.
[82] ZHONG L, GAO L, LI L, et al. Trends-process analytical technology in solid oral dosage manufacturing[J]. Eur J Pharm Bio Pharm, 2020, 153: 187.
[83] DE M A, UYTTERSPROT J S, CHAVEZ P F, et al. The application of near-infrared spatially resolved spectroscopy in scope of achieving continuous real-time quality monitoring and control of tablets with challenging dimensions[J]. Int J Pharm, 2023, 641: 123064.
[84] FONTEYNE M, VERCRUYSSE J, DE Leersnyder F, et al. Process analytical technology for continuous manufacturing of solid -dosage forms[J]. TrAC Trend Anal Chem, 2015, 67: 159.
[85] DULAR VOVKO A, VREČER F. Process analytical technology tools for process control of roller compaction in solid pharmaceuticals manufacturing[J]. Acta Pharm, 2020, 70(4): 443.
[86] 张坤峰,王政,曹君杰,等. 中药口服固体制剂原辅料近红外光谱数据库的构建及应用[J]. 分析测试学报,2021,40(1):1.
[87] 刘秋安,徐芳芳,张欣,等. 基于近红外光谱技术和分类与回归树算法建立天舒片崩解时间预测模型[J]. 中草药,2021,52(16):4837.
[88] 朱卫丰,沈玉,邓攀,等. 过程分析技术在中药制造工业中的应用[J]. 中国中药杂志,2024,49(9):2299.
[89] 王锦轩,姚霞,李耿. 基于化学特征的中药鉴定技术进展及趋势[J]. 中国中药杂志,2024,49(17):4617.
[90] 张磊,林梅,陈雪艳,等. 基于数据驱动的中药制药过程质量标志物(Q-Marker)监测方法研究及实践[J]. 中草药,2024,55(7):2452.
[91] 安思宇,张磊,尚献召,等. 红参提取物总皂苷近红外定量分析建模中的变量筛选[J]. 光谱学与光谱分析,2021,41(1):206.
[92] 王芬,徐冰,刘雨,等. 中药质量源于设计方法和应用:连续制造[J]. 世界中医药,2018,13(3):8.
[93] AM ENDE M T, AM ENDE D J. Chemical engineering in the pharmaceutical industry: drug product design, development, and modeling[M].State of New Jersey:John Wiley & Sons, 2019: 547.
[94] ALAM M A, LIU Y A, DOLPH S, et al. Benchtop NIR method development for continuous manufacturing scale to enable efficient PAT application for solid oral dosage form[J]. Int J Pharm, 2021, 601: 120581.
[95] 徐浩原,任曼华,何显洪,等. 原辅料粉体学性质对片剂连续制造的影响[J]. 中国粉体技术,2024,30(6):97.
[96] 王翔,王学成,朱雯婷,等. 新技术及装备在中药丸剂现代制造中的应用与展望[J]. 中国中药杂志,2024,49(19):5125.
[97] 闫凯境,孙小兵,荣昌盛,等. 一种连续性的液体凝固的智能滴丸机:CN201610807423. 3[P]. 2020-05-22.
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多