过氧化氢干雾灭菌器对洁净环境灭菌效果的验证研究
过氧化氢干雾灭菌技术是利用特殊的喷雾设备将过氧化氢消毒液雾化为粒径<10 μm 的小颗粒,这些小颗粒在空中可在短时间内将其水分迅速挥发为干颗粒,研究表明,过氧化氢的雾化粒子越小,在空气中悬浮的时间越长,就越有机会与空气中的细菌充分接触而达到灭菌的目的。
过氧化氢干雾的性质主要包括有: (1) 过氧化氢干雾在空气中进行无规则运动,遵循布朗运动原理并且不会沉降; (2) 过氧化氢干雾不会聚集在一起或者产生大的液滴; (3) 过氧化氢干雾在表面接触后会反弹,从而不会破裂而湿润表面[1]。过氧化氢干雾的这些性质让其具备良好的扩散效果和表面接触效果,非常适合应用于接触熏蒸式灭菌。过氧化氢干雾灭菌与其他气雾灭菌技术的比较见表1[2]。

表1 过氧化氢干雾灭菌与其他气雾灭菌技术的比较
过氧化氢灭菌器能够把过氧化氢液体形态变成纯正的干雾形态,以使其弥漫到整个待灭菌空间完成熏蒸灭菌的处理过程。过氧化氢干雾灭菌技术可以对洁净车间内空气及区域内设备物品的外表面灭菌,使灭菌空间的微生物负载得以有效消除。该技术目前被广泛用于制药、生物技术医学产品、化妆品以及保健品的生产。可安全用于不锈钢、塑料、玻璃、地板、墙壁等各种表面和空间消毒。过氧化氢干雾灭菌设备所用过氧化氢消毒液的浓度一般在5% ~ 10%,灭菌的成本较低; 干雾灭菌器系统使用少量的杀孢子剂就能完成高效的杀菌效果,由于用量少,具备较好的材料兼容性,对设备及其附件、墙壁、地面及辅助工具没有任何腐蚀性,是新一代的生态环保型灭菌技术[2]。本文对洁净区环境采用过氧化氢干雾灭菌器的灭菌效果及过氧化氢残留情况进行验证研究。
Part
1
材料与方法
1.1
验证用设备
欧菲姆OXY-30000 过氧化氢灭菌器,供应商法国欧菲姆。
1.2
验证用的试剂材料
过氧化氢杀孢子剂、嗜热脂肪芽孢生物指示剂(ATCC7953) 、化学指示剂、恒温培养箱、浮游菌采样器、胰酪大豆胨琼脂平皿培养基、德尔格过氧化氢浓度监测仪。
1.3
实验方法
过氧化氢灭菌器干雾灭菌效果的验证操作过程应制定详细的验证方案,大致的操作过程见文献[2]。
1.3.1 过氧化氢干雾分布均匀性确认方法
将欧菲姆OXY-30000 过氧化氢灭菌器放置在指定位置,并准备好适量的过氧化氢。灭菌前关闭洁净区空调系统新风进口阀门及排风阀门,洁净区内设备保持正常工作状态。
将化学指示剂分别放置在过氧化氢灭菌器所在房间的四周墙角(墙角放置分上下两层,下层离地10 cm,指示剂编号为1~4,上层离天花板10 cm,指示剂编号为5 ~ 8) 及设备关键位置(指示剂编号为9~ 32) 。
按照经计算的杀孢子剂用量调试好对应设备的用量,按下设备上的启动按钮,设备进行60 s 倒计时后,设备自行启动,开始喷雾,人员撤离出洁净区。
达到设定喷雾量时,设备自行停机,开始灭菌计时,灭菌保持120 min 后结束,然后开启净化空调系统并置换新风30 min,操作人员方可进入洁净区检查化学指示剂,观察指示剂变色情况。
1.3.2 灭菌效果确认方法[3]
过氧化氢干雾分布均匀性测试合格后再进行灭菌效果确认,将生物指示剂( 嗜热脂肪芽孢杆菌ATCC 7953) 分别放置在房间的四周墙角及设备关键位置。使用生物指示剂对灭菌房间及设备进行监测。
将欧菲姆OXY-30000 过氧化氢灭菌器放置在远离设备及墙壁的地方,喷嘴口离设备或墙壁的距离不少于3.0 m。
每个洁净房间内使用1 台过氧化氢灭菌器,按照经计算的过氧化氢杀孢子剂用量分别对四台欧菲姆OXY-30000 过氧化氢灭菌器进行用量设置,四台欧菲姆OXY-30000 过氧化氢灭菌器A1、A2、A3、A4 号设备用量依次设定为: 630,650,650,700 mL。洁净房间(过氧化氢灭菌器) 使用的生物指示剂编号依次为1-4、5-8、9-12、13-17。
关闭空调系统进排风。按设备上的启动按钮,开启欧菲姆OXY-30000 过氧化氢灭菌器,过氧化氢干雾通过喷头注入车间内。达到设定喷雾量时,设备自行停机,开始灭菌计时,灭菌保持120 min 后结束。
将经过氧化氢干雾灭菌后的生物指示剂全部放置于56 ℃培养箱内,恒温培养48 h,另取未经过氧化氢干雾灭菌的生物指示剂同时同步以同种方式接种培养,作为阳性对照。将对照管及灭菌后的生物指示剂进行对比观察。以确认过氧化氢干雾器在设定参数下的灭菌效果。
1.3.3 沉降菌监测方法
取胰酪大豆胨琼脂平皿培养基80个,根据洁净区沉降菌监测的取样计划,摆放在经过氧化氢干雾灭菌器灭菌后房间及设备表面,每个取样位点的沉降菌平皿暴露采样4 h,同时取3 个培养基作空白对照,采集完的培养基及空白对照培养基倒置于30~ 35 ℃培养箱中连续恒温培养5d,记录培养皿中菌落数,并与洁净区沉降菌的指标对比分析。
1.3.4 浮游菌监测方法
浮游菌监测的取样点为过氧化氢干雾灭菌器灭菌后房间,根据洁净区浮游菌监测的取样计划,使用胰酪大豆胨琼脂平皿培养基,放置在浮游菌采样器上,进行空气浮游菌的取样,各个取样点的取样量设为1000 L,同时取3 个培养基作空白对照,采集浮游菌样品的培养基及空白对照培养基倒置于30 ~ 35 ℃培养箱中连续恒温培养5 d,记录培养皿中菌落数,并与洁净区浮游菌的指标对比分析。
1.3.5 空气中过氧化氢残留监测方法
通过空调以及排风系统的全排风和过氧化氢自身分解成水和氧气,房间内部过氧化氢残留一般在30 min 内能降到职业健康允许暴露水平值(1×10-6) 以下( 依据“美国职业安全与人体健康”标准: 当环境中过氧化氢浓度小于1×10-6时,对人体健康是安全的)。
过氧化氢干雾灭菌结束,开启净化空调系统30 min 后,参照“过氧化氢干雾分布均匀性”的测试位点设计方案,用德尔格过氧化氢浓度监测仪对4 个洁净房间内的过氧化氢残留浓度进行测试。
Part
2
2.1
过氧化氢干雾分布均匀性确认结果
标准: 指示剂的过氧化氢反应区域应由紫色变成红色。待灭菌洁净区内过氧化氢干雾灭菌的过氧化氢化学指示剂的测试确认情况见表2。
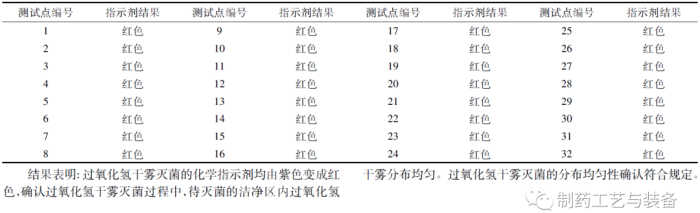
表2 待灭菌洁净区内过氧化氢灭菌化学指示剂的测试结果
2.2
灭菌效果确认结果
标准: 对照管应为阳性即变色( 呈黄色) ,灭菌后生物指示剂的菌管不变色( 呈紫色) 表示生物指示剂试验通过。
过氧化氢干雾灭菌效果的生物指示剂测试情况见表3。

结果表明: 经过56 ℃培养箱恒温培养48 h,对照管明显变色(呈黄色) ,结果判断为阳性,有微生物生长; 经灭菌处理的过氧化氢干雾灭菌效果测试用的17 支生物指示剂的菌管不变色(呈紫色) ,结果为阴性,判定为无微生物生长。由此确认设定参数条件下,欧菲姆OXY-30000 过氧化氢灭菌器在洁净区使用的灭菌效果合格。
2.3
沉降菌监测结果
根据洁净区沉降菌监测的取样计划,过氧化氢干雾灭菌的沉降菌培养结果为各采样点的沉降菌菌落数及空白对照均为Ocfu/皿,表明欧菲姆OXY-30000 过氧化氢灭菌器灭菌后的洁净区环境达到A 级洁净度下沉降菌标准规定,符合洁净区沉降菌限度的要求。
2.4
浮游菌监测结果
根据洁净区浮游菌监测的取样计划,过氧化氢干雾灭菌的浮游菌培养结果显示各采样点的浮游菌菌落数及空白对照均为Ocfu/皿,表明欧菲姆OXY-30000 过氧化氢灭菌器灭菌后的洁净区环境达到A 级洁净度下浮游菌标准规定,符合洁净区浮游菌限度的要求。
2.5
过氧化氢残留浓度量监测结果
标准: B+A 洁净区内空气中的过氧化氢残留浓度量: ≤1 mg /L。经过净化处理后,欧菲姆OXY-30000 过氧化氢灭菌器灭菌后空气中过氧化氢残留量监测情况见表4。
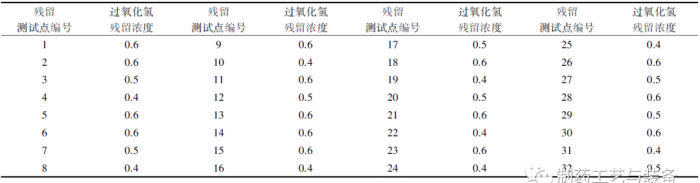
表4 过氧化氢灭菌器灭菌后空气中过氧化氢残留量监测结果( 单位: ×10-6 )
结果表明: 过氧化氢干雾灭菌结束经30 min 排风后,用德尔格过氧化氢浓度监测仪对洁净车间进行过氧化氢残留测试,测试结果表明,洁净区空气中的过氧化氢残留浓度量均≤1×10-6-6,过氧化氢残留测试符合标准规定,不会对人体造成危害。
Part
3
本文通过使用化学指示剂对过氧化氢干雾均匀性进行监测,确认了如下结果: (1) 欧菲姆OXY-30000 过氧化氢灭菌器干雾灭菌,洁净房间内的过氧化氢分布均匀; (2) 通过使用生物指示剂对欧菲姆OXY-30000 过氧化氢灭菌器干雾灭菌效果进行监测,确认了过氧化氢干雾达到有效的灭菌效果; (3) 通过对过氧化氢干雾灭菌的房间及房间设备进行沉降菌监测、浮游菌监测,确认了使用欧菲姆OXY-30000 过氧化氢灭菌器干雾灭菌后的洁净区域及设备微生物水平能达到A 级洁净级别要求;(4) 通过使用过氧化氢残留浓度监测仪对车间进行过氧化氢残留测试,过氧化氢残留浓度量均≤1×10-6,符合标准规定,表明过氧化氢残留不会对人体造成危害。洁净区域经过过氧化氢熏蒸消毒灭菌后,洁净区域环境的微生物被杀灭,过氧化氢残留对洁净区环境无影响,干雾灭菌器的灭菌效果达到预期要求。
干雾灭菌器是一种将液体消毒液雾化然后进行消毒的设备。设备利用超声雾化器产生电子高频振荡(振荡频率为1.7 MHz或2.4 MHz。超过人听觉范围,对人体及动物无伤害)以及通过陶瓷雾化片产生的高频谐振,来实现将液态水分子结构打散而产生自然飘逸的水雾,在雾化过程中将释放大量的负离子,其与空气中漂浮的烟雾、粉尘等产生静电式反应,使其沉淀。该干雾产生的过程不需加热或使用化学试剂。与加热雾化方式比较,能源节省了90%。还能有效去除甲醛、一氧化碳、细菌等有害物质,使空气得到净化,减少疾病的发生。通过本文的验证测试,确认了药品生产洁净区内使用过氧化氢灭菌器干雾灭菌的有效性和安全性。在指定区域的药品生产过程中,可以将过氧化氢干雾灭菌技术投入生产使用以便更有效地控制洁净区的微生物限度,保障药品生产的微生物控制能力和无菌保障水平。
参考文献
[1] 周志图.过氧化氢干雾灭菌器: 201921357859.2[P].2020-08-14.
[2] 宋大海.过氧化氢( 干雾) 灭菌及其在药厂的应用[J].机电信息,2015( 20) : 44-49.
[3] 中华人民共和国国家卫生和计划生育委员会.过氧化氢气体灭菌生物指示物检验方法: GB/T 33417—2016[S].北京: 中国标准出版社,2017.
撰稿人 | 张黄梅、刘兴、王正会
责任编辑 | 胡静
审核人 | 何发
邵丽竹
何发
热点文章
-
几种典型制药工艺流程图分析
2025-10-11
-
阿司匹林合成工艺及装置改进
2025-10-21
-
辐照辐照灭菌技术在制药行业中的应用灭菌技术在制药行业中的应用
2025-10-11
-
中药颗粒剂生产中的现代化工艺改造
2025-11-04
-
《药包材GMP(2025)》与药品GMP深度对比:核心差异、新增要点与实施指引
2025-11-25
-
2025年50家头部药企的竞争格局与核心趋势分析
2025-10-21
-
一文看懂新药研发到上市的全流程
2025-11-25
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多