如何正确进行仪器性能的确认?
制药生产关系到人们的生命健康,其数据的真实准确至关重要。分析仪器是进行药品质量检验工作的必要设备,《药品生产质量管理规范(2010年修订)》第一百四十条明确提出,应当建立确认与验证的文件和记录,并能以文件和记录证明达到以下预定的目标:
(一)设计确认应当证明厂房、设施、设备的设计符合预定用途和本规范要求;
(二)安装确认应当证明厂房、设施、设备的建造和安装符合设计标准;
(三)运行确认应当证明厂房、设施、设备的运行符合设计标准;
(四)确认应当证明厂房、设施、设备在正常操作方法和工艺条件下能够持续符合标准;
(五)工艺验证应当证明一个生产工艺按照规定的工艺参数能够持续生产出符合预定用途和注册要求的产品。
分析仪器属于检验设备,属于上述(四)的范畴,而PQ(Performance Qualification)的含义即性能确认。性能确认不仅在《药品生产质量管理规范》中有明确规定,在美国药典USP<1225>分析方法验证、ICH分析方法验证的通则里也有相关要求。
分析仪器的性能确认包括哪些项目?这些项目的具体含义分别是什么?本文以药企常用的分析仪器“总有机碳分析仪”(TOC分析仪)为例,对性能验证作出科学诠释,旨在减少仪器故障的发生率,避免不合格情况的出现,将风险降到最低(图1)。
图1 使用实验室TOC 分析仪进行制药用水分析
检验方法验证
检验方法验证(即检验仪器的确认)是根据检测项目的要求,预先设置一定的验证内容,并通过设计合理的实验来验证所采用的分析方法是否符合检测项目的要求。检验方法验证的基本内容包括方案的起草、审批以及检验仪器的确认。其中,方案的起草与审批,企业需根据自身情况进行撰写。至于检验仪器的确认,则包括多个检测项目。
验证参数释义
《药品生产质量管理规范(2010年修订)》中明确指出,检验方法验证的检测项目包括精密度、定量限/检测限、准确度、线性/范围、专属性、样品溶液稳定性以及系统适应性。以下是这些验证参数的具体含义。
精密度
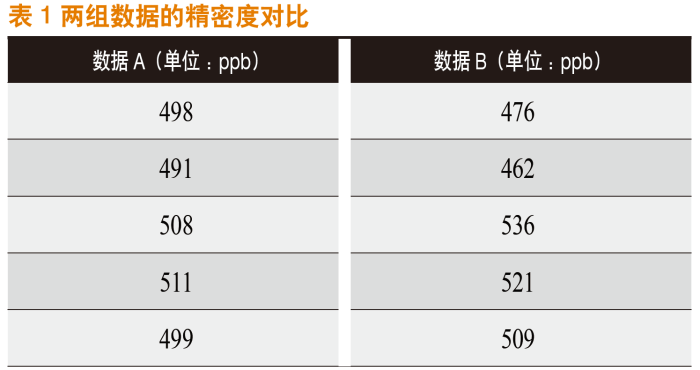
精密度指在一定的受控条件下重复测定均一样品所得测定值的一致程度,它反映了测量系统存在的随机误差大小。比如,用不同品牌的总有机碳分析仪对同一个水样进行测定,仪器的精密度越高,测量数据就越集中,倘若测量数据均集中在真值附近,则测量结果就越理想。举例而言,同样配置500 ppb(1 ppm=1 mg C/l,1 ppb=1μg C/l)的标准蔗糖溶液,表1的两组数据中,数据A的精密度较好。
准确度
准确度指在一定实验条件下多次测定的平均值与真值相符合的程度,用来表示误差的大小。精密度和准确度的区别就如同士兵打靶,如果子弹头分布很松散,则表明射击精密度低;如果子弹头密集在一起,则表明射击精密度高。在射击精密度高的情况下,聚集在枪靶中心的子弹头越多,则准确度越高。图2表示精密度高,准确度低;图3则表示精密度低,准确度高。
图2 精密度高,准确度低图
图3 精密度低,准确度高
定量限/检测限
定量限(Limit of Quantification,LOQ),指可定量测定样品中待测组分的最低浓度或最低量。此处所指的最低浓度,应满足上述精密度和准确度的要求。比如在满足1%精密度和±2%准确度的前提下,测量最低浓度为4 ppb的水样。如果低于这个值,测量结果将不再准确。
检测限(Limit of Detection,LOD),指能够被识别和检测的最低浓度。当仪器处于稳定状态时,仪器本身存在着噪声会导致测量读数出现漂移和波动。此值通常是仪器噪声水平标准偏差的3倍,检测限表示检测器对测定物质敏感程度的指标,其值越低,则说明检测器性能越好。
线性/范围
在给定范围内,所提供的样品与测试结果之间存在线性关系。通常,两点确定一条直线,对于最后的测试数据要求,应列出回归方程、相关系数、残差平方和以及线性图(或其他数学模型)。回归系数以1为基准,距离1越近则表示线性越好。
专属性
专属性指在其他成分(如杂质、降解产物、辅料等)可能存在的情况下,采用的方法能准确测定出被测物的特性,反映的是对被测物质准确而专属的测定能力,是用于复杂样品分析时相互干扰程度的度量。比如,对于总有机碳分析仪而言,不论样品化学结构或分子组成如何,都能准确地测量出其中的有机碳化合物。
以此建立专属性验证标样组,所使用的品种如下:
1瓶试剂水(空白溶液);
1瓶500 ppb的TOC标样(甲醇);
1瓶500 ppb的TOC标样(烟酰胺);
1瓶500 ppb的TOC标样(邻苯二甲酸氢钾,简称KHP)。
甲醇的分子式为CH3OH,由甲基和羟基组成,一个分子中仅含有一个碳原子,具有醇的化学性质,容易挥发和流失。即便只有一个碳原子,总有机碳分析仪仍能探测到它的存在,说明其专属性是合格的。
烟酰胺含有一个氮的杂原子,同样适用于含碳物质的测试。通过专属性测试,也能够测量出其中含有的物质。
KHP是一种呈无色单斜结晶或白色结晶性粉末状的化学物质,其特点是具有一个苯环,较难氧化,化学性质稳定,便于保存。可使用KHP进行检测,进而反映仪器的氧化能力。
样品溶液稳定性
样品溶液稳定性也称鲁棒性,是指仪器在受到扰动或者不确定的情况下,仍然可以维持某些性能的特性。英文名字为Robustness,即健壮和强壮。标样组设有以下几个品种:
1瓶试剂水(空白溶液);
1瓶500 ppb的TOC标样(USP 蔗糖);
1瓶500 ppb的TOC标样(USP 1,4-苯醌)。
根据美国药典USP<1225>分析方法验证的要求,所使用的试验方法必须是稳定的。举例而言,TOC既与温度无关,也与pH值无关,即使改变温度或pH值,也不会影响样品溶液的稳定性。
系统适用性
可通过两种最极端的物质,即一个在自然环境中最容易氧化的物质“蔗糖”和另外一种在自然环境中最不容易氧化的物质“1,4-苯醌”进行测试。各自配置500 ppb浓度的蔗糖溶液、500 ppb浓度的1,4-苯醌溶液,以及空白溶液放置到总有机碳分析仪中进行测定,测定的响应值分别记为Rs、Rss以及Rw,通过测定三种溶液,确定总有机碳分析仪的适用性。响应效率(Re)按下列公式计算:
Re=100[(Rss-Rw)/(Rs-Rw)]
如果85 %<Re<115 %,则确定该分析仪适用。药企可以根据自身生产的产品对风险进行评估。建议同步进行系统适用性测试(SST),以记录整个测量系统的性能(即人员、工艺、仪器和标样)。系统适用性标样的可接受回收率范围在85 %~115 %。如果能够通过系统适用性测试,则表明总有机碳分析仪的氧化性能良好。
结语
药企质量部和工程部人员不应只满足于对照药典和药品GMP指南中有关规定的字面理解,而应该从根本上掌握性能验证与各个测定项目的真正含义。在此基础上,使用合格的分析仪器来满足药品质量检测的需要。
本文作者就职于苏伊士Sievers分析仪。
邵丽竹
何发
热点文章
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
微生物发酵技术在植物活性成分提取中的应用研究进展
2026-03-06
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略















评论
加载更多