吹灌封一体化技术在国内基础输液产业中的应用及前景展望
静脉注射给药途径在我国药品不良反应中占比超过 50%。基础输液作为我国使用最广泛、用量最大的输液产品,其生产工艺及包装材料结构对临床安全性有着重要影响。吹灌封一体化技术(BFS)作为无菌制剂领域的先进制造工艺,在保障产品质量与降低污染风险方面具有显著优势,但它在基础输液产业中的应用广度与技术价值仍不相称。国家药品集中带量采购政策的常态化运行有效减轻了患者负担,同时也为基础输液等成熟产品的价格形成机制优化创造了有利条件。未来可进一步考量在医保支付标准中生产工艺及包装材料对基础输液安全性、经济性、适宜性的影响,通过真实世界综合价值评估完善基础输液医保支付体系,引导产业高质量发展,提高患者用药安全水平。
Part1 前言
2025 年 3 月 18 日,国家卫生健康委员会办公厅印发《2025 年国家医疗质量安全改进目标》,再次将“提高住院患者静脉输液规范使用率”列为十大改进目标之一,这也是静脉输液安全连续五年被列为十大改进目标之一 [1-5]。
2025 年 4 月 7 日,国家药品不良反应监测中心发布《国家药品不良反应年度监测报告(2024 年)》,按剂型统计,2024 年化学药品不良反应 / 事件报告中,注射剂占比 62.7% 和 31.9%,其他剂型占 5.4%。2024 年儿童药品不良反应 / 事件报告中,注射剂占 72.1%,口服制剂占 21.1%,其他制剂占 6.8%。根据 2020 年至2023 年度不良反应年度监测报告统计分析,注射剂中静脉给药不良反应占比均超过 90%,儿童患者的不良反应发生率均高于成人 [6-10]。
基础输液是我国最基本、用量最大的输液产品,属于国家医保目录甲类药品,不同包装材料在药学质量及临床安全方面存在差异化表现。全密闭式输液技术作为保障用药安全的重要发展方向,在国内的推广应用程度尚待进一步提升,以满足患者在静脉输液用药方面更安全、便捷的临床需求 [11]。
Part2 基础输液生产工艺及包装材料发展
随着医药工业的发展及更好地满足临床安全性及便捷性需求,基础输液产业经历了三个发展阶段 [12]。
第一阶段:全开放式输液包装系统。20 世纪 20年代,世界上第一代玻璃瓶包装的静脉输液产品诞生。该包装形式将药液置于广口瓶内,暴露在空气中,存在较大的用药安全风险,目前国内外市场已完全淘汰。
第二阶段:半开放式输液包装系统。20 世纪 30 年代,第二代输液产品诞生。输注时需连接进气管,使空气进入瓶内产生压力,药液才能输入人体。半开放式输注被空气污染的概率较大,设备老化,橡胶塞颗粒及玻璃碎屑的危害显著增加。目前,国外发达国家市场份额在10%以下,国内市场占有率在50%左右,存在较大差距。
第三阶段:全密闭式输液包装系统。20 世纪 70年代,第三代输液产品诞生,将硬塑料材质容器替换为塑料软袋包装。无需导入外界空气,在全密闭式状态下,通过袋体自收缩即可完成输液。国内企业相继推出了直立式软袋及内封式聚丙烯袋包装,兼具塑料瓶的临床便捷性优势及软袋的临床安全性优势,在市场上得到了广泛认可。全密闭式输液包装容器已成为国际主流选择,在欧美日等医药工业发达国家,全密闭式输液临床使用率达到 90% 以上。而在我国,受多种客观因素影响,全密闭式输液包装容器的使用普及率虽有所提升,但与国际水平相比仍存在差距。例如,二级及以下医院因成本等因素制约,使用率低于 50%。然而,随着国产技术的日益成熟和政策的有力引导,这一差距正逐步缩小。
Part3 吹灌封一体化技术(BFS)
BFS 技术已获得国内外药品监管部门及行业协会的广泛认可。美国食品药品监督管理局(FDA)、美国药典委员会(USP)、欧盟药品生产质量管理规范(GMP)以及中国新版 GMP 附录均设有专门章节阐述其技术要求,其中美国注射剂协会(PDA)将其视为无菌生产领域的先进工艺之一。此外,我国2010版GMP在附录一(无菌药品)中新增了第五章吹灌封技术,旨在鼓励药品生产企业采用 BFS 工艺以提高无菌药品质量和研发能力。
在 BFS 工艺中,采用热塑性聚合物形成内包装主容器。颗粒状聚合物(粒状颗粒)通过真空转移至封闭通道。该系统将聚合物颗粒送入标准塑料热熔体挤出工艺。在挤出过程中,聚合物被加热至超过 170℃,承受20 000 kPa 以上的压力。挤出机中塑料的温度、压力和密闭性减少了任何污染物(如微粒、真菌、细菌芽孢、内毒素)与最终灌装产品接触的可能性。该工艺设计使BFS 技术在以下三个维度展现出显著优势:
最小化人工干预:吹灌封容器由挤出的热塑性型坯形成灌装产品,然后通过连续、整合的高度自动化操作密封,减少操作所需人员数量。减少人员干预可降低人为错误及人员干预导致的污染风险。吹灌封机械可配备空气管理系统(如采用持续的正压除菌过滤空气覆盖关键灌装区域),从而减少人员干预带来的影响与风险。在关键干预之后、无菌灌装之前,产品通道会通过蒸汽进行在线灭菌。
最小化空间要求:由于关键灌装区域设置在吹灌封设备内部,该工艺设计降低了对空间的需求。吹灌封工艺不需要单独设置清洗、除热源、冷却、组装、灌装、加塞或轧盖位置。
最小化物流:对于内包装原料,吹灌封技术减少了供应商数量与物料供应的物流成本,并提供了额外的控制。对于吹灌封工艺而言,树脂供应商是吹灌封工艺中形成容器时使用的唯一内包装原料供应链来源。
Part4 BFS 技术在国内基础输液产业中的应用
BFS 技术起源于德国,在 20 世纪 60 年代主要应用于冲洗剂等产品,70 年代应用于小容量注射剂,80 年代则应用于大容量注射剂。目前,在欧盟、南美洲、印度、墨西哥等国家和地区,该技术在基础输液产业化中得到了广泛应用。尤其是在德国,BFS 输液产品的市场占有率超过了 75%。而在我国,BFS 技术在基础输液产业化方面的应用尚处于起步阶段,市场占有率不足 1%。
4.1
生产工艺控制
表 1 基于 BFS 技术的基础输液生产工艺优势
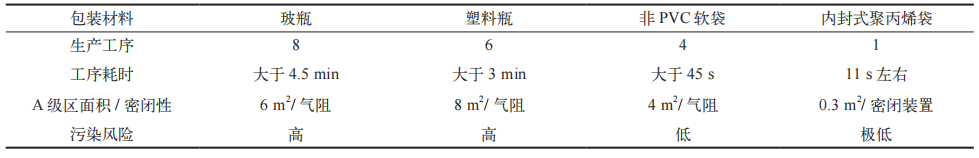
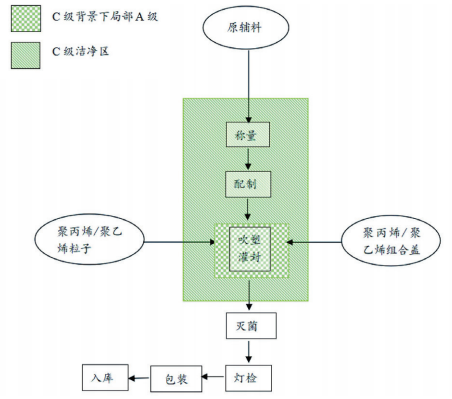
图 1 基于吹灌封一体化技术的基础输液生产工艺流程图
4.2
影响输液安全性指标控制
4.2.1
不溶性微粒
成年人毛细血管管径一般为 6 ~ 8 μm,而儿童毛细血管管径仅有 3 ~ 5 μm。不溶性微粒粒径小于 2 μm可通过肾交换排出体内,而 2 μm 到 10 μm 的不溶性微粒可在体内长期存在达 20 年。由于这些微粒进入体内后无法被代谢,因此更易引起不良反应,有必要关注儿童群体中不良反应与不溶性微粒的相关性。
输液中的不溶性微粒受生产过程中的多种因素影响,因此控制输液生产过程中的不溶性微粒含量非常重要 [14]。目前,已开发出显微镜法、光散射法、光阻法以及电阻法等多种不溶性微粒检测技术。然而,各国药典仅对注射剂中粒径在 10 μm 及以上的不溶性微粒进行控制,对粒径小于 10 μm 的微粒却没有明确的要求。研究发现,某些药品中 2 ~ 10 μm 微粒的数量远多于10 μm 及以上的微粒,且这些不可代谢的不溶性微粒可能对人体造成潜在的严重危害 [15]。
4.2.2
细菌内毒素
表 2 基础输液细菌内毒素(EU/ml)标准
4.2.3
临床便捷性
基础输液虽长期以来被视为低风险药品,但其潜在的安全隐患不容忽视。现有市场上常见的包装形式包括玻璃瓶、塑料瓶、非 PVC 软袋、直立式聚丙烯袋以及内封式聚丙烯袋,其中半开放式系统在输注过程中需引入空气以维持压力,这显著增加了空气污染与中心静脉导管相关血流感染(CLABSI)的发生风险。相较之下,全密闭式系统通过自封闭技术避免空气进入,能够有效降低感染率和患者死亡率。国家《静脉治疗护理技术操作标准》已明确建议优先采用全密闭式系统,但在我国临床实践中的应用率仍不理想。
基础输液产品的不同包装形式会影响临床使用的便捷性。内封式聚丙烯袋作为密闭式容器,具有自体收缩排液功能,液体残留量较低,相较于玻璃瓶、塑料瓶等开放式或半开放式输液包装形式具有明显的临床优势。此外,内封式聚丙烯袋具备直立功能,提高了临床使用的便捷性,且相较于软袋能够承受更高的机械强度,漏液率较低。
Part5 发展与展望
参考文献
[1]国家卫生健康委办公厅. 2025年国家医疗质量安全改进目标[EB/OL]. [2025-03-18]. https://www.nhc.gov.cn/yzygj/c100068/202503/ad63fb8ce9e24013a68db52049ecc524/files/1743410147292_68704.pdf.
[2] 国家卫生健康委办公厅. 2024年国家医疗质量安全改进目标[EB/OL]. [2024-02-01]. https://www.nhc.gov.cn/yzygj/c100068/202402/0359e2adda284e69b676e94c24426b0d/files/1733999813027_60751.pdf.
[3] 国家卫生健康委办公厅. 2023年国家医疗质量安全改进目标[EB/OL]. [2023-02-24]. https://www.nhc.gov.cn/yzygj/c100068/202302/5d9f7e4ef1d8472fa9ac6d19140dfb83/files/1733999837372_74067.pdf.
[4] 国家卫生健康委办公厅. 2022年国家医疗质量安全改进目标[EB/OL]. [2022-03-02]. https://www.nhc.gov.cn/cms-search/downFiles/52710130bc5048e589d305ebef92fc20.pdf.
[5] 国家卫生健康委办公厅. 2021年国家医疗质量安全改进目标[EB/OL]. [2021-02-09]. https://www.nhc.gov.cn/yzygj/c100068/202102/116305f4cb174ef59b02be71ac826b6b/files/1733999823832_79780.pdf.
[6] 国家药品不良反应监测中心. 国家药品不良反应监测年度报告(2024年)[EB/OL]. [2025-04-07]. https://www.cdr-adr.org.cn/center_news/202504/t20250407_51076.html.
[7] 国家药品不良反应监测中心. 国家药品不良反应监测年度报告(2023年)[EB/OL]. [2024-03-26].https://www.cdr-adr.org.cn/drug_1/aqjs_1/drug_aqjs_sjbg/202403/t20240326_50614.html.
[8] 国家药品不良反应监测中心. 国家药品不良反应监测年度报告(2022年)[EB/OL]. [2023-03-24].https://www.cdr-adr.org.cn/drug_1/aqjs_1/drug_aqjs_sjbg/202303/t20230324_50019.html.
[9] 国家药品不良反应监测中心. 国家药品不良反应监测年度报告(2021年)[EB/OL]. [2022-03-30].https://www.cdr-adr.org.cn/drug_1/aqjs_1/drug_aqjs_sjbg/202203/t20220330_49586.html.
[10] 国家药品不良反应监测中心. 国家药品不良反应监测年度报告(2020年)[EB/OL]. [2021-03-26].https://www.cdr-adr.org.cn/tzgg_home/202103/t20210326_48414.html.
[11] 苗雅楠,骆泰庆,王薇. 各类基础输液产品包装的综合评价:文献系统综述[J].中国卫生资源,2020,23(3):232-247.
[12] 鄂海燕,王亚丽,唐玲,等. 国内静脉输液技术溯源[J]. 中西医结合护理,2022,8(3):124-128.
[13] 中国医药包装协会. 基础输液临床使用评估指南:T/CNPPA 3003-2018[S]. 北京:中国医药包装协会,2018.
[14] 彭姝,李慧芬,任重远,等. 影响输液不溶性微粒的相关因素[J]. 中国药品标准,2019,20(2):101-109.
[15] 王宏亮. 化药注射剂中不溶性微粒的产生原因及控制策略分析[J]. 药物评价研究,2022,45(9):1909-1913.
[16] 李英,关玮伟,张英,等. 不同基础输液与儿科常用药加药前后不溶性微粒考察[J]. 中国临床药理学杂志,2019,35(14):1526-1529
邵丽竹
何发
相关推荐
-
打造工业AI新时代,西门子科技大会即将在京启幕
2026年3月23日,西门子科技大会将在京启幕。博乐仁携手蔡崇信等领袖共话工业AI,首发26款本土新品,呈现3000平米沉浸式展区,定义工业AI新时代,加速产业智能化转型。
2026-03-17 西门子
-
礼来投资30亿美元加码在华供应链
美国制药巨头礼来公司3月11日宣布,计划未来十年累计投资30亿美元全面扩展在华供应链产能,打造口服固体制剂本土生产与供应体系。这是礼来过去两年内在中国的第二次重大投资,也是其有史以来规模最大的全球生产扩张计划的重要组成部分。
2026-03-16 网络、礼来
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略
















评论
加载更多