Arvinas在靶向蛋白降解领域处于领先地位, 其研发管线包括多个PROTAC药物,如用于治疗雌激素受体阳性/人表皮生长因子2阴性(ER+/HER2-)乳腺癌的vepdegestrant(ARV-471),用于治疗转移性去势抵抗性前列腺癌(mCRPC)的ARV-766,以及能穿透血脑屏障的口服降解剂ARV-102(LRRK2)用于治疗帕金森病(图1)[1]。
Arvinas与多家大型制药公司建立了合作关系,包括与辉瑞达成20亿美元合作,以及与诺华达成超10亿美元合作。这些合作有助于加速其PROTAC药物的研发和商业化进程。

图1. Arvinas研发管线
Vepdegestrant是一种选择性、口服生物利用度高且强效的小分子降解剂,能够特异性靶向和降解雌激素受体(ER)。在临床前研究中,Vepdegestrant在肿瘤细胞中显示出高达97%的ER降解率,并在多种ER驱动的异种移植模型中显著缩小肿瘤。
Vepdegestrant是首个进入临床3期的PROTAC药物,Arvinas和辉瑞计划到2025年公布针对二线ER+/HER2-转移性乳腺癌(mBC)患者的3期单药治疗临床试验VERITAC-2的主要数据,并在ER+/HER2- mBC患者中启动两项新的3期联合试验(图2)。

图2. 3期单药治疗临床试验VERITAC-2方案
除此之外,Vepdegestrant还在临床上开展多项实验,包括评估Vepdegestrant联合CDK4/6抑制剂在重度预处理的局部晚期或转移性ER+/HER2-乳腺癌患者中的安全性和有效性的I/II期VERITAC研究,评估Vepdegestrant与CDK4/6抑制剂联合治疗局部晚期或转移性ER+/HER2-乳腺癌患者的效果和安全性的1期TACTIVE-U研究等(图3)。
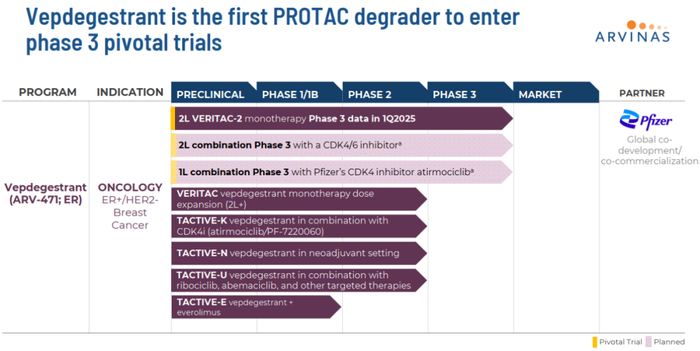
图3. Vepdegestrant临床实验布局
ARV-102是由Arvinas公司开发的一种新型口服PROTAC降解剂,旨在穿过血脑屏障,靶向降解富亮氨酸重复激酶2(LRRK2),这是一种大型多结构域支架激酶。LRRK2活性和表达的增加在遗传上参与多种神经疾病的发病机制,包括帕金森病和进行性核上性麻痹(图4)。
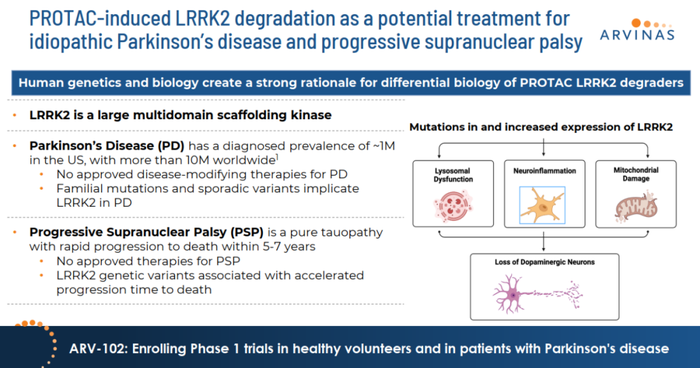
图4. 靶向LRRK2的口服PROTAC ARV-102
与传统的LRRK2激酶抑制剂相比,ARV-102显示出更好的靶向结合、更高的效力以及更强的通路结合能力。在小鼠模型中,ARV-102的效力比激酶抑制剂高出约100倍,能够显著影响大脑中的靶标和溶酶体通路标记物Phospho RAB(图5)。
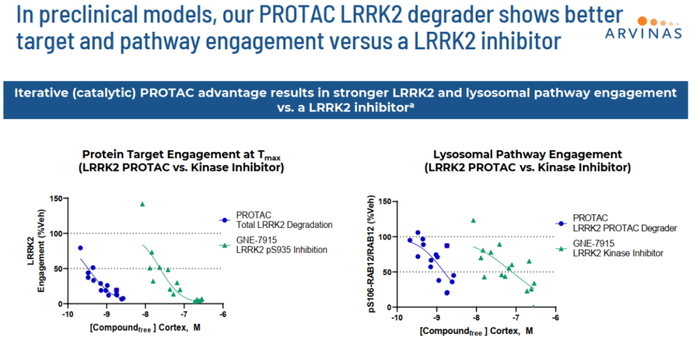
图5. ARV-102比抑制剂显示更强活性
2024年2月20日,Arvinas宣布已完成ARV-102在1期临床试验中的首位受试者给药。该试验由荷兰莱顿人类药物研究中心(CHDR)招募健康志愿者,旨在评估ARV-102在人体中的安全性、耐受性、药代动力学和药效学情况,包括评估LRRK2降解情况及探索LRRK2通路生物标志物。
ARV-393是由Arvinas公司开发的一种口服小分子BCL6降解剂,通过连接链将BCL6抑制剂与CRBN配体连接而得。
ARV-393在几种NHL细胞系来源的异种移植模型中表现出剂量响应性的肿瘤生长抑制,这与BCL6的降解相关(图6)。

图6. ARV-393的细胞活性
在临床前研究中,ARV-393在多种非霍奇金淋巴瘤(NHL)患者来源的异种移植模型中诱导肿瘤消退(图7)。
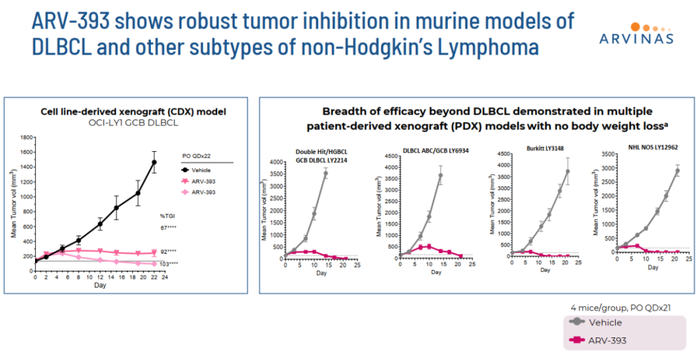
图7. ARV-393小鼠体内药效
目前,ARV-393正在进行一项多中心、首次人体、1期临床试验(NCT06393738),旨在评估ARV-393在晚期B细胞NHL或nTFHL-AI患者中的安全性、耐受性、药代动力学、药效学和初步抗肿瘤活性。
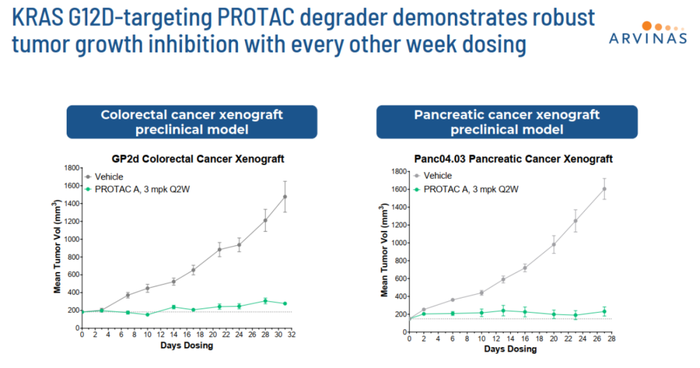
Arvinas还在开发针对KRAS-G12D突变的PROTAC降解剂,旨在通过降解KRAS-G12D蛋白来治疗癌症。
在临床前研究中,该KRAS-G12D降解剂在多种肿瘤细胞中显示很强的抑制活性(图8)。
百济神州的CDAC(Chimeric Degradation Activating Compound)技术平台是一种创新的蛋白降解技术,旨在通过靶向降解特定蛋白质来治疗疾病。CDAC平台具有更广泛的E3连接酶识别能力以及组织特异性等优势。
BGB-16673是百济基于其CDAC平台开发的首款口服靶向BTK的嵌合式降解激活化合物,通过触发BTK蛋白的消除,防止BTK活性并中断其作为结合伴侣的功能。它对野生型BTK和多种突变型BTK均有效。BTK在B细胞的发育和成熟中起重要作用,多种血液癌症细胞表现出过度的BTK活性,导致癌细胞的生存和生长[2]。
2024年8月,BGB-16673被FDA授予快速通道认定,用于治疗既往接受过至少两线治疗(包括BTK抑制剂和BCL2抑制剂)的复发/难治性(R/R)慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)成年患者。
在2024年欧洲血液学协会年会上公布的1/2期首次人体试验(CaDAnCe-101,NCT05006716)数据显示,BGB-16673用于治疗既往接受过多线治疗的R/R CLL/SLL患者具有可耐受的安全性和良好的有效性(图9)。
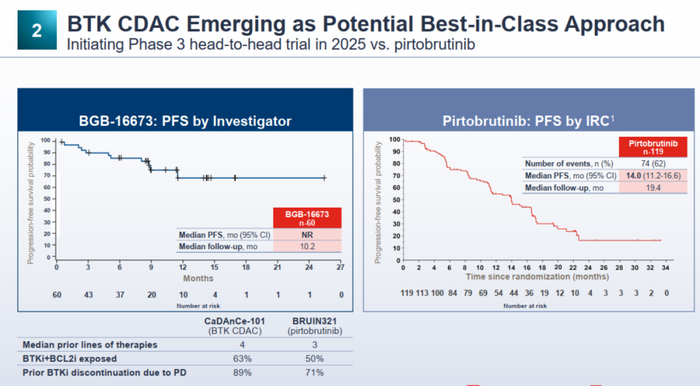
图9. CaDAnCe-101实验结果
百济计划在2025-2026年启动与礼来的Pirtobrutinib头对头的针对R/R CLL的3期临床研究。
BGB-60366是由百济研发的一款具有差异化作用机制的新型EGFR降解剂(EGFR CDAC),通过独特的机制有望实现EGFR信号的完全抑制,破坏EGFR支架功能,产生持久的信号抑制作用。在前期治疗线中,其非冗余机制有望有效防止耐药性的发生,为患者提供更长久的治疗效果。
临床前研究显示,BGB-60366对奥希替尼敏感和耐药的EGFR突变均表现出较高的有效性,同时对野生型EGFR无影响,蛋白质组选择性良好,每日口服给药即可表现出较强的治疗效果(图10)。
2024年11月14日,百济神州的BGB-60366片的临床试验申请已成功获得中国国家药监局药品审评中心(CDE)受理,已于2024年12月启动一项开放标签、多中心的1a/1b期临床研究,评估BGB-60366在晚期或转移性EGFR突变的非小细胞肺癌患者中的安全性、耐受性、药代动力学、药效学和初步抗肿瘤活性。该研究计划纳入93名受试者。
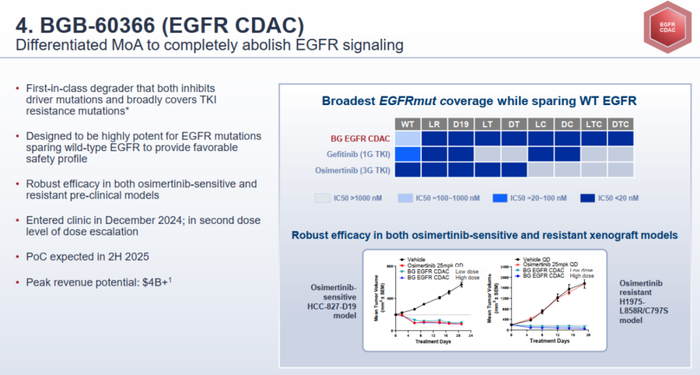
图10. BGB-60366临床前结果
BGB-45035是由百济基于CDAC技术平台研发的一款靶向IRAK4的蛋白降解剂,临床前研究显示,BGB-45035对IRAK4的降解效果显著,能够有效抑制炎症信号通路,从而发挥良好的抗炎作用(图11)。
2024年6月,百济神州启动了一项评估BGB-45035在健康受试者中单次和多次递增剂量的安全性、耐受性、药代动力学和药效学以及食物效应的1期随机研究,随后8月14日,BGB-45035片获得CDE的临床试验默示许可,拟用于治疗中重度特应性皮炎。
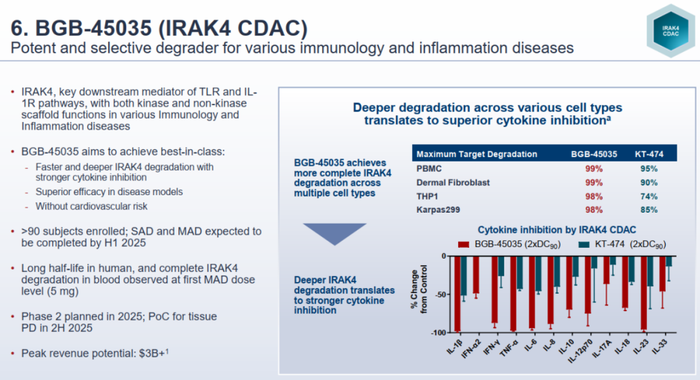
图11. BGB-45035临床前结果
Kymera Therapeutics是一家成立于2015年专注于开发蛋白降解剂的创新型企业,布局的靶点有IRAK4、STAT6、TYK2等,主要用于治疗癌症和免疫性炎症疾病,如化脓性汗腺炎(HS)、特应性皮炎(AD)和炎症性肠病(IBD)等(图12)[3]。
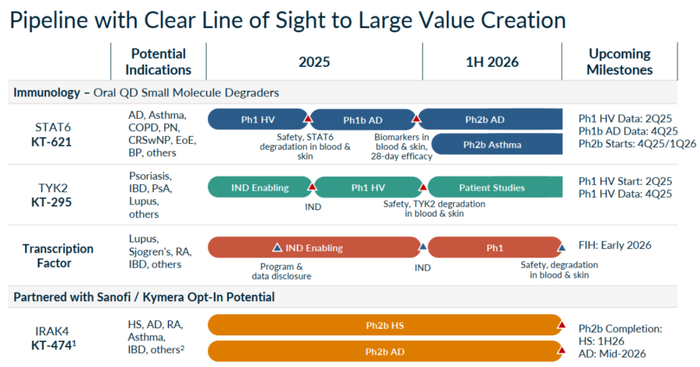
图12. Kymera Therapeutics临床管线和关键节点
KT-474是一种潜在的first-in-class的IRAK4降解剂,正在开发用于治疗TLR/IL-1R驱动的免疫炎症性疾病,例如特应性皮炎、化脓性汗腺炎、类风湿性关节炎等(图13)。
与靶向单一细胞因子的单克隆抗体相比,KT-474旨在更广泛地阻断TLR/IL-1R介导的炎症,通过消除 IRAK4的激酶和支架功能来实现通路抑制。
2020年7月,Kymera 曾与赛诺菲达成多项计划的战略合作,获得1.5亿美元的预付款,并可能获得超过20亿美元的潜在开发、监管和销售里程碑,以及可观的特许权使用费。
2023年11月13日,Kymera公布了KT-474的1期临床试验取得积极结果,并发表于《Nature Medicine》。
研究结果显示:在105名健康志愿者(HV)中,单剂量600-1600 mg后IRAK4降解平均降低≥93%,14天后单剂量50-200 mg后平均降低≥95%,在接受75 mg KT-474治疗的患者中,血液中也实现了类似的IRAK4降解,表明该药物对缓解化脓性汗腺炎(HS)和特应性皮炎(AD)患者的疾病负担和症状产生了积极的作用,且在中度至重度疾病患者中观察到了全身抗炎作用。
2023年12月7日,Kymera Therapeutics宣布第一位患者已在2期ADVANTA研究中接受给药,用于评估KT-474在特应性皮炎(AD)中的作用,触发与赛诺菲合作产生的1500万美元里程碑付款。
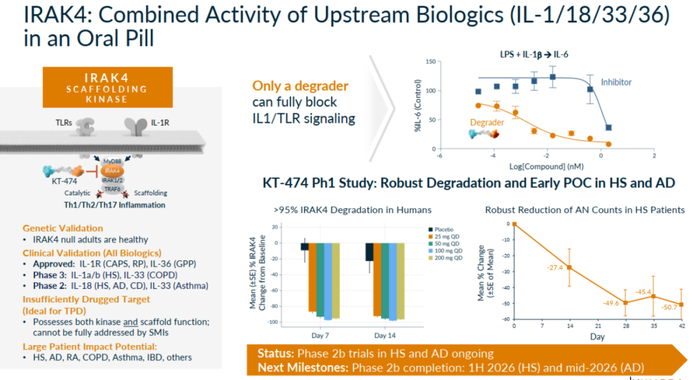
图13. KT-474临床实验结果
KT-295是一种潜在的first-in-class的TYK2降解剂,通过降解TYK2来抑制其激酶和支架功能,从而广泛阻断IL-23、IL-12和I型干扰素(IFN)信号通路。与传统的小分子抑制剂不同,KT-295在皮摩尔水平上显示出强大的降解活性,并且在临床前动物模型中显示出比KT-294更强的体内活性(图14)。
KT-295在临床前研究中显示出对TYK2的高度选择性和强大的降解活性,有望成为首个在IBD和银屑病等疾病中达到类似生物制剂效果的口服疗法,Kymera计划在2025年上半年将KT-295推进到1期临床试验,并预计在当年晚些时候报告1期数据。
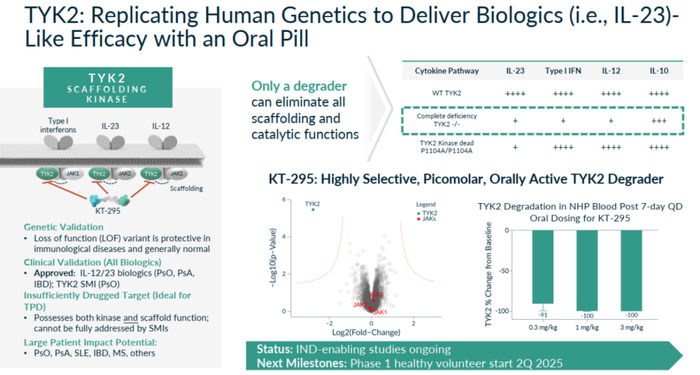
图14. KT-295是一种潜在的first-in-class的TYK2降解剂
KT-621是一种潜在的first-in-class的口服STAT6降解剂,通过降解STAT6来抑制其转录因子功能,从而广泛阻断IL-4/IL-13信号通路,调节过敏性2型炎症反应。
KT-621在多种临床前模型中表现出与度普利尤单抗相当或优效的活性,且耐受性良好。在hIL4/hIL4RA人源化小鼠的鼻内尘螨(HDM)诱导哮喘模型中,口服KT-621耐受良好,连续给药30天,与度普利尤单抗的体内疗效相当(图15)。
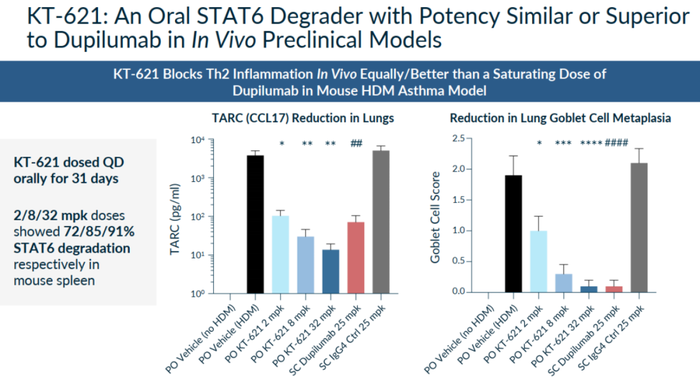
图15. KT-621临床前药效结果
KT-621对STAT6的选择性优于其他STAT6,且在关键的人TH2细胞检测中完全阻断IL-4/IL-13功能,其皮摩尔效价优于度普利尤单抗(图16)。
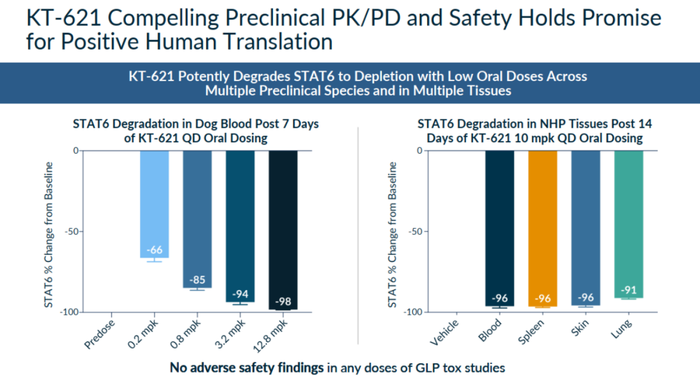
图16. KT-621的PK/PD结果
KT-621的1期临床试验已于2024年10月24日开始给药,预计2025年上半年公布初步结果。该试验将评估KT-621在健康志愿者中的安全性、耐受性、药代动力学和药效学。
Kymera计划在2025年第二季度开始针对特应性皮炎(AD)患者的Ib期试验,预计数据将在第四季度公布,AD和哮喘的IIb期试验计划分别于2025年底和2026年初开始。
靶向蛋白降解领域正在蓬勃发展,全球各大药企和新兴企业纷纷加入布局,已经有多款药物进入临床,尤其是Arvinas的ARV-471和BMS的BMS-986365都已进入临床3期,相信不久的将来就会有首款靶向蛋白降解药物获批上市。
1.Arvinas: 43rd Annual J.P. Morgan Healthcare Conference
2.BeiGene: 43rd Annual J.P. Morgan Healthcare Conference
3.Kymera Therapeutics: 43rd Annual J.P. Morgan Healthcare Conference





























评论
加载更多