美国顺铂不再短缺

自2023年2月份开始,顺铂在美国市场上开始出现短缺,到2023年3月下旬短缺情况加剧,大量的美国医院开始限制对这种药物的供应,许多患者不得不减量用药、寻找替代用药以及需要等药,面临严重治疗延误风险。
严重依赖印度供应
顺铂是一种抗癌药,能够抑制癌细胞的生长和分裂,是临床上常用的化疗药物之一。根据美国国家癌症研究所的数据,10%到20%的癌症患者中有使用这种药物治疗。
一直以来,美国在顺铂等药物的供应方面非常依赖印度仿制药,美国市场一半以上的顺铂,由一家名为Intas的印度制药公司供应。
据FDA肿瘤卓越中心主任Richard Pazdur博士表示,美国这次顺铂短缺正是始于2022年11月FDA对Intas一家位于印度Gujarat的制造工厂一次现场突击检查,FDA调查人员发现,这家制造工厂存在严重的质量控制问题,包括故意撕碎cGMP文件,销毁原始数据等11项违规。之后,FDA便停止了该工厂向美国的出口。为解决FDA发现的质量问题,在2023年2月,Intas关停了顺铂及相关替代品的生产线。
而在Intas工厂关闭之前,FDA事实上并不知道这家工厂生产的顺铂占据美国进口顺铂市场如此大的份额。因此在这家工厂关停后,美国顺铂市场供应巨大的缺口出现了。
除了Intas之外,Teva、Hikma Pharmaceuticals等在内5家顺铂生产的制药公司均不同程度出现顺铂供应短缺,和延期交货等情况。
顺铂短缺的加剧,也引发市场的连锁反应。美国市场对同样是抗癌药的卡铂需求增大增,很快也一药难求,一并出现在了FDA的药品紧缺名单上。2023年5月,包括卡培他滨片、卡铂注射液、顺铂注射液在内的抗癌药都出现了短缺。
考虑美国本土的生产情况,FDA不得不选择向中国求助。2023年3月,FDA向齐鲁制药一封紧急邮件,询问齐鲁制药的顺铂注射液能否出口美国。得到齐鲁制药的肯定答复后,FDA迅速启动了快速审批程序,仅用2个月就完成了审批。2023年6月6日,齐鲁制药的顺铂注射液正式美国上市销售。
美国药物短缺创新高
美国药物短缺已经由来已久,并且短缺现象日益加剧。根据美国卫生系统药师协会(ASHP)数据,截至2024年第一季度,美国有323种药物处于短缺状态,这是ASHP自2001年开始追踪药物短缺以来的最高水平,创下新高。
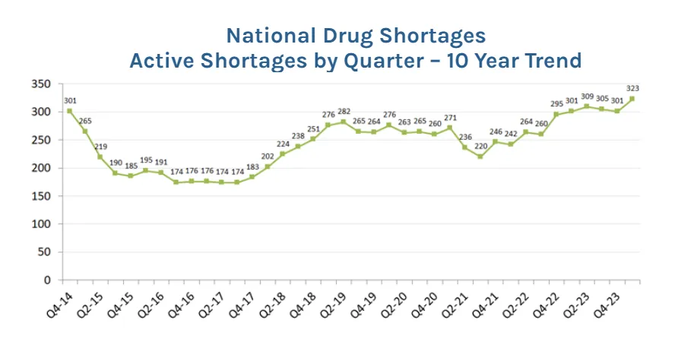
根据ASHP这个统计,除了顺铂、卡铂等抗癌药外,药物短缺现象已经出现多个治疗领域,从急救注射剂到糖尿病治疗药物。其中备受影响包括的糖尿病药物Ozempic和Mounjaro、过敏治疗药物肾上腺素、儿童常用抗生素阿莫西林、以及重症监护中常用的注射剂等。
除了Ozempic和Mounjaro这类由于需求激增而产能跟不上的新药之外,其中短缺的大部分都是仿制药。据美国医疗行业人士表示,主要原因系很多生产商看不到这类药物的利润,退出了这一市场。
为了缓解药物短缺问题,FDA也将目光投向了美国以外的制药企业。
参考出处:
https://www.accessdata.fda.gov/scripts/drugshortages/dsp_ActiveIngredientDetails.cfm?AI=Cisplatin%20Injection&st=r&tab=tabs-1
https://www.fiercepharma.com/manufacturing/fda-heralds-end-us-shortfall-chemo-drug-cisplatin
凭一己之力令美国癌症化药告急的印度药企Intas是何方神圣
美国三百余种药物短缺!全球仿制药机会,华海、齐鲁、新华等能否突围?
撰稿人 | 不周 生物制药小编
责任编辑 | 邵丽竹
审核人 | 何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多