全球首款:Merus递交HER2/HER3双抗上市申请

该上市申请依据的是eNRGy 1/2期临床试验数据。

Zenocutuzumab为全球首创的HER2/HER3双抗。
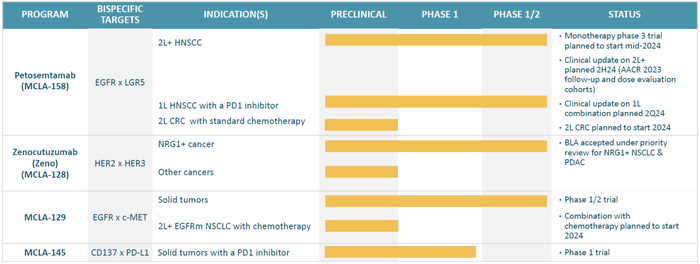
Zenocutuzumab此前已经获得FDA的突破疗法认证和快速通道资格。

Zenocutuzumab的临床方案设计如下。
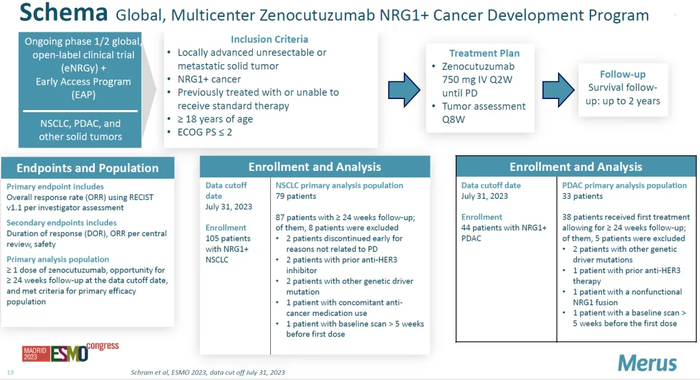
对于NRG1+非小细胞肺癌,ORR为37.2%,CRB为61.5%,mDOR为14.9个月,起效平均时间为1.8个月。

对于NRG1+胰腺癌,ORR为42.4%,CBR为72.7%,mDOR为9.1个月,起效平均时间为1.8个月。

总结
先声药业曾在2018年引进Zenocutuzumab的中国权益,后终止合作。Merus的EGFR/cMET双抗则将中国权益授权给贝达药业,目前处于1/2期临床阶段。

撰稿人 | Armstrong 医药笔记
责任编辑 | 邵丽竹
审核人 | 何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多