药典中的“温度”你了解多少?


中国药典 Ch.P<0601>相对密度测定法,温度要求:20℃;
美国药典USP<841> Specific gravity,温度要求:25℃;
欧洲药典EP<2.2.5> Relative density,温度要求:20℃。
旋光度
中国药典Ch.P<0621>旋光度测定法,温度要求:20±0.5℃;
美国药典USP<781> Optical rotation,温度要求:25±0.5℃;
欧洲药典EP<2.2.7> Optical rotation,温度要求:20±0.5℃。
折光率
中国药典Ch.P<0622>折光率测定法,温度要求:20±0.5℃;
美国药典USP<831> Refractive index,温度要求:20℃;
欧洲药典EP<2.2.6> Refractive index,温度要求:20±0.5℃。
炽灼残渣/硫酸灰分
中国药典Ch.P<0841>炽灼残渣检测法,温度要求:700~800℃,(如需将残渣留作重金属检查,则炽灼温度500~600℃);
美国药典USP<281> Residue on ignition,温度要求:600±50℃;
欧洲药典EP<2.4.14> Sulfated ash,温度要求:600±50℃;
欧洲药典EP<2.4.16> Total ash,温度要求:600℃±25℃;
pH
中国药典Ch.P<0632>,不同温度的k值:列出k值计算公式,两位有效数字;
美国药典USP<791> pH,不同温度的k值:列出15.00~35.00℃ 5个温度下的k值,4位有效数字。温度一般要求是25±2℃;
欧洲药典EP<2.2.3> Potentiometric determination of pH,不同温度的k值:列出15~35℃ 5个温度下的k值,3位有效数字。温度一般要求是20-25℃。
中美欧药典中凡例对于温度的要求及解释
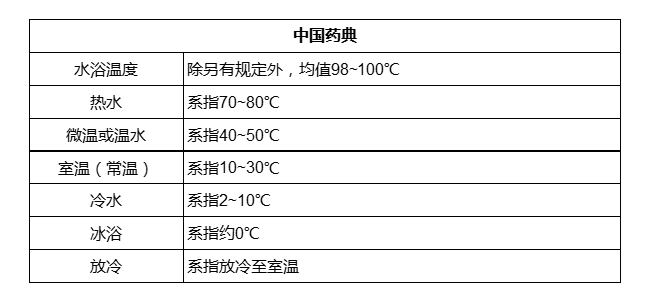
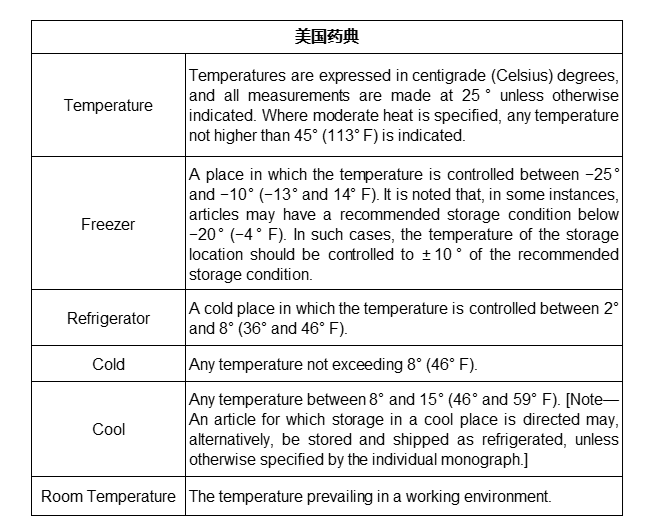
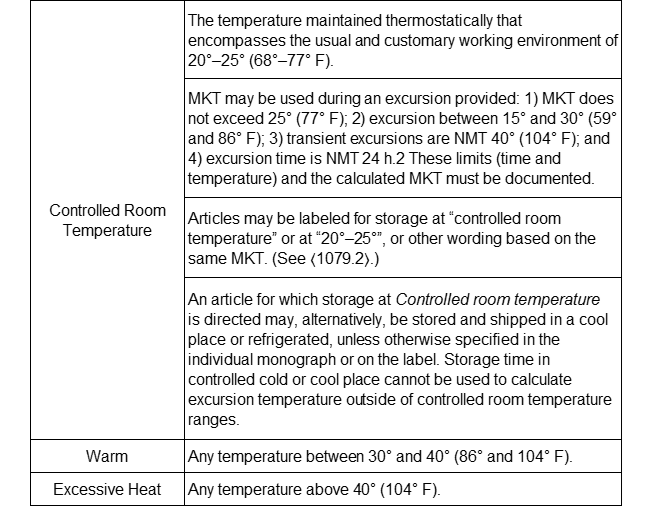

撰稿人 | 润柏医药
责任编辑 | 胡静
审核人 | 何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多