药物产品生产过程中过滤器可析出安全风险的冲洗研究
简介
监管机构要求进行可溶出物和可析出物 (E&L) 风险评估,以评估最终药品中可析出物对患者的安全风险。E&L 风险评估包括生产过程中使用的材料、医疗器械和容器密闭系统的风险识别、风险分析和风险评估。风险可以按严重性(危害的可能后果的衡量标准)和概率(已识别风险发生的可能性)进行评分。失效模式效应分析可用于描述与药品接触的工艺步骤和材料。了解风险发生的方式和地点可用于对产品生产过程、存储和配料中每个步骤的严重性和可能性进行评分。此外,材料的生物相容性和来自供应商的可溶出物信息可用于支持材料评分。可影响可析出物的数量和水平的因素包括接触时间、流体成分、产品接触表面积比、温度、材料的相容性和可析出物的减少潜力。当材料被评为高风险时,需要进一步开展工作,例如,进行可溶出物和可析出物研究,以了解产品质量和安全的风险。
过滤器通常用于生物制药行业的上游和下游工艺,以去除或控制生物负荷。当在生产过程结束时用于过滤药品时,过滤器往往被认为是最终药品中可析出物的潜在高风险。这主要是由于它们与药物产品接触的表面积大,并且在工艺后期减少可析出物的可能性较低。通常,过滤器在使用前需要冲洗,以调节和去除潜在的可析出物。供应商可能会提供有关调节和冲洗过滤器的可溶出物信息和建议,但这些研究倾向于使用不适用于实际生产过程的苛刻或加速条件,因此可能高估了潜在的可析出物和冲洗量。生产过程是特定于产品的,包括预处理步骤,这些步骤未包含在供应商提供的可溶出物信息中。
来自伽马辐照过滤器装置的典型可析出物由膜亲水剂(如果使用)、有机酸和一些可通过冲洗过滤器轻松去除的挥发物组成。过滤器的可溶出物是来自膜或过滤器外壳的分解产物、添加剂或来自初始聚合的起始材料。
总有机碳 (TOC) 分析可用于估计溶出材料的总量并提供可溶出物的概况。可溶出物的表征通常通过分别使用顶空 GC-MS、直接进样 GC-MS 和液相色谱质谱 (LC-MS) 筛选挥发性、半挥发性和非挥发性物质的材料溶出物来完成。TOC 是量化筛选方法中未检测到的可溶出物的有效工具。样品的 TOC 分析显示对于从过滤器中获取可溶出物的准确概况非常有用,并且可用于计算最小冲洗量。使用 TOC 的过滤冲洗研究建议执行初始冲洗并丢弃初始冲洗,以最大程度地减少可析出物。
在本案例研究中,使用过滤器对药品进行除菌,然后再将其灌装到最终容器(1 mL 注射器)中,最终过滤器下游没有产品合并。由于过滤器的表面积大并且没有减少可析出物的可能性,因此过滤器被评为高故障模式。因此,对过滤器的可溶出性研究旨在模拟生产过程,并提供对最终药品中潜在可析出物风险的理解。用水冲洗过滤器并收集累积馏分,以获得 TOC 溶出曲线,表明潜在可析出物的总量。此外,使用顶空 GC-MS 分析收集的馏分,以筛选挥发性物质,并使用直接进样 GC-MS 筛选半挥发性物质。没有研究水溶出物的非挥发性物质,因为众所周知,水溶出物仅显示可忽略不计的非挥发性可溶出物。在本案例研究的生产过程中,最初用 DP 冲洗过滤器,以去除潜在的可析出物,并在将 DP 灌装到最终容器之前丢弃初始体积。本研究的目的是确定通过过滤器的最小冲洗体积,以去除潜在的可析出物,并确保质量和产品安全。
材料与方法
实验设计
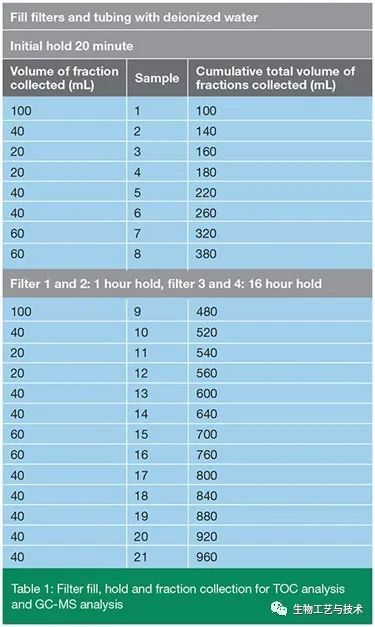
进行了四次过滤器实验,从保持 20 分钟开始,并以特定流速初始冲洗 380 mL,以代表生产过程中的灌装步骤。初次冲洗后,对两个过滤器应用 1 小时保持,对另外两个过滤器应用 16 小时保持。在过滤器之后和收集馏分之前,连接一根管子以模拟在生产过程中过滤和最终灌装注射器之间的管子体积。如表 1 中所述,收集馏分用于 TOC 分析和 GC-MS 分析。
分析评估阈值
ICH M7 指南评估和控制药物中的 DNA 反应性(诱变)杂质以限制潜在致癌风险中概述的原则被用作定义报告阈值的方法。考虑到药品的不同剂量和给药方式,已定义了与 ICH M7 中的毒理学关注阈值 (TTC) 概念一致的报告阈值,即 10 mcg/day,给药持续时间为 1 至 10 年。基于每天 3 个注射器的最大剂量,TTC 相当于 3.3 mcg/注射器的最大可析出水平。从这些注射器中输送的标称体积为 1 mL。因此,这相当于 3.3 mcg/mL 作为生产过程的输出,并且是为 TOC 分析设置的报告阈值。
由于受控可提取物研究使用去离子水而不是实际药物产品,并且由于 GC-MS 的响应因子变化,因此对使用 GC-MS 检测的可溶出物应用不确定因子。1.6 mcg/mL 的分析评估阈值 (AET 50%) 用于 GC-MS 检测的可溶出物。
设备和样品制备
总有机碳 (TOC)
在配备 GE 自动进样器的 Sievers M9 TOC 仪器上对收集的水馏分进行 TOC 测量。氧化剂是 15% 的过硫酸铵水溶液,酸化剂是 6 摩尔磷酸水溶液。Sievers 认证的 TOC 40 mL 样品瓶用于收集 40 mL 及以下的馏分。将较大的馏分收集在选定尺寸的Durans玻璃中以减少顶部空间,用 10% v/v 硝酸溶液和纯净水进行预冲洗。这些在使用前进行了预测试。使用前确保所有玻璃器皿的浓度低于 0.05 mg/L。制备浓度均为 500 ppb 的 1,4-苯醌和蔗糖溶液,并使用样品溶液进行分析,以确保测量的准确性。在过滤器冲洗前,用于 TOC 的水的测量值小于 0.05 mg/L。
顶空气相色谱质谱法 (HS GC-MS)
使用装有能够进行顶空分析的 Gerstel MPS 的 Agilent 8890 气相色谱仪和质谱仪分析水馏分的等分试样的挥发性物质。使用分流模式(比例 5:1)。载气为恒定流速为 1 mL/分钟的氦气。使用 DB624,60 m x 0.25 mm x 1.4 µm 膜厚分析柱,温度梯度为 35 °C 至 240 °C,历时 45 分钟。质谱仪在扫描模式下使用 m/z 30–500 范围和 5 分钟的溶剂延迟运行。在 80 °C 下以 500 rpm 的搅拌速度孵育 60 分钟。单个挥发性物质的半定量基于内标添加,在本例中为甲苯-d8(99.6%,Sigma-Aldrich)。对于每个样品制备,将 1 g ± 0.1 g 氯化钠(≥ 99%,Sigma-Aldrich)放入 10 mL 顶空钳口瓶中,然后加入 1.0 mL 去离子水和 20 mcL 浓度为 80 mcg/mL的内标。使用 1000 mcL 的注射体积。
气相色谱质谱法 (GC-MS)
使用配备 Gerstel MPS 的 Agilent 7890 气相色谱仪和质谱仪分析等份的水馏分的半挥发性物质。脉冲不分流,初始进样脉冲压力为 15 psi,持续 1 分钟,1 分钟后吹扫至分流口的流量为 50 mL/min。前入口温度设置为 300 °C。载气为氦气,流速恒定为 1 mL/min。使用 HP1,50 m x 0.32mm x 1.05 µm 膜厚分析柱,温度梯度为 60 °C 至 300 °C,历时 24 分钟。质谱仪在扫描模式下运行,使用 m/z 30–500 范围和 6.5 分钟的溶剂延迟。单个半挥发性物质的半定量基于内标添加,在本例中为芴-d10(≥ 99%,Sigma-Aldrich)。对于每个样品制备,将 1.0 mL 去离子水和 20 mcL 80 mcg/mL 内标置于玻璃离心管中。然后使用氯仿(99.9%,ACROS Organics)作为萃取溶剂对所有制剂进行分散液-液微萃取(DLLME)。使用 1 mcL 的注射体积。
结果和讨论
TOC
与通过过滤器后的水样中所见的水平相比,管路中的 TOC 水平最低 (0.06 mcg/mL)。来自过滤器的样品中的 TOC 水平未针对来自管路的 TOC 水平进行校正,并且被认为是最坏的情况。图 1 显示了获得的数据。
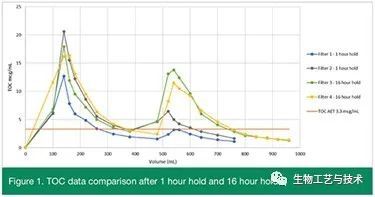
图 1 中过滤器冲洗曲线上的数据点代表样本收集点。额外的累积馏分 800 mL、840 mL、880 mL、920 mL 和 960 mL 仅通过过滤器收集并保留 16 小时,并显示 TOC 水平进一步降低。
过滤器之间存在一些差异,但是所有四个过滤器都遵循相同的趋势。保持 20 分钟并开始冲洗后,TOC 水平在前 100 mL 中增加。在模拟管路体积的 140 mL 冲洗后,TOC 水平达到最大值,之后水平再次下降。在用 380 mL 冲洗后和保持之前,所有过滤器的 TOC 水平不超过 3.3 mcg/mL 的 AET。在保持并再次冲洗过滤器后,TOC 水平再次增加到大于 3.3 mcg/mL,随后 TOC 水平下降。保持 1 小时后过滤器冲洗中的最大 TOC 水平低于保持 16 小时后过滤器冲洗中的最大 TOC 水平。这些数据证实了在之前的研究中已经观察到的情况,其中显示大约两倍的过滤器死体积已经包含过滤器释放的 TOC 的 50-70%。
此外,与 16 小时保持相比,1 小时保持将 TOC 水平降低至不大于 3.3 mcg/mL 所需的冲洗量更少。第一次保持后,在 140 mL、160 mL 或 180 mL 冲洗馏分中检测到最高 TOC 水平,表明可析出物积聚在过滤器上,而不是过滤器后的 140 mL 管路中。当生产过程继续进行时,可析出物会在过滤器中积聚并被冲出过滤器。还表明,过滤器的 TOC 水平是多种可析出物的总和,这些可析出物在过滤器冲洗过程中缓慢释放成累积馏分。
TOC 分析检测所有含碳化合物,并指示可析出物的总量。TOC 可以在这里应用,作为一种快速筛选工具,并且使用比通常静态的可溶出物研究更温和的条件。
挥发性和半挥发性物质
在 TOC 分析完成后,对单个挥发性和半挥发性物质进行了筛选。使用相同样品的不同等分试样。选择具有最高 TOC 水平的选定馏分作为最坏情况进行分析。
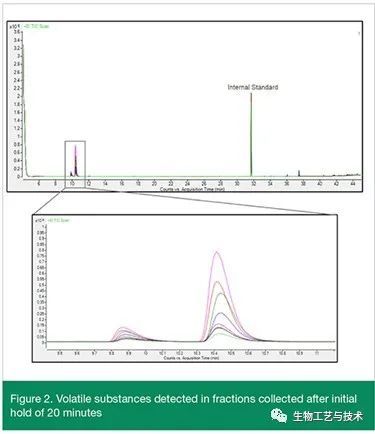
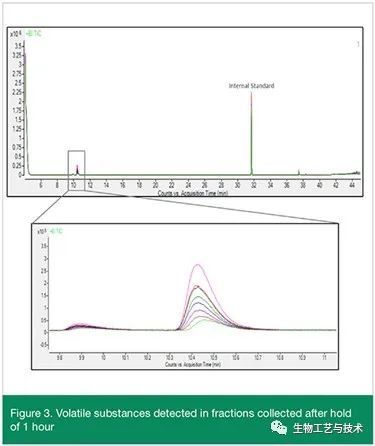
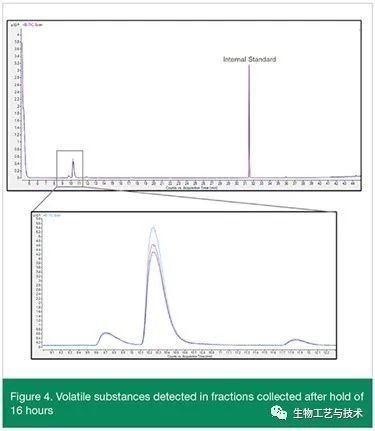
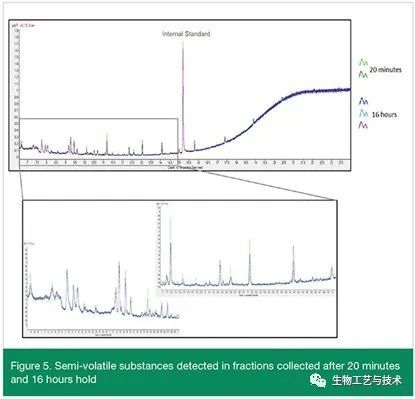
图 2、图 3、图 4 和图 5 显示了初始保持 20 分钟、1 小时和 16 小时后从过滤器收集的馏分的叠加色谱图。上图显示了叠加色谱图和内标,所有峰均不超过 1.6 mcg/mL。下图显示了灰色方块的扩展色谱图,并表明相同的峰出现在多个累积馏分中,表明物质分布在多个 1 mL 注射器中。
挥发性和半挥发性物质的筛选表明,在初始保持 20 分钟、1 小时和 16 小时后,挥发性和半挥发性物质的水平不超过 1.6 mcg/mL AET。色谱图中存在多个峰表明多个潜在的可析出物可以从过滤器中析出,并且在几个累积馏分中检测到的峰表明物质不会最终出现在单个 1 mL 注射器中,而是分布在多个注射器中。
总结
在这项研究中,TOC 已被证明是一种有价值的筛选和分析可析出物的工具。
尽管在最初的 20 分钟、1 小时和 16 小时保持后的累积馏分中 TOC 水平大于 3.3 mcg/mL,但单个物质的水平不超过 1.6 mcg/mL 的 AET,强大的冲洗策略实现了最终过滤器下游没有产品合并的工艺。
在目前的生产过程中,在最初的 20 分钟保持后,至少有 380 mL 的药品被丢弃,这降低了患者暴露于大于 3.3 mcg/mL 的可析出物的风险,其中大部分可析出物被丢弃。这表明过滤器在用于生产过程之前始终进行冲洗是多么重要,因为在过滤器冲洗过程中存在的化合物水平会降低。
如果没有这项过滤器冲洗研究,则必须按照供应商的建议使用超过 1 L的默认冲洗量。设置的 380 mL 体积超过推荐体积的一半。
过滤器中可析出物的潜在安全风险与生产过程中的过滤器冲洗方案相结合被证明是低的,并且确定了过滤器冲洗的最小体积,以确保工艺优化。
原文:J. Marques, P. Booij, R. Collier, flush studies to review the leachable safety risk of a filter in the drug product manufacturing process. Biopharm Asia, 2022.
内容来源:生物工艺与技术
责任编辑:胡静 审核人:何发
邵丽竹
何发
热点文章
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
微生物发酵技术在植物活性成分提取中的应用研究进展
2026-03-06
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多