新药 | γ分泌酶抑制剂研究进展:Nirogacestat递交治疗硬纤维瘤的NDA

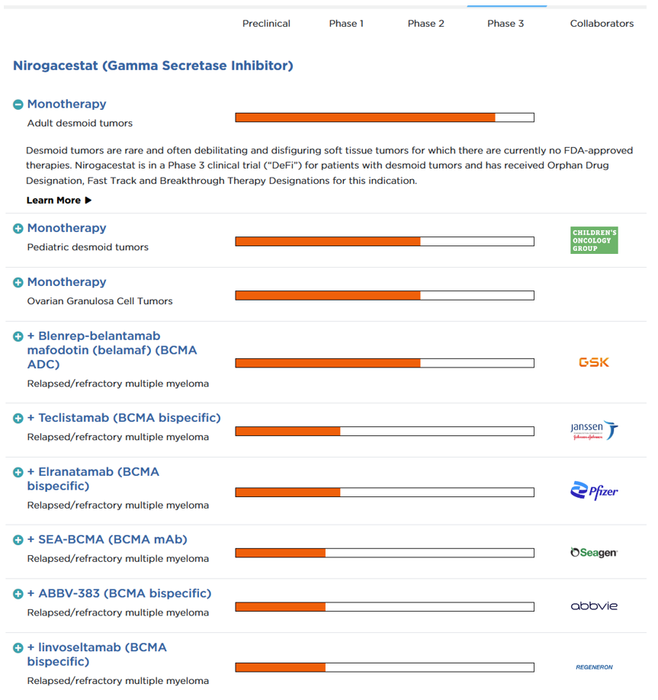
Nirogacestat是一种口服、选择性、小分子γ分泌酶抑制剂,被开发单药治疗成人/小儿硬纤维瘤和卵巢颗粒细胞瘤,以及联合BCMA靶向药治疗复发或难治性多发性骨髓瘤。γ-分泌酶能够切割多种跨膜蛋白复合体,其中包括Notch蛋白,而Notch蛋白被认为能够激活导致硬纤维瘤生长的信号通路。
此前,Nirogacestat曾被FDA授予治疗硬纤维瘤的孤儿药资格认定(2018/06)和治疗进行性、不可切除的、复发性或难治性硬纤维瘤或深部纤维瘤病成人患者的快速通道和突破性疗法资格认定。
Nirogacestat的NDA提交资料根据FDA的实时肿瘤审查 (RTOR) 项目进行审查,包括3期临床试验DeFi的数据。DeFi是一项全球、随机、双盲、安慰剂对照试验,试验中142例受试者(Nirogacestat,n = 70;安慰剂n = 72)每日接受2次150 mg Nirogacestat或安慰剂治疗,主要终点是每个盲态独立中心阅片的无进展生存期(PFS),预设的次要终点是安全性、客观缓解率(ORR)和患者报告结局(PROs)。
2022年ESMO上公布的结果显示:经盲法独立中心审查,与安慰剂相比,Nirogacestat组患者的PFS显著改善。此外,与安慰剂相比,Nirogacestat组的ORR显著改善(41% vs 8%;P<0.001),中位缓解时间为5.6个月(Vs11.1个月)。Nirogacestat组的CR率为7%(Vs 0%)。而且,与安慰剂相比,使用Nirogacestat早期和持续治疗中观察到所有预设PRO的统计学和临床指标均有显著改善
安全性方面,Nirogacestat治疗的不良事件中95%为1/2级,其中最常见的是腹泻(84%)、恶心(54%)、疲劳(51%)、低磷血症(42%)和斑丘疹(32%)。
硬纤维瘤是一种罕见的局部侵袭性软组织肿瘤,通常会使人衰弱和毁容,并能侵袭周围的健康组织,引起严重病态,包括剧烈疼痛、内出血、关节活动能力丧失,罕见情况下甚至导致死亡。据估计,美国每年有1000-1500名新诊断硬纤维瘤病例。目前,FDA还没批准系统治疗硬纤维瘤的药物。
若顺利,Nirogacestat有望成为FDA批准的首款治疗硬纤维瘤的γ分泌酶抑制剂。除治疗硬纤维瘤,Nirogacestat还被开发治疗多发性骨髓瘤(MM)。这是由于γ分泌酶可直接裂解膜结合 B 细胞成熟抗原 (BCMA),导致细胞表面释放 BCMA 胞外域 (ECD)。通过抑制γ分泌酶,可以保留膜结合的BCMA,增加靶密度,同时降低可溶性 BCMA ECD 的水平,其可以作为 BCMA 定向治疗的诱饵受体。
Nirogacestat已在MM临床前模型中表现出增强BCMA靶向治疗活性的能力。目前,SpringWorks已先后与多家行业领先的BCMA靶向药开发公司合作,评估Nirogacestat作为BCMA增效剂治疗复发或难治性MM的潜力。
此外,目前全球还有多款在研γ分泌酶抑制剂(详见下表),其中AL102治疗硬纤维瘤的临床试验已进入3期临床。2022年ESMO上公布的AL102治疗硬纤维瘤2/3期临床试验结果显示:AL102所有剂量组均有疗效,且早期肿瘤应答程度随着时间的推移而加深。

AL102 和AL101由BMS开发,2017年12月Ayala公司这两款药物的全球开发和商业化权益。2018年12月,诺华与Ayala公司就AL102 达成了一项许可协议。据协议,Ayala公司获得诺华1000万美元的股权投资,诺华则有资格获得开发、临床、监管和商业化AL102的权利,以及AL102净销售额的分层特许权使用费。而AL101是一种用于肿瘤适应症的Notch基因突变抑制剂,专门针对抑制γ分泌酶,目前治疗携带Notch基因激活突变的腺样囊性癌(ACC)临床试验已进入2期临床。
除治疗硬性纤维瘤、MM等肿瘤,γ分泌酶抑制剂还有望用于治疗感音神经性听力损失、阿尔茨海默病。
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多