韩国制药行业掠影
近几年,随着全球新冠疫情的爆发,全球供应链危机持续发酵,制造业受到较大的冲击。制药产业虽然也受到疫情影响,但这同时也是制药业发展的机会。近年来韩国制药产业发展迅猛,制药、生物产业也正在慢慢成为引领韩国经济的未来主力产业,据韩国产业通商资源部发表的《2021年全年进出口动向》中的数据显示,2021年韩国医药品出口额为84.9亿美元,同比增长20.5%,其增长势头领先于其它任何行业,不容小觑。
韩国CRO市场
韩国CRO(医药研发合同外包服务机构)市场发展迅速,是亚洲临床试验研究发展最快的国家之一,韩国政府为了建设世界一流的临床试验基地,扩大临床试验能力,提高临床研究专业人员的能力,对临床试验基础设施进行了大量投资,韩国已经成为国际多中心临床试验的一个中心。下面我们来通过一组数据了解一下:
韩国2017-2019年批准的临床试验数量对比
年份 |
2017 |
2018 |
2019 |
数量 |
658 |
679 |
714 |
全球2017-2019年新注册的临床试验数量对比
年份 |
2017 |
2018 |
2019 |
数量 |
7865 |
8386 |
8196 |
2019年韩国批准的临床试验数量为714项,比2018年(679例)增加5.2%,比2017年(658例)增加8.5%;另一方面,2019年全球新注册的临床试验数量达到8196个,与2018年(8386例)相比下降了2.3%。这些数据显示,与全球临床试验的增长趋势相反,在过去几年内韩国批准的临床试验数在稳步增长,而且国内临床试验能力得到了极大的提高。
同时,韩国拥有透明的监管体系,其国际多中心临床试验中心受到全球多国家的青睐,许多主要的国际临床研究机构和制药公司都在韩国开展临床试验工作,开展的临床试验数量也居全球领先水平。
韩国著名药企
韩国大型药品生产企业主要有东亚制药、韩美制药、大熊制药、柳韩洋行(Yuhan)、富光制药、绿十字、韩国科玛、钟根堂、Celltrion、三星生物等。
韩国东亚制药株氏会社(Dong-A制药):韩国最大的药品生产和贸易集团,成立于1932年,总部位于韩国首尔,迄今已有90年的历史。公司主要从事医药产品和医疗器械的研发、生产和销售,生产产品包括处方药、非处方药、健康消费品、生物制品、原料药和医疗器械等;
韩美制药:韩国第二大制药企业,总部位于韩国首尔,是一家国际性制药企业,目前门诊处方量和研发投入在韩国均排名第一。公司致力于研发创新型药物,产品管线丰富(图1),研发投入资金占营收比例超过了15%(图2)。公司有完善的药物研发和生产平台,并且拥有韩国最大的药物研究中心,在糖尿病持续给药领域以及肺癌领域都获得了重大突破。公司以长效蛋白、多肽药物技术和口服药物技术为核心,重点开展肿瘤、自身免疫病和代谢紊乱的生物药、化学药及多肽药物研发,在抗生素、心血管、消化、抗肿瘤、儿科等多个领域均居于全球先进地位。
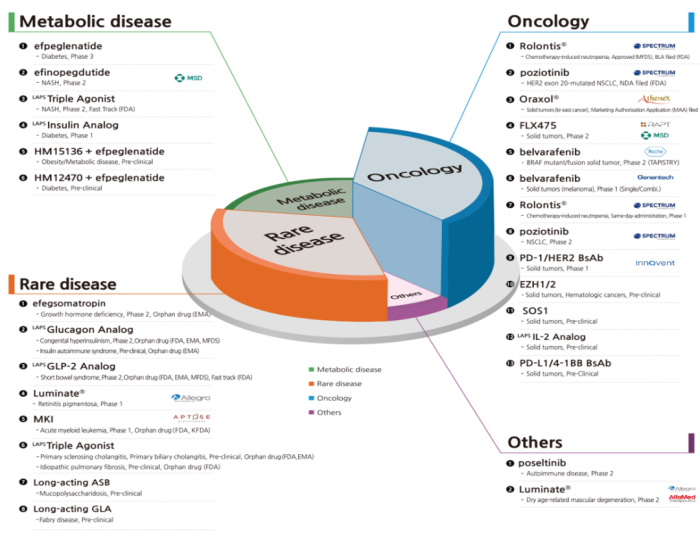
图1 韩美制药研发管线(图片来源:韩美制药官网)
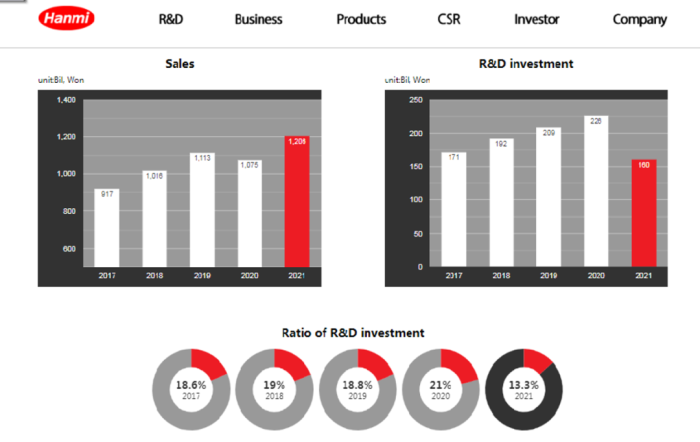
图2 韩美制药历年来研发投入占比(图片来源:韩美制药官网)
大熊制药(Daewoong 制药):韩国国内最大的处方药企业集团,成立于1945年,总部位于韩国首都首尔。大熊制药一直致力于研发、生产、销售和布局能改善全球健康的创新药物,具有丰富的产品线。大熊制药在处方药和OTC药品生产、化学合成、药物释放技术、IT解决方案等方面都占有举足轻重地位,公司多个产品在FDA注册,原料药出口到40多个国家和地区,详情可参阅《药企观察/太极旗下的大熊制药》一文。
柳韩洋行(Yuhan) :柳韩洋行(Yuhan)是韩国的一家制药和化工企业,创立于1926,致力于解决各类流行疾病,连续20年被评为韩国最受尊敬的企业。公司始终强调研发在企业运营中的重要性,针对目前市场上极具需求的领域集中力量投入研发,特别是在炎症、自体免疫类疾病、癌症以及代谢疾病的对应治疗方法方面,积累了专业知识和丰富的经验。另外公司可提供从原料药和医药中间体的研发到商业化生产的一站式定制合成生产服务,成为国际制药市场的优秀合作伙伴。
近年来韩国从政府政策、审评审批、监管环境以及产业发展等方面多方位大力支持生物制药产业,目前韩国生物医药产业在全球占据重要地位, Celltrion和三星生物(SamsungBioepis)已经成为生物医药领域的佼佼者。
2003年5月韩国食品药品管理局(KFDA)首次发布《生物制品审评与批准条例(MFDS通知)》,目的是确保产品批准和审评的适合性,对审查安全性和有效性、规格和分析方法、标准和要求制定详细的程序,并根据《药事法》、《医药品等安全相关的规则》对生物类似药的制造、销售和变更事项给予批准,该条例至今已修订了二十余次。
2009 年6 月,韩国食品药品安全部(MFDS) 参照WHO指南以及EMA指南发布了第1 个生物类似药指南《生物类似药评估指南》,作为总体性指南,于2010 年生效。此后,基于生物类似药的研发、相关的临床和管理经验以及全球监管协调,不断在修订现有指导原则的必要性上达成共识,并陆续发布了多个辅助性专项指南。
2014年,韩国政府制定了《生物制药产业的前景及发展战略》,确立了Bio-Pharma 2020核心课题和各领域的具体课题,其中有针对生物类似药/Biobetter领域的多个课题。
2015 年10 月韩国药政当局发布了新版《生物类似药评估指南》。
Celltrion公司:韩国最大的生物制药公司,也是目前全球第二大单克隆抗体生产企业,全球生物制药领先公司。公司总部位于韩国仁川,始建于2002年,并于2008年成功上市。公司主要业务是生物类似药,新型生物制剂和CMO。公司不仅为欧美大型的制药公司从事研发和生产外包的业务,同时自己也投入大量资金进行生物药以及化学药品的研发。2013年9月Celltrion向全球市场首个推出英夫利昔单抗类似物(Remsima)的抗体生物类似药,是全球首家开拓出"抗体生物仿制药"的公司,获得了全世界的瞩目。2017年2月Celltrion又推出了首 个利妥昔单抗类似物(Truxima)。2018年2月,Celltrion的曲妥珠单抗类似物(Herzuma)获批上市,这是全球第二家获批上市的生物类似产品,首家上市的是来自韩国的三星生物(SamsungBioepis)。
三星生物(SamsungBioepis):三星生物成立于2012年,致力于高品质生物仿制药的研发创新。公司虽然起步较晚,但在免疫和肿瘤生物类似药产品线的研发、生产和全球注册方面已经卓有成效。另外,公司注重联合发展道路,Samsung Bioepis先后与Biogen、默克、BMS等多家跨国企业都签订了合作协议,开发和商业化多个生物类似药。详情可参阅《进军中国大陆市场!三星Bioepis的生物仿制药之路》。
参考资料
1-韩国MFDS官网MFDS's Operation of Clinical Trial Authorization and Safety Management
2-美国国立卫生研究院临床研究数据库(www.clinicaltrials.gov)
3-韩美制药官网
4-柳韩洋行官网
作者简介:zhulikou431,高级工程师、PDA会员、ISPE会员、ECA会员、PQRI会员、资深无菌GMP专家,在无菌工艺开发和验证、药品研发和注册、CTD文件撰写和审核、法规审计、国际认证、国际注册、质量体系建设与维护领域,以及无菌检验、环境监控等领域皆具有较深造诣。近几年开始着力关注制药宏观领域趋势分析和制药企业并购项目的风险管理工作。
来源: CPhI制药在线
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多