仿制药立项全攻略之原料药基本情况调研

(图片来源于网络,侵权删除)
这么重要的原料药好像在之前调研的时候我们都没有怎么好好在乎过,找个资质齐全的厂家买一个不就齐活了么?那为啥现在要单独拿出来强调?
因为现在情况不一样了!
集采前
作为药品的上游,原料药企的日子并不光鲜,工作辛苦,工作环境差,每天面对的危险的高压反应釜和海量的高毒的化学试剂,做出来的产品也是任人挑选,真是操着卖白粉的心,赚着卖面粉的钱,简直就是高学历的民工,一点不像个化学家!
集采后
集采对供应量和供应速度的硬性要求,原料药企业的地位实现了逆袭,因为原料药而导致的集采断供和亏钱,大家都知道,笔者就不多说了。
所有制剂企业对上游原料药企态度上有了质的变化:以前是财大气粗,买方就是上帝,对于原料药公司随便挑;如今找到一家靠谱的公司就恨不得签个长期合作协议,因为买不到原料或者原料涨价,对于集采保供的企业是致命的。
当然,也有些不愿意被人“卡脖子”的制剂企业意识到了原料药的重要性,纷纷走上了原料药和制剂一体化的道路。
建设自己的原料药生产线或基地:
京新药业斥资40亿元在山东新建原料药、医药中间体为主的生产基地;
复星医药在常德投资建厂;
海辰药业在安庆投资建厂;
珠海润都在荆门投资建厂;
奥翔药业、昂利康、广生堂和富祥药业,在2020年先后抛出了非公开发行再融资扩产原料药的预案。
收购原料药企业:
康惠制药以3264万元收购原料药企业;
金达威以3亿元收购原料药企。
对于我们制剂厂家的立项人员,调研的前提是一定要对以上大环境有足够清晰的认知,才能写出靠谱的报告。
如果为一个新的制剂项目做原料药调研报告,我们一般从以下几个方面进行调研,并结合自家的情况进行考虑。
从下游制剂所处生命周期来看,原料药可以分为专利原料药、特色原料药和大宗原料药三类。
专利原料药
主要对应的是专利保护期内药品。
合作模式一般是由制剂厂家自行生产或以合同定制方式委托专业原料药公司进行生产。
这类产品利润率高,需要较强的研发能力。受委托的原料药厂通常自临床前或临床阶段已经介入研究了,开发合成路线并提供临床试验批次,在产品上市后会成为该专利药品的核心原料药供应商。此种情况下,专利药企业和原料药企业的合作关系一般较为稳定, 且通常会拓展合作项目。
特色原料药
主要对应专利保护期过后较短时间药品,利润率仍可维持在较高水平,仅少数企业可进行生产。
特色原料药的研发通常在专利到期前5-6年即已开始,除仿制药企业或原料药企业自行研发生产外,仿制药企业经常与原料药企业合作进行首仿抢仿,以在专利到期的时间窗口内及时进行注册申报并上市销售,从而获取更大市场份额。此种情况下,仿制药企业和原料药企业关系相对紧密。
大宗原料药
主要对应专利保护期过后较长时间药品,产品利润率低,但需求量较大,市场竞争激烈, 成本控制是核心竞争力之一。一般需要具备规模化优势,与下游客户合作关系较为松散, 主要通过市场化渠道销售。
作为立项人员的第一任务,一定是搞清楚自己调研的原料现在处于哪种阶段,当前国内的产能如何。
下面我们以瑞舒伐他汀钙为例,看一下立项调研需要注意的问题。
瑞舒伐他汀钙首年集采基数换算成原料药不到5吨,再分摊到3家中标企业头上仅3.5吨。而中国2018年出口瑞舒伐他汀钙原料药及高级中间体超过20吨,产能远远高于上述需求,而多出的产能还需要国外市场来消化,全球年需约150吨的瑞舒伐他汀钙原料药,这基本上是由中印两个国家来生产。
如果说你正在调研的原料药,是上述这个样子,哪怕目标是奔着集采去的,也没有必要再投入高额的成本进行自研,不如找个靠谱的原料药供应企业多签几年合同,皆大欢喜。
如果是国内产能本就不足,或者质量很难保证的原料药,在研究和生产难度适合本企业的情况之下,则值得投入成本进行研发,除了和自己家制剂形成原料制剂一体化的优势,说不定还能创造出一块额外的收入。
这部分数据的调研一般情况下不太容易。
需求相对好计算,根据集采所公布的采购量或者国内样本医院销量的放大数据再加上规格,一算即可得出。
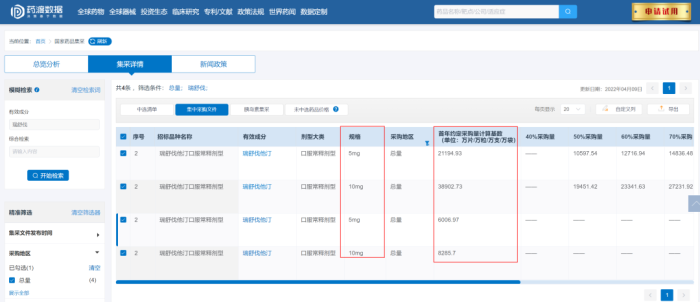
图片来源:药渡数据库
但是,产能一般就不太好预测了,请原谅笔者在这方面也不太专业(公司舍不得购买相应数据库),所以一般数据来源于一些行业报告,实在搞不定的就只能从上市批准的企业数进行大概的推测了。

图片来源于网络,侵权删除
无论是想自研调研竞争对手的情况,或者是想找个靠谱的供应商,本步骤都不能省略。
但是查起来也简单,基本上查一下原辅包信息登记平台和CDE注册申报信息即可得到。
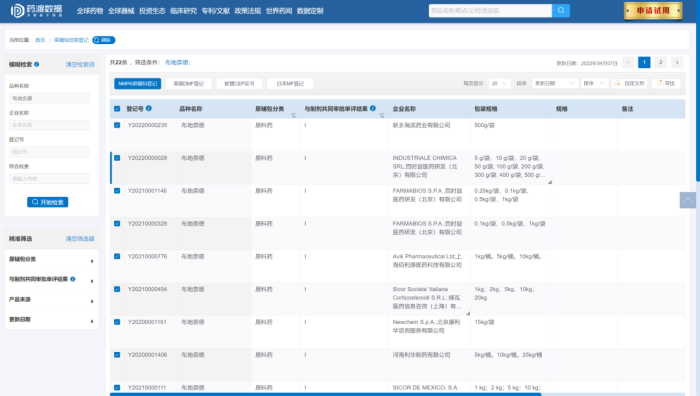
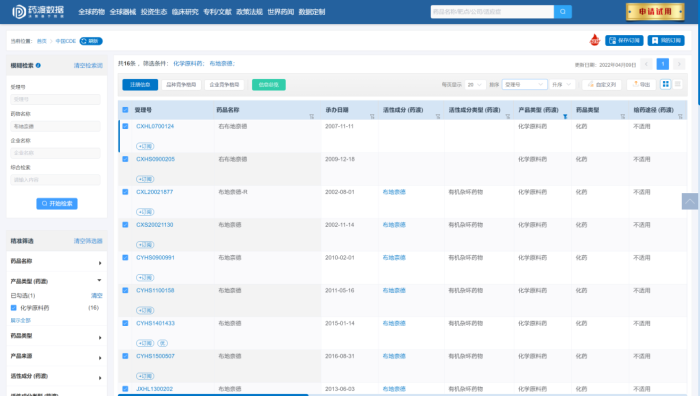
除了已经经过DMF注册的原料药,还有大量化工品,如果想找供应商的话,还可以提前找一些供应商进行询价,并进行价格对比。
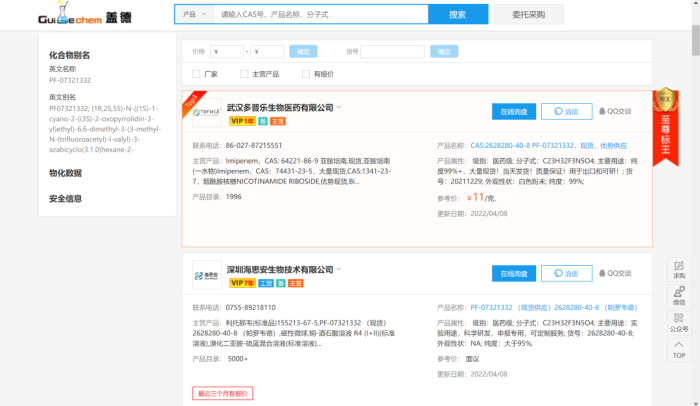
图片来源:盖得化工网
除了在中国原辅包信息登记平台的备案情况,在美国DMF登记和欧洲CEP和日本MF的登记情况也需要进行调研。
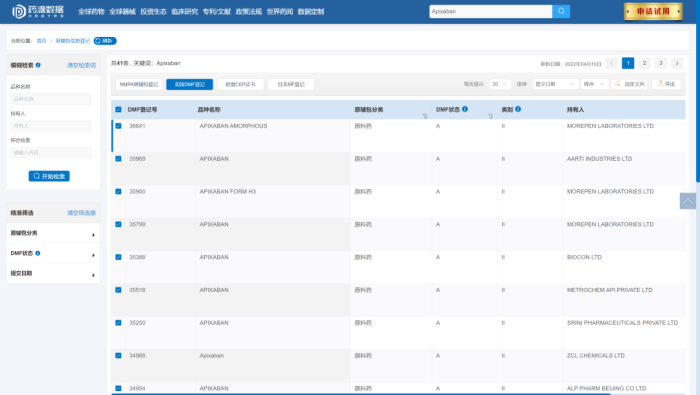
图片来源:药渡数据库
03原料药的质量和工艺情况
如果想确定原料药自研的难度,我们需要查原料药的质量标准,确定原料药的工艺难度等,这个相信大家都非常熟悉,笔者就不做过多介绍了。
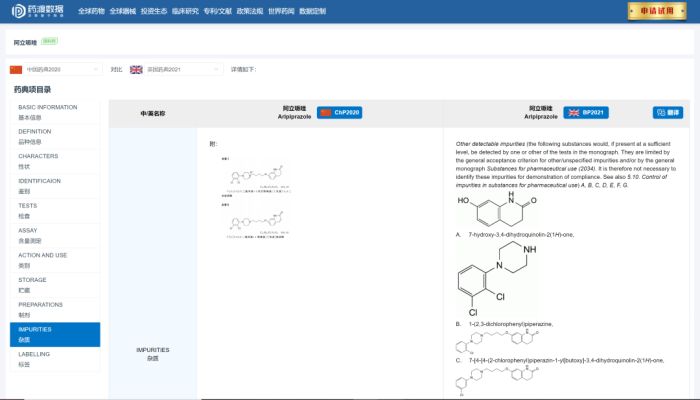
药典杂质对比-来自药渡数据库
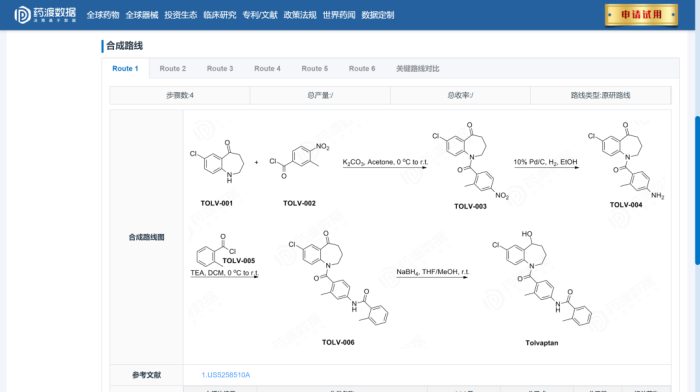
原研路线及其文献的查询-来自药渡数据库
结合自家生产线情况和所调研原料的产能情况和备案情况,即可对原料药情况进行初步的判断。
本文来源于药渡仿制
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多