线性pH梯度在单抗领域的应用
如何对现有提纯技术进行优化升级,或者寻求一种高效的新方法作为补充,是业界研发人员重点研究的领域——在业界,线性pH梯度一直是难以攻克的课题,因为普通的酸碱溶液混合,不是线性呈现的。它在pH值5.5~8.5的区间不受控制,形成S形的快速变化的曲线。这样的跳变使线性pH梯度无法形成,也就难以进行广泛地研发和应用测试,线性pH梯度相对于盐梯度的优越性一直没有被生物制药领域发现和深度开发。
文/ 刘德宇,李国荣
药用蛋白质的下游制备通常是用盐梯度溶液作为流动相,通过层析柱来分离蛋白质及其杂质。这种基于离子交换色谱柱(IEC)的层析法,是生物制药下游生产中一个不可缺少的加工步骤。它的原理是通过逐步增加缓冲液的盐浓度,减少离子介质与蛋白质之间的相互吸引,使不同的蛋白质根据盐浓度的不同先后分离,从而相继洗脱出来。
单抗(mAb)的下游提纯同样采用层析法,流动相也是盐溶液,Protein A是单抗提纯方法首选的亲和填料,已经在实际生产中应用了30年之久。使用Protein A和盐梯度提纯单抗的工艺方法是成熟的,但是其客观存在的缺点也被大家所熟知,比如工艺复杂、步骤繁琐等不利因素。首先,Protein A填料价格昂贵而且被国外少数供应商垄断,致使制药企业的生产成本较高。其次,因为仿制药没有专利保护,导致国内生产厂家之间竞争激烈,企业盈利情况不容乐观。再次,如果有一天,国外Protein A供应商因国家之间发生贸易战争或其他不可抗力,停止向中国的生物制药公司出售Protein A,或者以任何理由大幅提价,你是否不寒而栗?面对以上不可预测的突发状况,需要大量Protein A的制药厂,是否会被迫停止生产?谁又能保证这样的极端情况永远不会发生?
如何对现有提纯技术进行优化升级,或者寻求一种高效的新方法作为补充,是业界研发人员重点研究的领域。
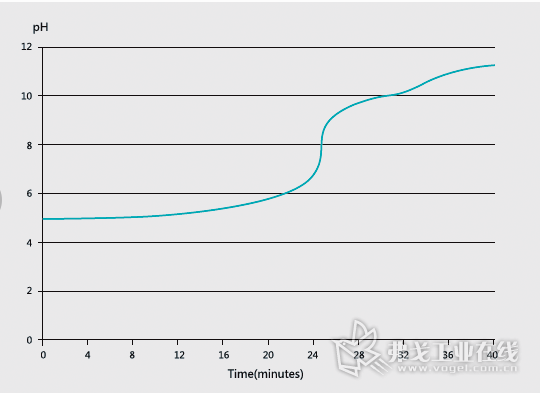
图1 普通酸碱溶液的混合pH值在5.5~8.5区间不受控制
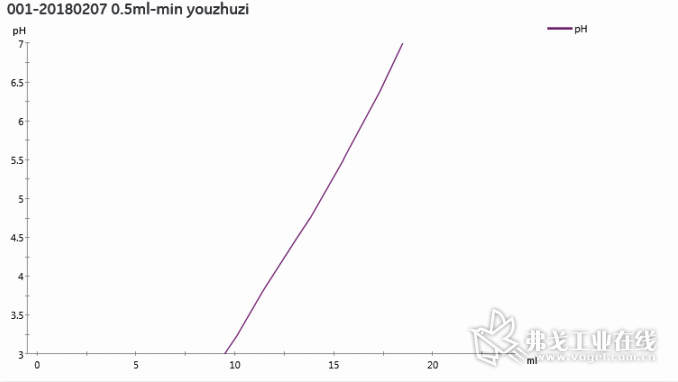
图2a 苏州美极MJB001,线性pH 3~7梯度缓冲溶液(GE AKTA Pure,0.5 ml/min)
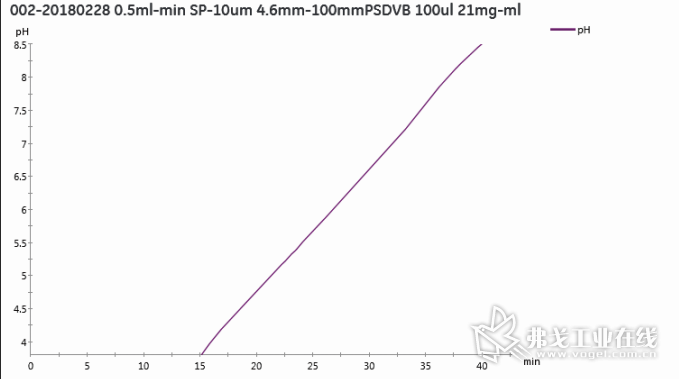
图2b 苏州美极MJB002,线性pH 4~8.5梯度缓冲溶液(GE AKTA Pure,0.5 ml/min)
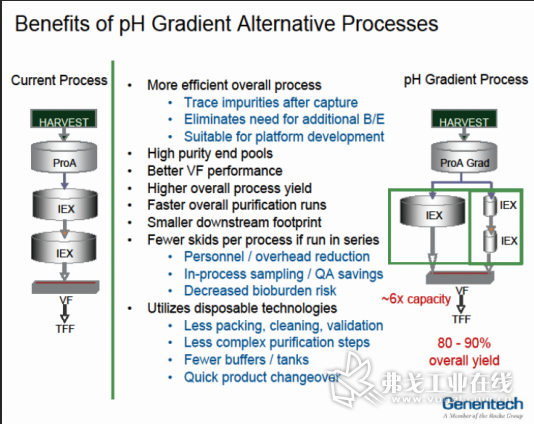
图3 线性pH梯度工艺应用于生物制药下游
研究课题的新方法
在业界,线性pH梯度一直是难以攻克的课题。因为普通的酸碱溶液混合,不是线性呈现的,它在pH值5.5~8.5的区间不受控制,形成S形的快速变化的曲线(如图1)。这样的跳变使线性pH梯度无法形成,也就难以进行广泛地研发和应用测试,线性pH梯度相对于盐梯度的优越性一直没有被生物制药领域发现和深度开发。
经过不断的研发,苏州美极医疗科技有限公司配制出了多款性能稳定的线性pH梯度缓冲溶液(如图2a和图2b)。
最近,Genentech(基因泰克)的一项研究发现,与传统的盐梯度结合/洗脱平台相对比,线性pH梯度不仅可以降低产品中的杂质含量,而且可以提高下游工艺的效率(如图3所示)。此外,从单克隆单体中分离二聚体和聚合体的线性pH梯度工艺,可以从实验室规模扩展到中试规模(如图4所示)。在中试规模的实验中,回收率为86%,纯度为99.3%,对比实验室88%的回收率和99.2%的纯度,其结果是非常积极和令人鼓舞的商业化扩大。
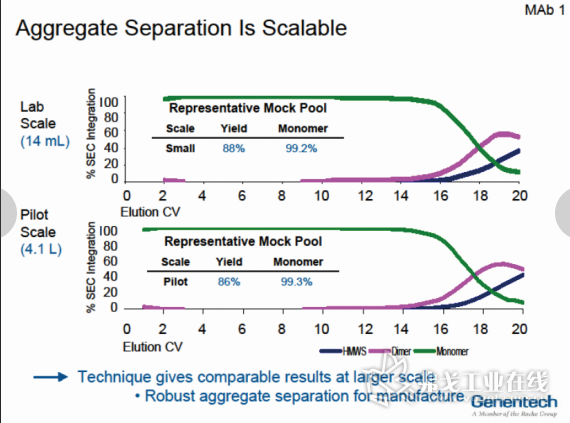
图4 从实验室规模扩展到中试规模mAb,二聚体和聚合体分离
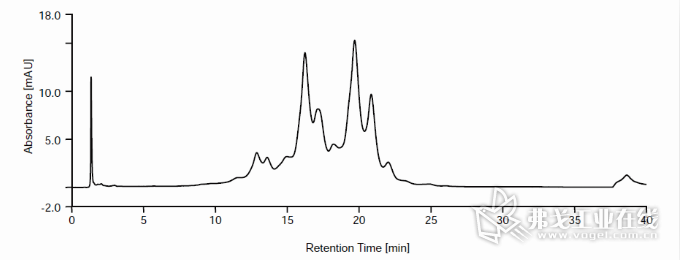
图5 mAb盐梯度洗脱elution:84 mM to 132 mMNaCl,30 minutes,1.6 mM/min
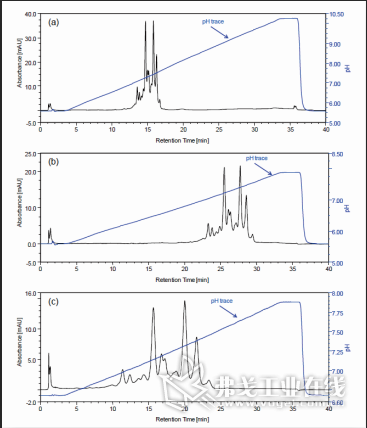
图6同一个mAb样本在 3种范围不同的线性pH梯度洗脱
几乎同时,美国的赛默飞世尔(Thermo Fisher)科技公司也做了很多关于线性pH梯度缓冲溶液的实验,证明了线性pH梯度的优越性。其中一个研发实验,证明了线性pH梯度缓冲溶液在分离提纯中可以替代盐梯度溶液,具有更好的分离效果。效果验证如下:
把粗杂的单克隆抗体样本装入阳离子柱中,分别使用盐和线性pH梯度分离的结果对比(如图5和图6)。传统盐梯度分离效果并不理想,单抗变异体(variants)峰宽而且重叠(84 mM到132 mM氯化钠,1.6 mM/min,30 min,见图5);反之,线性梯度pH 6.75~pH 7.9,在相同时间内,洗脱效果较好。(如图6c,实验数据表明分离峰窄,重叠峰分开, 效果明确比盐好。)这个实验可以有效验证:
① 不需要Protein A,阳离子填料也可以分离单抗及其变异体(variants)。
② 线性pH梯度的分离效果比盐梯度更好。
③ 很多细节只能从线性pH梯度分离中突出。
在过去的2年中, 很多公开发表的科学论文阐述了只用阳离子填料和线性pH梯度提纯单抗(mAbs)的可行性和优越性。赛默飞的另一个研发实验,是以线性pH梯度作为分离平台进行的高分辨率质量检测,使用pH 5.5~10.2的线性梯度和阳离子填料,分别对Rituximab、trastuzumab、adalimumab 和 bevacizumab共4个已经被美国FDA批准销售的单抗样本进行测试,取得了令人满意的结果。以Rituximab为例,线性pH梯度缓冲溶液表现出了比传统盐溶液对样本更好的分离性能,使难分离的杂质显露出来(如图7a和图7b所示)。
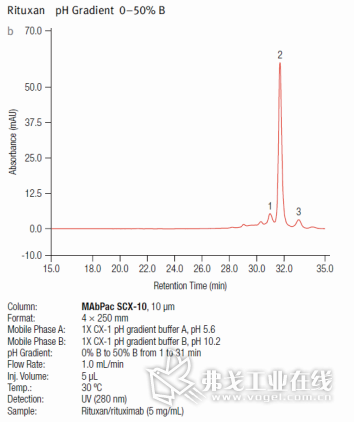
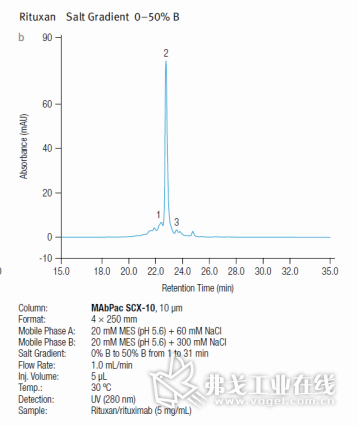
图7a单抗Rituan在线性pH梯度的分离结果 图7b 单抗Rituan在盐溶液的分离结果
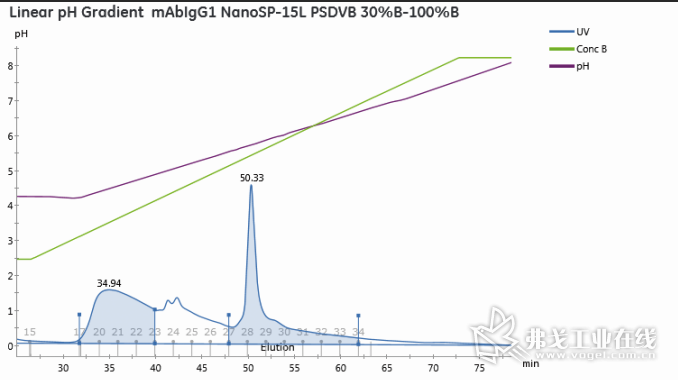
图8 线性pH 4.3~8.0梯度缓冲溶液和国产阳离子填料,提纯出单抗
应用实验
针对医药界提纯技术的升级优化,苏州美极也进行了相应的研究,在苏州纳微科技有限公司金百胜、黄帮友的协助下,用线性pH梯度作为流动相,配合纳微阳离子填料而不使用Protein A进行单抗层析实验(如图8)。
美极的中试分离实验
把两种蛋白质Trypsinogen 和 Ribonuclease A,pI相近但是不同,分别为7.6 和8.5, 混合在一起装入在阳离子交换柱中,分别用线性pH梯度缓冲溶液和非线性缓冲溶液进行分离。
试验结果:
(蓝线)非线性缓冲液, pH值从5.5不可控制的跳变到8.5,两种蛋白质几乎在同一时间洗脱出来,无法分离,其纯度和效率很低(如图9所示)。
(红线)美极的线性pH梯度,使这两种蛋白质被基线分离,确保了非常好的回收效果。(如图9所示)。
实验分析:因为两种蛋白的pI值与pH值存在相关性,如果没有合适的缓冲溶液,线性pH梯度不能形成,Trypsinogen 和Ribonuclease A 便不能在适当的pH下分离出来。
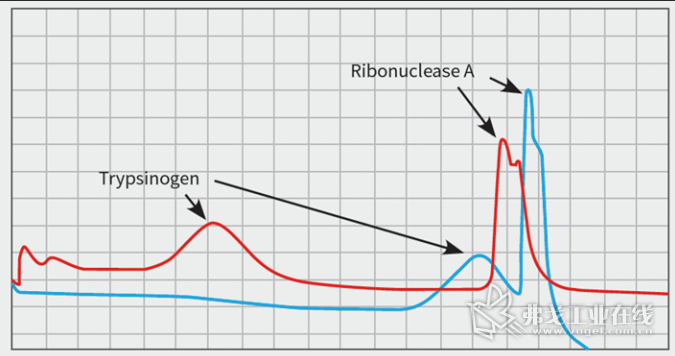
图9两种pI相似的蛋白分离结果对比,红色:线性pH 5~8.5梯度的分离结果;蓝色:非线性pH梯度的分离结果
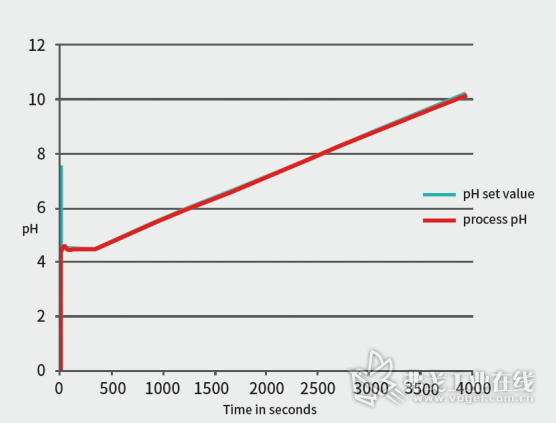
图10 线性pH 4.5~10.2梯度,蓝线是设定值,红线是实际值
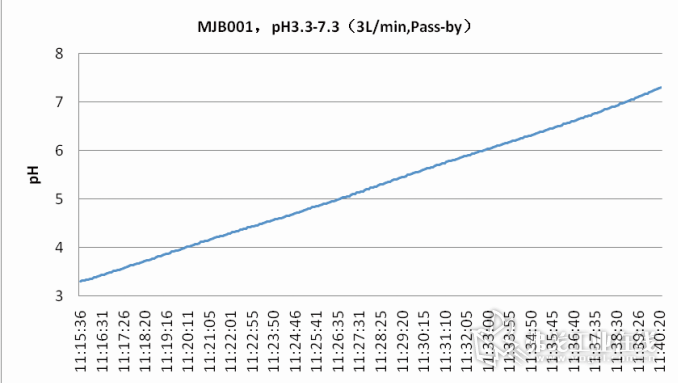
图11线性pH 3.3~7.3梯度
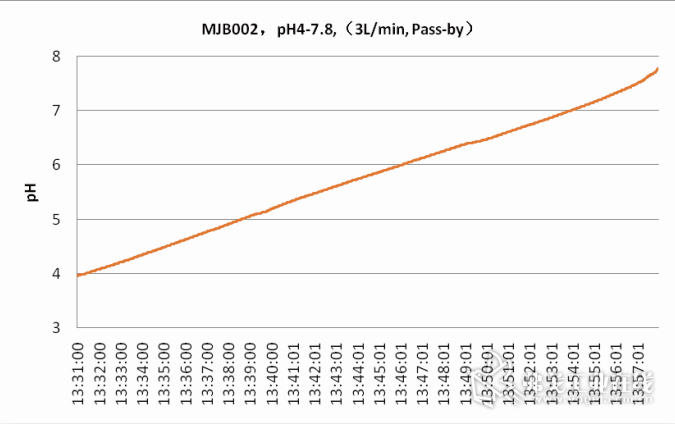
图12线性pH 4~7.8梯度
发展趋势
苏州美极的线性pH梯度配液中试设备mAbBuddy®,是全球第一家也是唯一能够在线配制线性pH梯度缓冲溶液的全能配液设备,满足中试和小规模量产需求,走在了同行业的前列。下面是mAbBuddy®配制出的三种线性pH梯度 (图10-12)。
总结
经过从实验室研发实验到中试设备的应用,已经可以证明,线性pH梯度可以在实验室色谱仪以及中试生产设备上实现。而且,从层析实验结果上看,线性pH梯度有很多明显的优势:
① 线性pH梯度可以替代盐梯度,如图7a和7b:相似pI的Trypsinogen和 Ribonuclease A 被基线分离。
② 层析后,线性pH梯度制备出的蛋白质,不需要脱盐,可以省去几个工艺环节,直接连接质谱去检测。这是因为大量的盐成分会影响质谱的检测,而线性pH梯度缓冲溶液无盐或很少盐,可以直接用质谱检测。如图7a和7b所示,线性pH梯度比盐梯度法分离效果更好。
③ 在单抗mAb提纯中,线性pH梯度不需要使用 Protein A,用离子交换填料配合线性pH梯度就可以分离单抗,成本低, 回收率好,纯度高。
④ 摆脱对少数protein A供应商的依赖。
⑤ 大幅降低生产成本,赢得市场竞争的胜利,获得较大利润空间。
随着社会的进步及新技术的创新,在技术应用领域,旧的方法必然会被更节约、更高效的新工艺替代。当新技术、新机会出现在眼前,只有具有敏锐眼光和敢于尝试的人能够把握得住。●
【参考文献】
[1] A Novel pH gradient Separation Platform for Monoclonal Antibody (mAb) Charge Variant Analysis, Application Note 20784, Thermo Fisher Scientific, USA
[2] High Resolution Charge Variant Analysis for Top-Selling Monoclonal Antibody Therapeutics Using a Linear pH Gradient Separation Platform, Application Note 21092, Thermo Fisher Scientific, USA.






加载更多