FDA加速批准常见误解
。

图片来源:CenterWatch
用于加速批准的替代终点(surrogate endpoint)是一个标记(marker),例如实验室测量、射线照相图像、体征或其他可以预测临床获益的指标,但其本身并不是临床获益的指标。同样,中间临床终点(intermediate clinical endpoint)是一种治疗效果的衡量标准,很可能预测药物的临床益处,例如对不可逆发病率和死亡率(IMM) 的影响。
FDA根据科学支持,决定是否接受提议的替代临床终点或者中间临床终点。根据FD&C 法案的要求,证明药物对替代或中间临床终点的影响的研究必须“充分且得到良好控制”。
使用替代或中间临床终点可以在药物批准过程中节省宝贵的时间。例如,FDA不必等待了解一种药物是否真的能延长癌症患者的生存期(对于未受试的患者来说,这样的时间是等不起的),而是可以根据药物缩小肿瘤的证据批准该药物,因为肿瘤缩小被认为很可能预示着真正的临床益处。在这个例子中,基于肿瘤缩小的批准,明显比等待了解患者是否真的活得更久要快得多。但制药公司在获批后仍需要进行深入研究,以确认肿瘤缩小实际上预示着患者会活得更久。如果验证性试最终证实了临床益处,FDA通常会不再做出进一步要求。但如果试验未能验证临床益处,或者没有证明足够的临床益处来抵消与药物相关的风险(例如,相对于根据观察到的替代终点的效果所推算出来有效性,比实际效果在大小和持续时间方面都要小得多的情况),FDA则可能会撤回药物的批准,或者更改药物的标签适应症。
对于FDA的加速批准条例,存在很多误解,这些误解损害了罕见疾病治疗的适当监管。其中最显著的三个误解来自于:

图片来源:Ars Technica
争论的焦点在于,那些凭借替代生物标志物(surrogate biomarkers)而获批的药物,可能会造就一批华而不实的昂贵产品,而这些药物实际上可能不会改善患者的预后。
实际上,加速批准途径的核心要义,就是缩短药物批准时间,针对的是那些无法在合理的时间范围内收集足够的临床结果数据的重要药物开发。使用经验证的准确生物标志物,可以有效地加快药物发现、临床研究和批准的周期。
HIV是一个具有代表性的例子,如果没有基于原发疾病生物标志物的批准,抗HIV药物就不可能在那么快的时间内出现在市场,其后果必然是成千上万的患者在无药可用的情况下绝望地死去。1992年首次批准的有效HIV药物使用了生物标志物,而不是漫长地等待常规临床结果。在第一批HIV药物上市后,更新产品不断问世,争取了宝贵的时间和数据。在第一个抗艾药物获批后,在接下来的16年间共有29种药物获批上市(其中包括四种药物组合),使HIV从起初的全人类恐惧,逐渐蜕化成为一种可以实现良好控制的疾病。如果墨守陈规地根据临床数据做出批准决定,人类恐怕仍处于高度恐艾的阶段。
替代生物标志物的性质,可以拿减肥做一个比喻。我们都知道,肥胖对人类健康害处颇多,为了身体健康,肥胖者需要减肥。那么减肥和身体健康之间就会建立一个关联,比如心脏健康程度,代谢疾病等。但衡量减肥的效果,不一定就非要以心脏健康和代谢病的控制作为标准。如果要尽快衡量减肥的效果,你可以直接选择体重作为标准,即替代生物标志物,只要在这个替代生物标志物上实现了终点,你就可以认为,减肥对于心脏健康和代谢病控制达到了目的。因为后两者并不完全是由肥胖所控制的,可能还包括饮食习惯、心理健康、生活习惯,熬不熬夜、抽不抽烟、酗不酗酒等。但只要体重达标,我们就可以认为减肥的终点完美达到,并对心脏健康和代谢疾病的控制产生益处。
此外,原发疾病生物标志物(primary disease biomarkers)具有良好的口碑。所有使用原发疾病生物标志物,来推算罕见遗传疾病治疗效果的获批药物,无论是通过加速批准还是标准批准,都无一例外地通过验证性研究,或者上市后研究,证明了它们临床有效性,并且没有一个被撤回。
所以说,代表潜在疾病状态的生物标志物不是审批过程中的妥协。事实上,原发疾病生物标志物,通过提供精确的疾病测量方法,在设计、开发和改进治疗方面,表现出优于常规临床终点的素质。
另一种普遍的误解是,第一个通过加速批准的药物,将成为未来同类产品的绊脚石。因为监管机构已经批准一种药物上市,加速批准的基础随之不复存在,对于其它同类药物将采取常规审批过程。这也是一种误解。例如罕见病杜氏肌营养不良症,第一个基于生物标志物的加速批准产品,它建立了一个明确的参照物,其疗效标准需要被今后的更新产品超越。Sarepta Therapeutic的基因疗法delandistrogene moxeparvovec就是这样一个踏着前药基础前进的先进疗法,同样可以接受加速批准。在写这篇文章的同时,FDA正准备就Sarepta Therapeutic的这款杜氏肌营养不良症的基因疗法产品进行一个咨询委员会会议。如果非要要求将来的杜氏肌营养不良症的竞争对手,通过完整的临床终点才能实现批准的话,这将成为这个领域难以承受之重。这些未来的竞争对手,他们将不得不与Sarepta的基因疗法进行头对头临床研究,这会产生极其高昂的费用,因为研究赞助商需要购买Sarepta的药物进行试验,然后进行一项大型的多年的研究,以寻找两种药物之间的结果差异。这种规则将破坏这个领域的药物升级。
第一个基于生物标志物的加速批准,将为整个行业提供了一个清晰的、准确的、基于证据的标杆,这种比较可以在更短的时间内实现,并不需要进行头对头研究。除了上文提及的HIV的好药迅速被更好的药物取代例子,1990年代第一批治疗纯合子家族性高胆固醇血症和尿素循环障碍的药物获得批准,也奠定在随后的几年里开发出多种更好药物的基础。溶酶体贮积症戈谢病(Gaucher’s disease)和法布里病(Fabry’s disease),它们的酶替代疗法的首次批准(均由生物标志物进行)引领了多种后续产品的上市。苯丙酮尿症的第一种药物沙丙蝶呤(sapropterin)的上市,就是以苯丙氨酸(phenylalanine)水平作为生物标志物的以实现的。而后续升级产品pegvaliase也是基于这个生物标志物登堂入室的,而且还有更多的候选药物正处于开发之中。
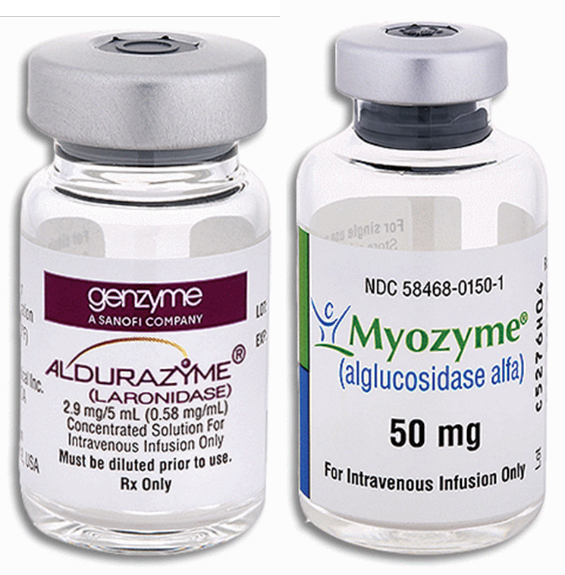
从相反的角度来看,黏多糖贮积症Ⅰ型(MPS I)和庞贝病(Pompe disease) 的酶替代疗法获批时,采取的是常规的临床终点而非生物标志物,然而这两种疾病在随后的20 年(Aldurazyme®,2003年上市)和17年(Myozyme®,2006年上市)中均没有获得后续批准。
事实是,首次基于生物标志物的批准,能够带来更多投资和对新药、好药物的批准,这与普遍认为的观点恰恰相反。生物标准物,并非先来先得。
在追求临床药物知识的过程中,对安慰剂对照组的一些不可逆转的伤害是可接受的
这种误解涉及到学术生物伦理学。许多疾病,例如杜氏肌营养不良症,临床终点驱动试验将需要更多的时间和更多的疾病进展,以便与治疗组进行比较,以充分支持研究。但未经治疗的对照组患者,将遭受不可逆转的伤害。对具有不可逆脑部或肌肉疾病的受试者,进行随机安慰剂对照研究设计的做法,应被视为不道德。对于杜氏肌营养不良症来说,要求一组儿童长期服用安慰剂以证明治疗组中有显著的临床益处,这也是明显不合理的做法。验证临床益处更恰当的做法,是在上市后确认试验中,使用更长的时间范围和更大的受试范围。
附:
加快治疗严重疾病的药物的供应符合每个人的利益,尤其是当药物是第一个可用的治疗药物,或者药物比现有治疗药物具有优势时,它们应该更快地脱颖而出造福患者。FDA已经开发出四种不同的审批方法来实现这个目标:

图片来源:ProEd
优先审查Priority Review
突破性疗法Breakthrough Therapy
加速审批Accelerated Approval
快速通道Fast Track
虽然这四种策略都包含着“速度”的基本因素,但它们之间是存在区别的:
加速审批Accelerated Approval:如正文
快速通道Fast Track:快速通道是一个旨在促进开发和加快药物审查,以针对严重疾病和未满足的医疗需求的过程。目的是让重要的新药更早地送到患者手中。快速通道针对广泛的严重疾病。确定病情是否严重,是基于药物是否会对生存、日常功能或如果不治疗病情进展的可能性等因素产生影响。艾滋病、老年痴呆症、心力衰竭和癌症是严重疾病的明显例子。然而,癫痫、抑郁症和糖尿病等疾病也被认为是严重的疾病。
未满足的医疗需求,指的是没有疗法的疾病,或者提供比现有疗法更好的治疗(有条件)。任何正在开发的,用于治疗或预防目前尚无疗法的疾病的药物,显然都是针对未满足的需求。如果有可用的疗法,快速通道药物必须显示出一些优于可用疗法的优势。
快速通道必须通过制药公司申请。该请求可以在药物开发过程中的任何时间发起。FDA将在六十天内审查请求,并根据药物是否满足条件而做出决定。一旦药物获得快速通道指定,在整个药物开发和审查过程中,制药公司应与FDA进行及时和频繁的沟通。沟通的频率确保问题快速解决,通常会导致药物批准更早得到批准。
突破性疗法Breakthrough Therapy:突破性疗法指定,是加快开发和审查治疗严重疾病的药物,其初步临床证据表明,该药物可能在临床重要终点上出比现有疗法有实质性改善。就突破性疗法认定而言,具有临床意义的终点,通常是指衡量对不可逆发病率或死亡率 (IMM) ,或者疾病严重后果的症状。
如果发起人未申请突破性疗法指定,FDA可能会视情况建议发起人考虑提交请求。获得突破性进展的药物可以获得优先审查。FDA与药物申请的发起人合作以加快审批过程。这个加速过程可以包括滚动审查、较小的临床试验和替代试验设计。
优先审查Priority Review:1992 年,根据《处方药使用者法》(PDUFA),FDA 同意了缩短药物审评时间的具体目标,并创建了一个两级审评时间系统:标准审查和优先审查。优先审查指定意味着 FDA 的目标是在 6 个月内对申请采取行动(标准审查为 10 个月)。FDA 决定每个申请的审查指定(标准或者优先)。但是,申请人可以明确要求优先审查(使用优先审查凭据Priority Review Voucher)。FDA 在收到BLA和NDA后 60 天内通知申请人优先审评指定。将药物指定为“优先审查”,并不会改变批准的科学标准。
Ref.
Fast Track, Breakthrough Therapy, Accelerated Approval, Priority Review. FDA.gov. 23. 02. 2018
Kakkis, E. D. et al. Three misconceptions about the accelerated drug approval pathway. STAT. 10. 05. 2023.
内容来源:药事纵横
责任编辑:胡静 审核人:何发
邵丽竹
何发
热点文章
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
微生物发酵技术在植物活性成分提取中的应用研究进展
2026-03-06
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多