干货分享!做好药厂洁净区环境监测知道这几点事半功倍
Ø 测试方法:静态条件下进行测试,采用风量罩套取每间洁净区房间高效过滤器送检测风风量。制剂车间洁净区风量每季度测试一次,其他洁净区风量每半年测试一次。
Ø 采样点:洁净区每间房间高效过滤器。
Ø 可接受标准:根据房间面积换算换气次数,与设计风量和换气次数进行比对应在设计范围内,并符合洁净级别的要求。
Ø 测试方法:
Ø 采样点:
Ø 可接受标准:洁净区与非洁净区之间、洁净级别不同的相邻房间之间的静压差应大于10帕。
Ø 测试方法:采用关键操作房间内放置温湿度表显示数值,每日生产前进行读数并记录。
Ø 采样点:关键操作房间。
Ø 可接受标准:一般温湿度应控制在温度18~26℃、相对湿度控制在45~65%,特殊情况根据不同产品生产工艺规定要求。
Ø 测试方法:
Ø 采样点:
Ø 可接受标准:
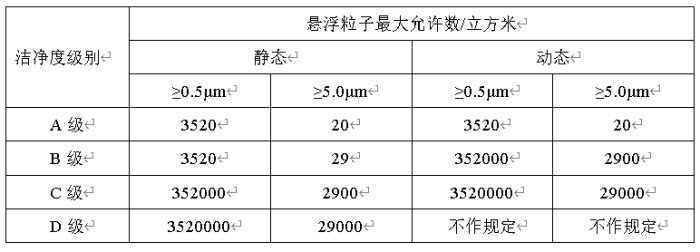
Ø 更换高效过滤器后应对悬浮粒子进行测试。
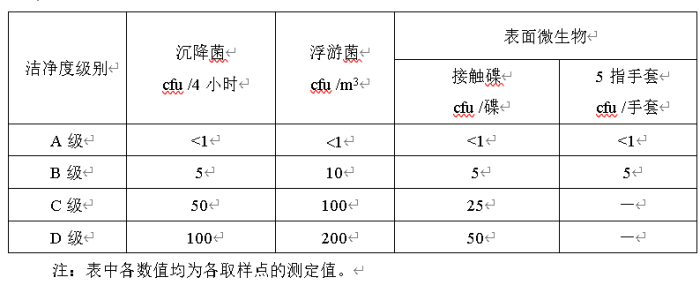
Ø 测试方法:
Ø 采样点:
Ø 测试方法:
Ø 采样点:
Ø 测试方法:

Ø 通知相关部门负责人;
Ø 经过调查判断超标的原因和导致的结果;
Ø 根据实际情况制定相应的纠正措施并执行以解决问题;
Ø 后续的回顾评价纠偏措施的有效性;
Ø 其他
内容来源:药事纵横
责任编辑:胡静 审核人:何发
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
走进标杆|霍尼韦尔 × 博腾股份:以数智之力,让好药更早惠及大众
2026-04-02
-
AI+制药行业潜力巨大,产业链相关公司梳理(名单)
2026-04-29
-
固体制剂制药工艺与质量控制研究
2026-03-17
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多