明胶胶囊交联问题的研究思路
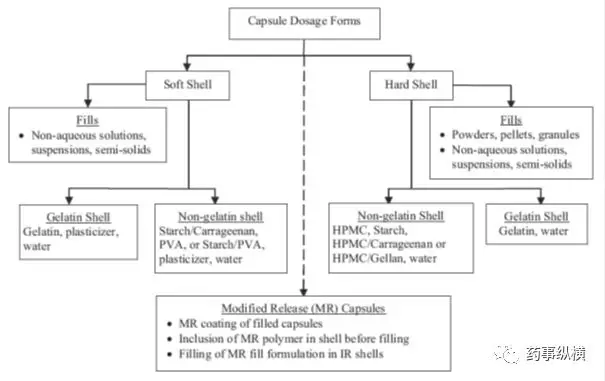
明胶胶囊交联现象指明胶囊壳在贮存过程中发生交联反应,使制剂在不加酶的溶出介质中的崩解、溶出、释放效率降低的现象。在药物的稳定性考察试验中,胶囊交联现象经常出现,表现为在进行溶出试验时胶囊变成了一个类似橡胶质样的胀大的水不溶膜,此水不溶膜在溶出试验中能够使胶囊的崩解时间延长、药物溶出速率下降、甚至造成药物完全不能溶出。

篮法中的胶囊交联现象

桨法中的胶囊交联现象
遇到明胶胶囊交联问题如何思考与应对?本文浅谈一下研究思路,仅供药物研发同仁参考。
一、交联反应的机理及防止措施
明胶是一系列水溶性胶原蛋白衍生物的混合物,它是一种线性高分子聚合物,分子量15000至25000,由酰胺键连接各种氨基酸构成,组成的氨基酸包括:甘氨酸25.5%;脯氨酸18.0%;羟脯氨酸14.1%;谷氨酸11.4%;丙氨酸8.5%;精氨酸8.5%;天门冬氨酸6.6%;赖氨酸4.1%;亮氨酸3.2%;缬氨酸2.5%;苯丙氨酸2.2%;苏氨酸1.9%;异亮氨酸1.4%;蛋氨酸1.0%;组氨酸0.8%;酪氨酸0.5%;丝氨酸0.4%;胱氨酸0.1%;半胱氨酸0.1%。
交联反应的形成主要归因于有三个官能团的氨基酸,尤其是赖氨酸。一些报道提出组氨酸和精氨酸也参与交联反应的形成。
1、交联反应的主要机理
明胶中赖氨酸游离氨基酸残基间发生交联反应。
赖氨酸残基的氧化去氨基化,得到一个末端的醛官能团,这个醛与相邻赖氨酸的ε-氨基结合得到一个亚胺,然后经过一系列aldol(羟醛反应)类缩合反应得到含有吡啶环的交联产物。
赖氨酸与外源的醛发生交联反应。
赖氨酸ε-氨基与外源的醛,比如处方中的杂质或处方与外界环境接触后生成的醛发生反应。这个反应生成一个羟甲基氨基衍生物,脱水后生成含有一个阳离子的亚胺,后者与另一分子的羟甲基氨基赖氨酸残基生成二亚甲基醚,最后重排生成一个连接两个赖氨酸ε-氨基的亚甲基,从而形成交联。
形成胺缩醛后发生交联反应。
胺缩醛,即乙缩醛的氨基形式。胺缩醛是通过阳离子亚胺中间体(同上述阳离子亚胺的形成过程)与一个游离氨基反应生成。这一反应对周围的pH很敏感。人体胃液的环境与体外溶出环境不同,胃液中含有酶,胶囊交联引起的溶出延迟或不溶出对于体内溶出究竟有没有意义目前还很难下结论。在胶囊剂产品的开发阶段,能够可能导致交联问题的每一个因素都应仔细考虑,从早期设计阶段就要尽可能避免,或者通过高温、高湿试验来进行预判,尽早采取措施进行防止或制定相应研究对策。
2、防止交联反应的方法
选择不易产生醛类物质或不易促进交联反应发生的辅料。
在制剂的辅料中,增塑剂、防腐剂、脂肪、聚乙烯化合物比如:PEG、脂肪族醇类、脂肪族酚类、聚乙烯甘油酯等均易产生醛类物质。非离子表面活性剂吐温80,由于分子中含有聚氧乙烯基,易发生氧化降解,形成甲醛。
对于易产生交联反应的药物,不宜开发成硬胶囊、软胶囊等剂型。
如吉非贝齐、依托度酸、氯霉素、呋喃妥因、扑热息痛、地高辛、维生素、布洛芬等在放样过程中均出现溶出度显著下降的情况。含有醛基的药物与明胶残基发生反应,使明胶发生交联。
控制外界环境中温度、湿度、光照等因素的影响。
交联反应的发生受外界环境中温度、湿度、光线的影响。胶囊应贮存在温度15~25℃,相对湿度30%~40%,阴凉干燥避光处贮存。室温下交联反应较不易发生,长期储存于高温下的明胶分子中氨基酸残基易发生自氧化而形成醛基,形成的醛基可以和周围明胶分子上的氨基酸残基发生交联反应,使明胶分子结构发生变化后,水溶性大幅下降。并且随着温度的升高,交联反应的程度越剧烈。高湿条件的影响尤为重大,它可以催化亚胺中间体的形成,催化辅料降解成促进交联反应发生的降解产物,同时使氧气更容易穿透明胶分子,从而加速对它的氧化作用。紫外可见光与高温、高湿相互作用也促进了交联反应的发生和促进明胶的自氧化有关。
囊壳处方因素的影响
囊壳处方是决定囊壳交联的主要因素:(1)明胶的选择:明胶的交联程度主要是受明胶中氨基酸的残基量影响,明胶中赖氨酸和精氨酸的含量越低,则交联发生程度和可能性越低。(2)囊壳的含水量:囊壳中含水量高时,可以加快明胶的氧化,使亚胺中间体的产生加快。(3)增塑剂:甘油和山梨醇等增塑剂会使明胶的自氧化作用增强。(4)遮光剂和着色剂:加入的遮光剂和着色剂可能诱导醛类分子产生,从而与明胶发生胺缩醛反应。(5)铁离子:胶囊中含有铁离子,使氨基酸经芬顿化学反应,生成羟基自由基(·OH),羟基自由基氧化氨基酸的氨基和中心碳原子,导致明胶交联,但铁离子含量对交联现象的影响不能确定。(6)铁离子和铝离子:Fe3+除催化羟基自由基生成外,Fe3+和Al3+能与明胶游离的羟基形成配合物。
二、明胶胶囊交联研究的指导原则USP<711>
USP<711> Dissolution溶出度项下规定,如果是因为交联引起了溶出度不符合标准规定,应进行二级溶出试验(Tier II),即添加酶和不添加酶溶出试验。对于不同pH的溶出介质,选用的酶的种类也不一样,以下为各个pH条件下推荐的酶种类、浓度、活性测定标准/方法(很有用哦!)。
Dissolution Medium with pH 4.0
Enzyme: Pepsin(胃蛋白酶), activity determined by the procedure in purified pepsin, in the Reagent Specifications section
Amount: A quantity of pepsin that results in an activity of NMT 750,000 Units/L of dissolution medium
Dissolution Medium with pH >4.0 and <6.8
Enzyme: Papain(木瓜蛋白酶), activity determined by the Assay test in the monograph for Papain; or bromelain(菠萝蛋白酶), activity determined by the procedure in bromelain, in the Reagent Specifications section
Amount: A quantity of papain that results in an activity of NMT 550,000 Units/L of dissolution medium, or a quantity of bromelain that results in an activity of NMT 30 gelatin-digesting units (GDU)/L of dissolution medium
Dissolution Medium with pH 6.8
Enzyme: Pancreatin(胰酶), protease activity determined by the procedure in Assay for protease activity (Casein digestive power) in the monograph for Pancreatin
Amount: A quantity of pancreatin that results in a protease activity of NMT 2000 Units/L of dissolution medium
溶出介质中含有表面活性剂或其他能影响酶活性的其他成分时,USP也有重要说明,作者将原文及主要翻译列举如下:
If the dissolution medium contains surfactant or other ingredients that are known to denature the enzyme used, a pretreatment step in the dissolution testing of the dosage form may be applied(加入预处理步骤).This pretreatment step is done using the specified dissolution medium without the surfactant or the ingredient and with the addition of the appropriate amount of enzyme according to the medium pH(预处理步骤中不含破坏成分只含有适当的酶). The amount of enzyme added is appropriate to the volume of dissolution medium used in the pretreatment(酶的量应该适当).To achieve the specified medium volume for the final dissolution testing, the pretreatment step may be conducted with a smaller volume of medium without the ingredient such that the final volume is obtained when the ingredient is added at the end of the pretreatment step(预处理步骤中应采用一个小的介质体积,预处理步骤结束后加至最终体积). All of the other conditions of the test (apparatus, rotation, orflow rate) should remain as described in the method or monograph(溶出条件与标准方法相同). Typically, the duration of the pretreatment step is NMT 15 min(通常,预处理步骤不超过15min). The required pretreatment time should be evaluated on a case-by-case basis and should be scientifically justified(所需的预处理时间具体问题具体分析,应进行科学说明). This time should be included in the total time of the test(预处理时间包括在总测定时间中). As an example, if the total time of the test is 45 min and 15 minare used in the pretreatment step, the test will continue for 30 min after the addition of the ingredient(例如,总溶出时间为45min,预处理为15min,加入其它成分后继续进行30min)。
了解影响酶活性的表面活性剂种类很重要。Guzman等就胃蛋白酶分别在含十二烷基硫酸钠(SDS)、十六烷基三甲基溴化铵(CTAB)、聚乙二醇辛基苯基醚(Triton X-100)和吐温-80四种表面活性剂的溶出介质中的活性进行了实验。结果表明,添加SDS会降低胃蛋白酶的活性,即使低浓度SDS仍会明显降低其活性。而添加任意浓度的CTAB、Triton X-100 和吐温-80均不会影响胃蛋白酶的活性。Guncheva等对胰蛋白酶进行相似研究,结果为非离子型表面活性剂(吐温-80和Triton X-100)能够增强胰蛋白酶的活性,而离子型表面活性剂(SDS和CTAB)会抑制其活性,因此在添加胰蛋白酶的体外溶出试验中建议使用非离子型表面活性剂。关于表面活性剂对溶出介质中木瓜蛋白酶和菠萝蛋白酶活性的影响研究尚未见报道。
三、问题分析与讨论
1、如何理解FDA溶出数据库中的Tier I和Tier II?
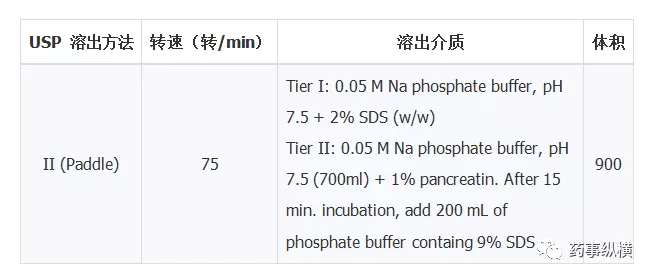
以Ziprasidone HCl胶囊为例,FDA溶出数据库中规定了Tier I和Tier II方法,见下表。根据USP711,如果胶囊有交联现象,可以在介质中加入酶。如果溶出介质中含有表面活性剂,酶活性会受到破坏,因此需要采用无酶介质进行预处理,最长时间不得超过15min,然后再加入含酶介质。本例中的意思是,该胶囊采用Tier I进行溶出测试,当发生交联的时候可采用Tier II。如果采用Tier I方法时发现S1阶段不合格,采用Tier II并应符合S1阶段要求,不必再继续采用Tier I方法继续考察S2、S3。
2、选择加入酶之前需要考虑哪些问题?
首先,应确定溶出变慢确实是由胶囊交联引起的,这一点很重要。方法有目测法(观察到胶囊吸水膨胀,没有破裂或者部分破裂)、转换法(把胶囊的内容物撞到新的没有发生交联的囊壳里)。其次,需要根据介质的pH,参考USP711选择加入酶的种类与来源(必要时根据研究情况固定厂家)。第三,需要酶种类规定测定酶活性,并确定下来酶的测定方法,因为酶的测定方法很关键。
3、在稳定性考察过程中发现交联怎么办?
首先,还是必须先评估并确定溶出变慢或不溶出是由交联引起的,而不是由制剂本身性能变化引起的。其次,根据USP711采用加酶的方法进行溶出度测试。第三,后续时间点均需采用加酶的方法进行测试,完成数据对比。
4、在每一个溶出杯中加酶还是配制含酶的介质?
根据USP711,如果因为交联引起溶出度试验失败,首先应考虑复测,而不是在已发生交联的溶出杯中加入酶。如果在每一个溶出杯中加入酶需要多次称量,加入,溶解非常麻烦,因此,建议一次配制含酶介质,如6L、8L、10L等。
5、如果在制剂开发阶段就发现了交联现象怎么考虑?
首先,应分析可能的原因,如醛、高温、高湿的影响。处方中成分是否含有少量的醛类或可能产生醛类的物质,如是,应进行辅料的内控或者替代研究;胶囊贮藏条件是否正确,如是,应选择恰当的包材及贮藏条件。
6、加酶的溶出方法是否需要进行方法学验证?
需要的。例如,(1)应检查并确定介质的pH;(2)根据pH选择酶的种类;(3)确定酶活性测定方法;(4)介质中酶的量如何计算;(5)研究并确定溶出度不符合规定是由胶囊交联引起的;(6)加入酶后的滤膜验证试验;(7)加入酶后对检测方法是否产生干扰(专属性);(8)如果介质中含有SDS等表面活性剂应研究预处理步骤中的时间、体积;(9)最终制定的加酶不加酶溶出方法。
四、案例分享:开发Tier II方法的思路
问题描述:某产品,经加速3个月后,采用Tier I 方法测定,即900 mL的0.01 N HCl+1.0% SDS溶液。发现溶出曲线中溶出量在10~60min明显下降,批内RSD明显变大,数据如下。由于限度为75%@45min,因此,溶出度已经不合格了。如何解决此类问题?
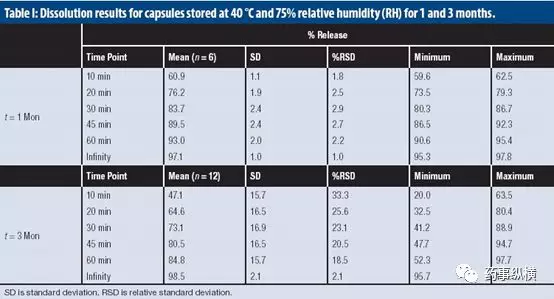
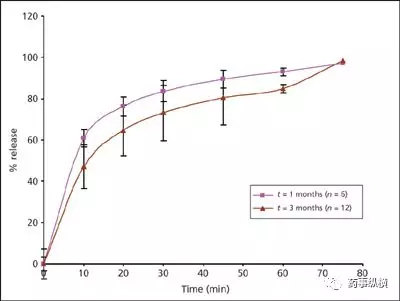
通过现象观察发现,可能是由于交联引起的,因此设计了三种实验,采用旧内容物+新胶囊壳、新内容物+旧胶囊壳、新内容物+新胶囊壳进行溶出曲线对比。根据对比可见,新内容物+旧胶囊壳的溶出量很低,变异大,因此与其他两组相比较可以判断是由胶囊壳产生交联引起的。
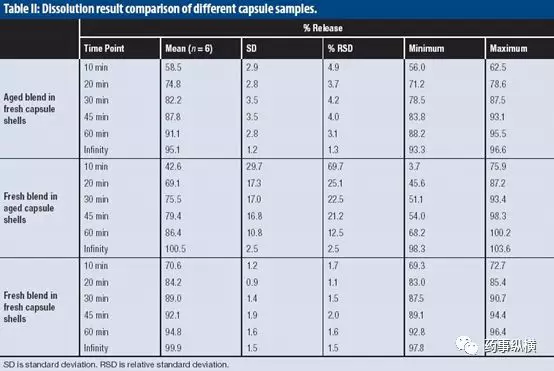
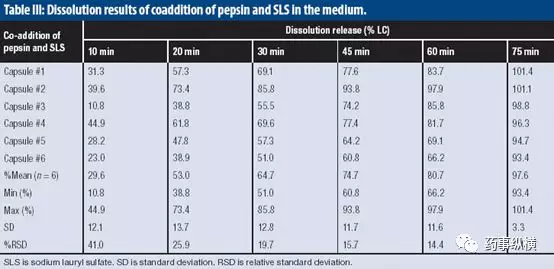
根据本品的介质pH,选择胃蛋白酶直接加入到900ml介质中,测定6粒胶囊的结果如下所示。结果表明,SDS引起了酶的降解,这种方法不可行,必须分步骤加入。
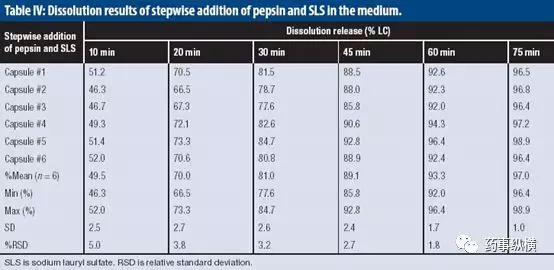
为了去除SDS对破囊试验的影响,介质1配制为不含SDS的0.01 N HCL + 750,000 units/L 胃蛋白酶溶液;先加入600 mL介质1,2min后发现6个胶囊开始散开,5min后加入300ml介质2,即0.01 N HCL+3%SDS溶液,最终介质组成为0.01 N HCL +1% SDS即500,000 units/L胃蛋白酶。
随后,整个Tier II方法进行了完整的方法学验证,包括线性、专属性、准确度、重复性、中间精密度、对照品溶液和供试品溶液稳定性等。
五、总结
明胶胶囊交联在胶囊剂开发中,特别是稳定性考察中经验遇到,采用合理的研究思路至关重要,中国药典溶出度通则中没有规定如何进行研究。作者建议,在注册申报阶段应考虑进行必要的说明,以免被发补。
六、参考文献
Rampurna P. Gullapalli, Carolyn L.Mazzitelli.Gelatin and Non-Gelatin Capsule Dosage Forms.Journal of Pharmaceutical Sciences, Volume 106, Issue 6, June 2017, Pages 1453-1465
Margareth R. C.Marques.Enzymes in the Dissolution Testing of Gelatin Capsules. AAPS Pharm Sci Tech, Vol. 15, No. 6, December 2014.1410-1416
谈颖, 夏鸣, 刘春晖, 等. 胶囊产生交联反应的研究[J]. 今日科苑, 2010(13): 137
张淼,梅梅,李煜,陈悦,洪利娅.明胶胶囊的交联现象及其在体外溶出试验中的研究进展[J]. 中国现代应用药学2018年2月第35卷第2期.302-305
USP <711> Dissolution
GUZMAN M L,MARQUES M R, ME M E O, et al. Enzymatic activity in the presence of surfactants commonly used in dissolution media, Part 1: Pepsin [J]. Results Pharma Sci,2016(6): 15-19.
GUNCHEVA M,STIPPLER E. Effect of four commonly used dissolution media surfactants on pancreatin proteolytic activity [J]. AAPS Pharmscitech, 2016, 18(4): 1402-1407.
X.Song, Y.Cui,M.Xie, "Gelatin Capsule Shell Cross Linking," Pharmaceutical Technology 35 (5) 62–68 (2011)
文章来源:药事纵横
邵丽竹
何发
热点文章
-
实施新版欧盟 GMP 附录 1 对制药洁净室设计的影响分析
2026-04-13
-
2.4 万亿市场背后:生物医药产业链全景图
2026-04-20
-
高活性固体制剂车间污染控制策略设计
2026-03-12
-
基于化工原理的中药提取车间优化设计与节能技术应用
2026-03-10
-
浅谈无菌药品生产过程中除菌过滤工艺的验证
2026-03-25
-
PDE 在药品共线风险评估中的应用探索
2026-03-13
-
浅谈无菌制剂生产过程中无菌保障措施的优化
2026-03-10
-
基于CFD仿真技术的灌装机充氮装置设计优化
本文以某制药产线的灌装机设备为研究对象,采用计算流体动力学(CFD)仿真技术对充氮装置的充氮性能进行分析,并结合分析结果对氮幕结构进行了优化设计。随后,针对优化方案进行性能仿真验证,结果显示优化后的顶空残氧量降低至0.252%。为了进一步验证优化方案的实际效果,将优化方案应用于实际产线进行性能测试,测得的顶空残氧量为0.68%,这一结果满足了小于1%的要求,表明其充氮保护性能已达到国际先进水平。
作者:王志刚、刘依宽、刘佳鑫
-
药品密封性检测 :用户需求与优化
-
可控冻融系统在生物原液上的应用
-
人用疫苗生产数字化转型
-
药包材生产质量管理的进阶策略
-
药厂洁净区域风量和压差的控制策略













评论
加载更多