一次性系统应用的风险把控思考
这也因此加速了在生物制品的研发生产中,一次性系统取代不锈钢系统的趋势。使用一次性系统可以通过降低资本成本,提高工厂灵活性,减少启动时间和成本以及消除非增值工艺步骤和交叉污染风险来显著影响制造工艺效率。此外,它还显著降低了工艺液体浪费、人工成本以及现场质量和验证要求。
如今,一次性工艺正逐渐取代不锈钢系统,涵盖了整个生物制药工艺过程的各个单元操作,从上游细胞培养到下游纯化,直至最终灌装。但在实际应用中,如果制药商们无法以安全稳妥的方式将各个组件以完全封闭的形式连接成一个完整的无菌系统,那么一次性技术的优势将无法得到充分发挥,过程中的风险也将增加。
全封闭的一次性系统的必要性
总的来说,在生物工艺的流体系统中,通常意义上的快速插拔式连接(如鲁尔接头)属于开放式连接;而一次性无菌连接领域的传统解决方案,即无菌软管接管机/封管机是否可以确保完整的封闭式连接也存在争议。
包括鲁尔接头在内的快速插拔连接方案通常能和相应管道配套使用,但这种接头属于开放式连接,对操作环境的要求很高,使用过程需配备层流罩(即需在层流保护下使用)或在Class A环境下使用。当脱离无菌环境,开放式连接依然可能带来外部污染。
此外,封管机和接管机也是软管无菌连接的传统解决方案。由于需要用到加热刀片,封管机和接管机仍然有可能将外部的污染物带入管路中,而且操作过程相对繁琐,增加了时间成本。同时,这两种机器也需适配特定型号的热塑管,增加库存压力和耗材成本,也增加了未知的风险。
基于此,传统的一次性无菌连接需要解决一些连接技术上的挑战,才能实现完整的全封闭系统:
传统的无菌连接方案对环境要求很高,而且依然存在外源性的污染风险(比如接管机的刀片等)。如何能在在有菌环境中仍然实现可靠、易操作的无菌连接和断开?
无菌连接和断开的传统解决方案需要不同的辅助设备和步骤。是否有能简化无菌连接和无菌断开的操作流程,将两种功能进行集成,从而节省时间和空间、降低风险?
除了上述基于降低污染风险的考虑,一次性系统的推进还需要考虑以下因素:
体积限制了一次性设备在大规模生产上的运用,包括大流量的下游应用和小流量的的小管路连接方案,比如针对细胞与基因治疗(CGT)领域的一次性连接。随着对更高产量生物制品和CGT应用的需求增加,一次性部件制造商已经在朝这个方向研发新的解决方案。比如,CPC的AseptiQuik L 可以做到1英寸到1.5英寸的大流量,而MicroCNX® 系列则可以连接小至1/16英寸(1.6mm)的管路。
一次性部件的完整性以及溶出物、析出物相关风险也需要企业针对自己的产品工艺进行评估。目前形成趋势的解决方案便是由部件制造商来对一次性部件进行预验证。
一次性设备的对接、溶液转移等步骤的自动化改良将是大势所趋,以减少隐形的人工成本和人工干预风险,保证产品的一致性和有效性等,同时减轻监管负担。
新一代的无菌连接技术
可见,传统的连接技术在有效形成封闭系统和灵活使用等方面均有可提升的空间。CPC 的一次性无菌连接系列产品便是为帮助制药商快速轻松、安全地传输生物介质而研发。

AseptiQuik® G DC 连接器是 CPC AseptiQuik® G 系列不分公母无菌连接器的最新成员,在无菌连接的基础上增加了无菌断开功能。
为了进一步简化生物制药,CPC实现了只需用一个产品便可以进行无菌连接和断开,无需使用额外的卡箍、夹具或接管机/封管机等任何辅助设备即可实现无菌连接和断开。
AseptiQuik® G DC 连接器软管倒钩端接尺寸包括 1/4英寸、3/8英寸 和 1/2英寸。其薄膜拉片可以确保同时安全去除两个膜片,内置自动截止阀,能在各种极端条件下实现可靠性能。

MicroCNX®是首款针对小规模封闭式无菌工艺的一次性连接器,为生物制药和再生医学领域的研发制造商提供一种简单、高效的小规模管路连接方案。
专为广泛使用小管径的应用而设计,包括1/16英寸(1.6mm)、3/32英寸(2.4mm)和1/8英寸(3.2mm),适用但不限于采样、培育扩增和早期细胞培养等工艺。
保证各连接流动路径一致,帮助制造商提高效率,减少创建封闭系统的时间和总成本,提供可靠的结果。
CPC的创新技术可以帮助制药商在有菌环境中仍然快速地进行管路的无菌连接和断开,形成真正的封闭式系统。直观的“翻转—咔嗒—拉拔”三步操作设计,可以确保用户方便传输介质,降低因操作失误所导致的风险。
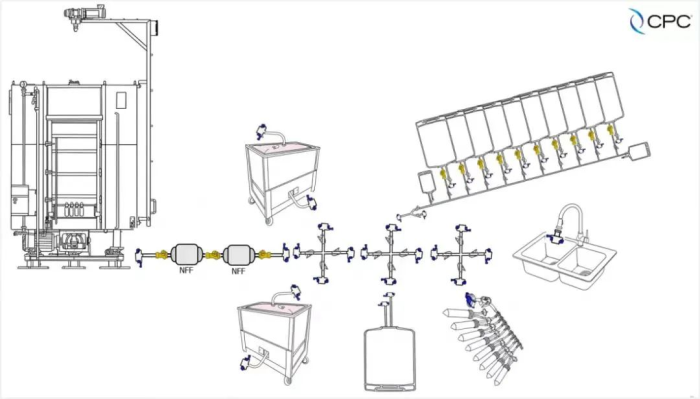
上游细胞培养中的无菌连接方案
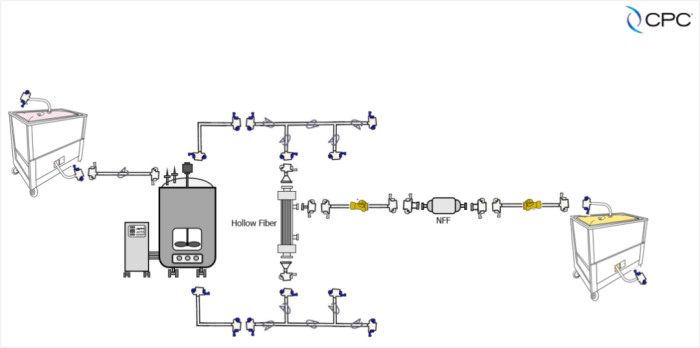
下游纯化过滤中的无菌连接方案
结语
对于无菌工艺而言,连接和断开管路进行流体输送而不增加污染风险是其关键。无菌连接技术可以将不同的子系统或工艺组合起来形成真正的封闭系统,从而提高了从上游发酵至下游灌装过程中的安全性、灵活性和效率。由于连接件是保持工艺无菌性的决定性因素之一,制药商需要仔细选择合适的连接方案和产品。同时,制药商应按照市场需求,持续开发产品,以满足制药商对无菌处理的需求。
CPC作为领先连接器专家,拥有40年丰富的经验,设计及生产超过10,000款连接器。CPC的工程师和设计团队可与您携手设计解决方案,为您的无菌断连保驾护航。
参考来源:
[1]Jayaraman P, Lim R, Ng J, Vemuri MC. Acceleration of Translational Mesenchymal Stromal Cell Therapy Through Consistent Quality GMP Manufacturing. Front Cell Dev Biol. 2021 Apr 13;9:648472. doi: 10.3389/fcell.2021.648472. PMID: 33928083; PMCID: PMC8076909.
[2]https://doi.org/10.1016/j.fbp.2013.12.002
[3]https://doi.org/10.1016/j.tibtech.2012.10.004
[4]洪小栩.药品生产用一次性使用系统风险管控的思考[J].中国食品药品监管,2022(02):51-59.
[5]黄景德,刘薇,黄义.一次性使用系统可靠性试验方案设计与分析[J].大连交通大学学报,2014,35(S1):131-134.
热点文章
-
2025版药典有哪些内容变动
2024-09-23
-
三种常见制粒技术对中药制剂内在质量的影响及生产过程控制要点
2024-09-27
-
科普 | 新药研发全流程梳理(图文版)
2024-12-03
-
中国药典2025版带来的冲击和影响
2024-10-04
-
洁净工作服清洗、灭菌及使用效期验证
2024-10-14
-
药品检查过程中关于偏差管理的分析与研究
2024-10-15
-
小组件 大作为:细胞和基因疗法 (CGT)工艺的闯关秘籍
2024-12-03
-
固体制剂高活性车间设计策略
口服固体制剂作为临床应用非常广泛的剂型之一,其传统生产模式存在产尘量大、生产暴露环节众多以及工序复杂等特点。因此,在生产 OEB4-5 级标准的口服固体制剂时,面临的挑战是多方面的。本文从车间建设的角度出发,探讨了针对高毒性或高活性等固体制剂生产所需采取的技术手段与措施。
作者:卞强、陈宁
-
降本增效的能源管理实施建议
-
直播预约 | 小核酸大未来:小核酸商业化生产与厂房设计建设
-
技驭未来,揭秘民营企业科技创新的基因密码
-
小柴胡颗粒连续逆流动态提取工艺研究
-
注射用甲苯磺酸奥马环素无菌检查抗菌活性的去除及验证













评论
加载更多