如何清洁无菌灌装区域?
先进的污染控制方法对成功的药品生产是十分关键的——尤其是对于那些不经过终端灭菌处理而在洁净室中使用无菌灌装技术包装的药品。
洁净室中通常有自动化设备、操作人员、灌装瓶、静脉袋,以及一定数量的待灌装药品。策略很简单,即对容器进行灭菌,对进入容器的所有东西进行灭菌,然后在几乎无菌的环境中进行灌装。
然而操作人员及其衣物无法达到无菌状态,因此必须依靠洁净的气流、工作服、手套以及清洁操作来保护产品不受生物污染,并使操作人员与产品不发生直接接触。污染物可通过气体、液体或附着于材料、衣物和皮肤上而进入洁净室中。还可由洁净室内的操作过程和操作人员的行动产生。一旦污染物沾染到表面上,尺寸小于10 μm的颗粒物不大可能被风吹到其他地方,但可能通过接触其他表面而发生转移,最终沾染到最终产品上。清洁后的小瓶、安瓿和柜子上可能仍然存在颗粒物,可能是由于操作中的摩擦产生的,也可能是从洁净室内其他地方转移过来的。颗粒物可能是由于玻璃或塑料表面材料剥落形成,也可能是由灌装后的化学反应引起,但较好的洁净室清洁操作并不能减少这些颗粒物的来源。
无菌灌装区域清洁的难度在于需要清洁的表面有很多:幕布、墙面、窗户、地板、天花板、桌面和机器的各处内外表面。以下将介绍无菌灌装室清洁和表面灭菌的一般原则。
无菌灌装洁净室
图1展示了无菌灌装区域的无菌性检测。所生产的材料不会接受终端灭菌处理,因此需要采取特别措施保证产品无菌。洁净室中的空气经过过滤。操作人员穿戴特殊的洁净室工作服装。洁净室中操作人员越少,产品中污染物颗粒越少。进入洁净室的材料要经过灭菌处理。

图1 通过灌装营养肉汤对无菌灌装区域进行无菌性检测
进行无菌灌装操作的要素包括设计、材料、区域分离、产品流、洁净度的连续性以及防范昆虫和啮齿类动物。设计要使清洁、消毒和维护操作便于进行,光滑表面、角落予以遮盖、灯具采用嵌入式安装方式、无凹处、室内管道设置尽量要少。热量、湿度和营养成分会促进微生物生长。因此应避免使用有孔材料和可发生代谢变化的含碳材料,并保持室内气流凉爽干燥,以避免这些因素的形成。产品流的关键是将受污染和未受污染的区域明确划分开来,避免发生物质交换。Van Gestel建议将洁净度划分为四个级别,从低到高依次是洁净室入口和符合美国联邦标准209 100 k级、10 k级和100级的无菌灌装区域。原材料、水和过滤器等应定期接受微生物和热原检测。操作人员应接受日常监控。对于墙面、天花板、地板和设备表面,应使用接触板进行监控。应定期使用支持微生物生长的培养基进行灌装操作,以检查灌装区域的无菌性。必须对人员进行培训和定期测试。
虽然无菌性是无菌洁净室的首要关心的问题,但防止非生命颗粒物污染也是一个重要问题。
使颗粒物难以去除的因素包括毛细作用力、静电作用力、硬化学键、热凝固、粘附力、范德华力、变形、嵌入、表面粗糙度及重力。
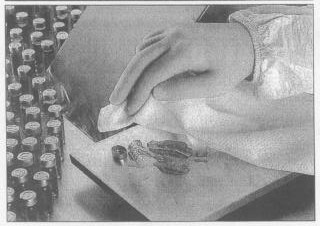
图2 在洁净室条件下对小瓶破碎后流出的液体和玻璃碎片进行清理
清洁策略
从建筑物入口到设备内表面的不同区域需要使用不同的方法和材料进行清洁。污染控制需要对入口、大厅和办公室进行常规清洁。紧挨着洁净室的区域,包括核心服务区,需要更为全面的清洁。更衣室和洁净室需要最为仔细和频繁的清洁。洁净室地板清洁应按从室内向入口的顺序进行,随后再对更衣室地板进行清洁。设备清洁可能需要拆卸、清洁和再次组装。
不论是否进行大致清洁都需要进行精准清洁。图2展示了在洁净室条件下对小瓶破碎后流出的液体和玻璃碎片进行清理的情形。精准清洁总要使用擦拭布或棉签。用于清洁的擦拭布和棉签应是最洁净的状态,因为所涉及产品的价值很高,清洁不成功造成的污染问题会很严重。本页列出了无菌灌装洁净室清洁所需的材料。
清洁材料
最洁净的擦拭布是由连续长丝纱(长的、不间断的纤维)而非短纤纱(短纤维)制成。作为原材料的纤维可以是天然的,也可以是切碎后合成的。织物构造方式包括短纤纱粘结、针织或编织。相比编织,针织形成的结构更具开放性和吸收性。用于擦拭布生产的材料包括棉及其他纤维素材料(包括人造棉)等天然材料,以及尼龙、聚丙烯和聚酯纤维等合成材料。合成材料更有可能实现很高的洁净度。擦拭布上的生物负载,通常以每张擦拭布上菌落形成单位数计量,取决于很多因素,主要包括原材料制作过程中的操作环节以及用于洗涤擦拭布的水质。最不具污染性的擦拭布往往是封边的,因为将织物切割成擦拭布往往会产生颗粒物和纤维,可能转移至设备和产品表面。对织物进行洗涤可以去除大部分颗粒物。图3是一张洗涤过的封边针织聚酯擦拭布的局部放大图。洗涤中使用水溶液,随后进行脱水、冲洗、脱水……最后将产品置于热空气中烘干。对于清洁要求较高的产品,洗涤用水使用前要除去离子并过滤。
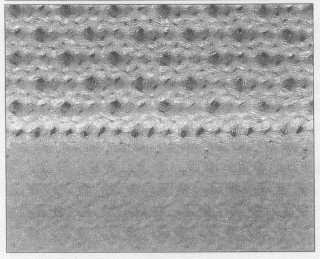
图3 一张洗涤过的封边针织聚酯擦拭布的局部放大图
用于无菌灌装区域清洁的擦拭布往往购买时已预先灭菌,通常使用gamma射线辐射,辐射剂量足以确保任何一张灭菌后的擦拭布上含有活性微生物的可能性小于百万分之一。这一辐射剂量一般接近25 kGy ( 2.5 Mrad ),这对聚酯纤维来说没什么问题。有时生产商会使用高压蒸汽,在2个标准大气压、121 ℃下对擦拭布进行灭菌。然而即使是死亡细菌也可能产生热原问题,因为革兰氏阴性菌外表面便是具有致热性的热原。蒸汽灭菌或辐射灭菌作为两种最常见的灭菌方法,并不能破坏热原,因此在进行任何终端灭菌操作前,必须要实行清洁生产,以最大程度地减少热原。
总的来说,擦拭布的重要品质包括:
吸水性;
洁净度:颗粒物含量低;
耐磨;
化学相容性;
可灭菌性;
便于使用;
防静电。
液体清洁剂
湿润擦拭效果较好,不仅是因为有的清洁液同时具有消毒效果,还是因为液体可以溶解颗粒物,并削弱颗粒物与被清洁表面的粘附力。去除颗粒很重要,因为颗粒中经常会裹藏着微生物,或使消毒剂无法接触到微生物。湿润擦拭布对颗粒物的吸引力远大于干燥擦拭布。但过度湿润的擦拭布则会使得一些颗粒物再次沉积到表面上。
新鲜配制的去离子水是高效的清洁剂,尤其能够很好地去除离子污染物,但通常会加入其它化学物质增强其效果。清洁液必须保持无菌状态。获取无菌水和保持无菌状态都是不易做到的;微生物可在去离子水中生长。通过过滤可以将微生物细胞从水中除去,但过了一段时间后,微生物的生长可透过过滤器,从而再次进入水中。异丙醇和水经常混合在一起施用于擦拭布上,用于清洁洁净室表面。但因为其对很多种孢子不具有杀灭效果,因此异丙醇水溶液并不用于药品生产过程中的灭菌。
常见的消毒剂水溶液包括漂白剂(次氯酸钠)、季铵盐化合物、过氧乙酸、过氧化氢、酚类等,这些物质经常混合制成配方独特的商业消毒剂产品。轮换使用两种以上的溶液是一项良好的实践,可以防止对任何一种溶液形成抗性的微生物持续留存。环境科学研究院对比了酒精、酚类、氯、戊二醛、季铵盐和碘的离子污染水平、有机物存在时的活性、在环保署注册为消毒剂还是灭菌剂、水溶性、残留活性、染色性以及对细菌、结核菌、细菌孢子、真菌及亲脂性和亲水性病毒的作用效果,得出的结论是“理想的消毒剂并不存在”。该公开发布的文件对洁净室消毒的以下选择作了说明:擦拭、拖地、冲洗、真空吸尘、喷雾、小物件浸润。
液体清洁剂的特性包括:
降低湿润表面的张力;
成分中包含水、烃类溶剂和碱性物质,帮助溶解离子和油脂;
挥发快;
挥发后残留物极少;
金属、卤素和挥发性有机物含量极少;
气味不重;
无毒、不易燃、不破坏臭氧。
预湿擦拭布可减少清洁溶液的用量,避免化学物质混合,确保清洁液中化学物质浓度适当,防止出现擦拭布与清洁液不相容的情况,并简化灭菌程序。应将其置于便于移动的容器中,避免交叉污染,并限制清洁液的挥发。
清洁方法
清洁人员应像洁净室中其他人员一样穿戴靴子、工作服、面罩、帽子和手套等。
首先,戴上手套,否则皮肤上的油和皮屑会沾染到待清洁表面上。另外也可防止具有腐蚀作用的清洁溶液接触皮肤。
然后,将擦拭布折叠,得到若干个干净的擦拭表面。若擦拭布是湿润的,则不要折叠,因为一次擦拭过后,沾染污物的清洁液会渗透擦拭布的折叠层。折叠的擦拭布还可以使手和手指的力均匀作用于表面上。
以平行轨迹擦拭,擦拭轨迹间充分重叠,确保无区域未被清洁。每条擦拭轨迹开始时,更换擦拭布表面或更换擦拭布,并从轨迹上最干净的一端开始擦拭。一条经验法则是,每擦拭10个擦拭布长度的距离更换一次擦拭布表面(若表面非常脏,则要更换更频繁些)。
对于消毒操作,要使用接近浸透的擦拭布,用足够的力度擦拭,留下可见的消毒剂膜。
因擦拭表面而转移到擦拭布上的污物量大致与污物在表面上的密度成正比,而从擦拭布上转移到表面上的污物量则大致与擦拭布上沾染的污物量成正比。转移率被定义为擦拭布的污物擦除率K(M/A)(与被清洁表面单位面积污物含量成正比)与擦拭布上污物再次沉积到表面上的再沉积率k(m/a)(与擦拭布单位面积污物含量成正比)的差值。(K和k的大小将取决于擦拭布、表面、清洁液和污物的特性。)我们希望在清洁过程中尽可能地保持擦拭布洁净,因此擦拭路径应是从较干净区域向较脏区域擦拭。就消毒操作而言,擦拭布应足够湿润,在被擦拭表面上留下一层液膜,该液膜要能存留较长时间以确保足够的灭菌效果。化学消毒效果取决于所要消灭的微生物种类、所使用的化学物质、时间、温度、浓度和对溶液的机械搅拌均匀度。上述各因素越有利,消毒就越彻底(但温度不能过高,以至于破坏用于消毒的化学物质的活性或损坏表面)。
清洁地板时,最好使用两个水桶,一个盛放清洁溶液,另一个用于冲洗脏拖把,冲洗之后再放入第一个水桶里浸润清洁溶液。地板在风干前应禁止通行,以防有人踩滑跌倒。
将化学剂倒入水中相对将水倒入化学剂中要更为安全(因为后者可能会使高浓度化学剂溅起)。为节约清洁液用量,应用清洁液浸润擦拭布用以清洁,而不要将清洁液直接施用于表面。勿要将擦拭布一张接一张地浸入清洁液中,以防止交叉污染。
清洁效果检查
成功的清洁实践要求在清洁后进行检查,看有无遗漏区域,并检查材料、清洁方法和操作人员是否有问题。可以使用检测表面污物的方法或确定产品适宜性(如产品外观或生物负载)的方法。
可使用以下方法检查洁净室表面的洁净度:亮光;紫外光;用深色或浅色擦拭布或棉签擦拭,之后用肉眼或显微镜评估;使用粘性胶带,随后用肉眼或显微镜评估;在光学粒子计数器或显微镜过滤器上连接真空头;对清洁后的区域进行冲洗,并用光学或电子显微镜对清洗液进行观察分析;使用液体颗粒计数器;进行生物测定;进行化学测定;进行放射性测定;使用无菌培养基接触板接触表面,然后进行培养。
无菌洁净室的清洁用具(根据1994年Thompson整理的内容稍作修改),均经过灭菌并仅用于洁净室:
擦拭布和棉签
清洁和消毒溶液
配药瓶
凳子或梯子
真空吸尘器(经中央系统或高效空气过滤器过滤冷却气和废气)
带绞拧装置的水桶
拖把
垃圾桶
总结
除非对无菌产品实行终端灭菌,否则便需要进行无菌处理。这就需要用到洁净室和无菌材料,包括无菌清洁材料。清洁始于工厂入口,越接近产品,清洁工作越是关键。清洁要从较干净的区域开始,向较不干净的区域进行。清洁所用材料本身必须是干净的。通过谨慎选择原材料和加工方式,可生产出干净的清洁材料。无菌灌装室中使用的清洁材料还必须是无菌的。要确保生产出的清洁材料无菌,可使用终端灭菌操作,通常包括辐射(gamma射线或电子束)或高压蒸汽灭菌。
【参考文献】
[1] T.E. Hansz and D.R. Linamen, “Planning, Programming, Designing, and Constructing a Cleanroom,” MDDI 17 (2), 73–86 (1995);
[2] Association for the Advancement of Medical Instrumentation, AAMI Standards and Recommended Practices: Vol. 1: Sterilization, AAMI, Arlington, VA, 1992;
[3] D.M. Carlberg, Cleanroom Microbiology for the Non-Microbiologist (Interpharm, Buffalo Grove, IL, 1995). Cleaning Aseptic Fill Areas;
[4]Institute of Environmental Sciences, Microorganisms in Cleanrooms, IESRP- CC023.1 (IES, Mount Prospect, IL, 1993);
[5] D.W. Cooper, “Sterility Assurance for Cleanroom Wipers,” presentation at the annual technical meeting of the Institute of Environmental Sciences, Anaheim, CA, April 1995;
[6] D.W. Cooper, “Cleaning Surfaces with Sterile Wipers,” presentation at Medical Design and Manufacturing East, New York, June 1995;
[7] K. Hiraoka, “Particle Control in Form/Fill/Seal Systems,” in Proceedings of the International Conference on Particle Detection, Metrology, and Control (Institute of Environmental Sciences and the Parenteral Drug Association, Arlington, VA, 1990), pp. 626–635;
[8] G. Van Gestel, “Clean Room Design and Operation,” in Sterilization of Medical Products, Vol. IV, E.R.L. Gaughran, R.L. Morrisey, and Y. Wang, Eds. (Polyscience, Montreal, 1986);
[9]J.F. Gallelli and M.J. Groves, “USP Perspectives on Particle Contamination of Injectable Products,” J. Pharm. Sci. Tech. 47 (6), 289–292 (1993);
[10] C.L. Thompson, “Cleanroom Cleaning,” presentation at Clean-Rooms ‘94 East, Philadelphia, March 1994;
[11] M.S. Favero and W.W. Bond, “The Use of Liquid Chemical Germicides,” in Sterilization Technology: A Practical Guide for Manufacturers and Users of Health Care Products, R.L. Morrisey and G.B. Phillips, Eds. (Van Nostrand Reinhold, New York, 1993);
[12] G.K. Bass, “Methods of Testing Disinfectants” in Disinfection, Sterilization, and Preservation, S.S. Block, Ed. (Lea &Febiger, Philadelphia, 1977);
[13]T.H. Leahy, “Microbiology of Sterilization Processes,” in Validation of Aseptic Pharmaceutical Processes, F.J. Carleton and J.P. Agalloco, Eds. (Marcel Dekker, New York, 1986);
[14] J.D. Wilson, “Validation of Sanitizers,” in Validation of Aseptic Pharmaceutical Processes, F.J. Carleton and J.P. Agalloco, Eds. (Marcel Dekker, New York, 1986);
[15]Institute of Environmental Sciences, Cleanroom Housekeeping—Operating and Monitoring Procedures, IES-RP-CC018.2 (IES, Mount Prospect, IL, 1992);
[16] J. Hansen et al., “Investigating AAMI Radiation Audit Results,” MDDI 16 (5), 218–222 (1994)。






加载更多