偏差流程要点分析和偏差处理成熟度的考量
Part
1
1.1
偏差概述
1.2
偏差的发现与报告
1.3
偏差分类

表1 与委托方协商共同管理偏差的方式
1.4
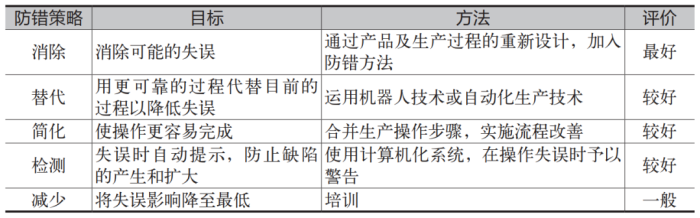
偏差的根本原因调查
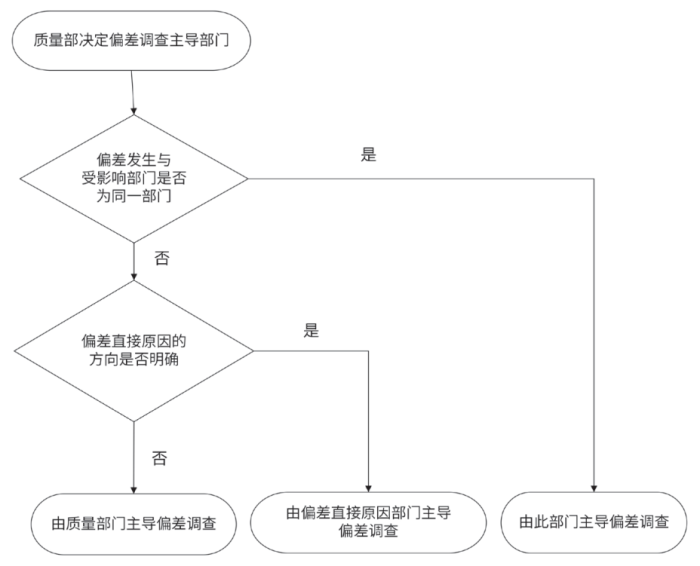
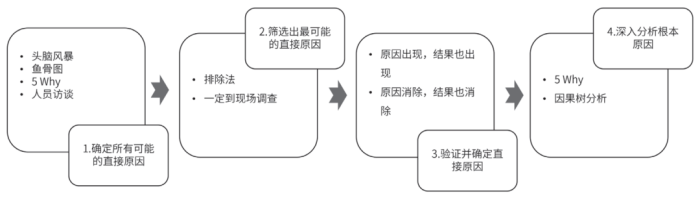
1.5
重复偏差管理的重点
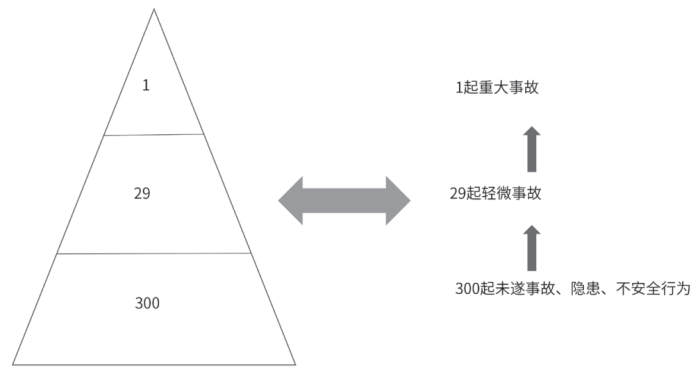
图3 海因里希安全法则
1.6
偏差的纠正措施与预防措施
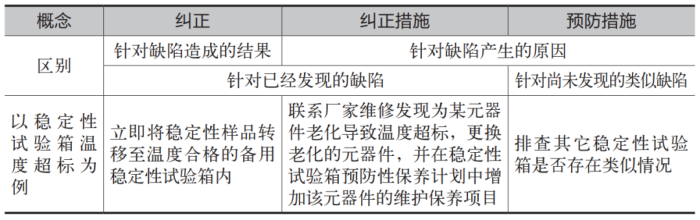
Part
2
Part
3
参考文献
[1] 中华人民共和国卫生部 . 药品生产质量管理规范(2010 年修订)[EB/OL].(2011-01-17),https://www.samr.gov.cn/zw/zfxxgk/fdzdgknr/bgt/art/2023/art_d5e1dbaa8f284277a5f6c3e2fc840d00.html.
[2]ICH.Q7 Good Manufacturing PracticeGuide for Active PharmaceuticalIngredients [EB/OL].(2015-06-10).https://database.ich.org/sites/default/files/Q7%20Guideline.pdf.
[3]PDA.Root Cause Investigations forCAPA: Clear and Simple[J](2020-06). https://www.pda.org/bookstore/product-detail/5724-capa.
[4]ISPE, PDA. Guide to ImprovingQuality Culture in PharmaceuticalManufacturing Facilities[J].2019.https://ispe.org/initiatives/regulatory/quality-culture.
撰稿人 | 郑文科、张磊
责任编辑 | 邵丽竹
审核人 | 何发
热点文章
-
一文搞定制药设备清洁验证分析方法的开发与验证
2024-03-12
-
偏差流程要点分析和偏差处理成熟度的考量
2024-02-29
-
工艺验证“连续三批”的含义?
2024-02-29
-
中美医药数据出境监管新规对生物医药企业国际化影响及合规建议
2024-03-18
-
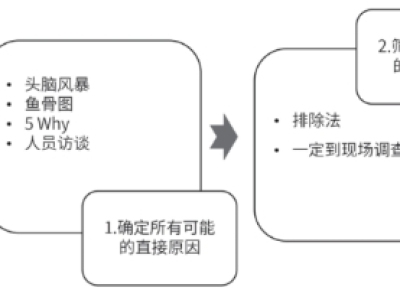
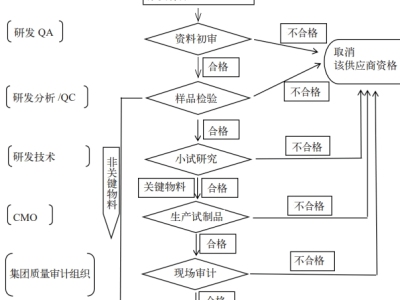
关于 B 证药品上市许可持有人供应商审计的思考
2024-03-01
-
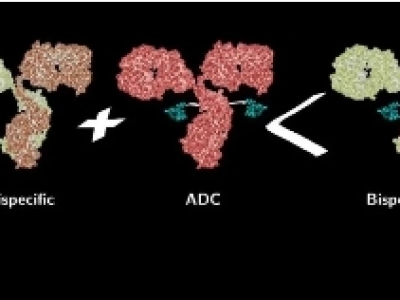
2024 AACR:中国双抗ADC们卷起来了?
2024-04-10
-
ADC药物市场爆发:年销售额破百亿,5款药物跻身10亿美元俱乐部
2024-02-23
-
数智赋能 质效双升 | 2024药品智能制造与质量控制技术交流会成功举办!
5月16日(第90届中国医药原料药/中间体/包装/设备交易会期间),“2024药品智能制造与质量控制技术交流会”在上海国家会展中心(上海)M103会议室顺利召开。本次会议由PharmaTEC制药业与国药励展联合主办,以“数智赋能·质效双升”为主题,邀请了来自产业链不同环节的8位专家,分享如何高效利用数字化、智能化及绿色化先进技术来赋能药品的研发与生产,助力制药行业朝向高质量发展。
作者:CICI
-
保证质量始终如一和生产稳定运行
-
预约报名,免费参会|药品智能制造与质量控制技术交流会(5月16日,上海)
-
紫外光谱检测自制熊果酸片剂的含量
-
一种提高醇沉沉渣排放速度的方法
-
收藏 | 统计方法在药品工艺验证中的应用










评论
加载更多