药品包材生产车间与流程管理
随着药品监管法规的不断更新,药品包材的管理也随之发生了重大变化——由过去的政府直接监管,变成了药品生产企业以供应商管理的形式对药品包材的质量进行管理。本文将以药品生产企业的视角,讲述对药品包材法规要求的理解、药品包材生产车间设计和质量管理的期望。
文/ 李瑸
本文作者就职于天津天士力圣特制药有限公司。
药品包材在中空制品行业中是一个非常细分的领域,其产品在中空制品全行业的占比微乎其微。但是由于其服务的最终产品的特殊性,药品包材具有注册管理要求高、法规监管要求高以及质量管理要求高的特点。从事中空制品行业的相关企业和即将从事药品包材生产的企业应对注册、法规和质量管理给予高度重视,合理有效地进行产品评估和企业质量管理。
1 药品包材法规概述
1.1 药品包材的定义与分类
药品包装是指选用适当的材料或容器、利用包装技术对药物制剂的半成品或成品进行分(灌)、封、装、贴签等操作,为药品提供品质保证、鉴定商标与说明的一种加工过程的总称。药品包装功能主要体现在3个方面,即保护功能、方便应用和商品宣传。
与药品包材相类似的产品还有医疗器械包材、化妆品和食品包材。由于其监管的要求各不相同,本文针对药品包材中对药品起保护作用的包装材料法规要求做详细介绍。
将药品包材按照与药品接触的关键程度进行分类,分为以下3类:
Ⅰ类药包材指直接接触药品且直接使用的药品包装用材料、容器,如HDPE瓶、PET瓶等。
Ⅱ类药包材指直接接触药品,但便于清洗,在实际使用过程中,经清洗后需要并可以消毒灭菌的药品包装用材料、容器,如西林瓶的胶塞。
Ⅲ类药包材指Ⅰ、Ⅱ类以外其他可能直接影响药品质量的药品包装用材料、容器,如西林瓶上的压盖。
1.2 药品法规的层级概述
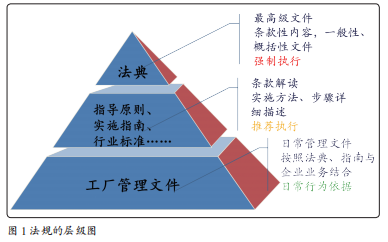
药品行业有着极高的法规符合性要求,药品法规、行业规范和企业的操作规程的层级关系如图1所示。法律法典在法规层级中属于最高级别的文件,其条款由于需要具有广泛适用性,所以法典性质的文件多数是条款性内容,描述概括性的、一般性的要求,但是法律和法典是强制要求执行的(例如,《中华人民共和国药品管理法》)。处于其下方中层分级的文件是一些指导原则、实施指南以及行业标准,这些文件会对某一专题内容讲述详细的实施方法,内容比法规法典更为详尽。这类文件虽然属于推荐而并非强制执行,但却是企业实践的主要参照标准和依据。最后一层分级也是数量最多的文件,大多属于企业日常管理文件和操作规程,这类文件依照法律法典、参照指导原则和实施指南具体制定,是评估企业日常行为的依据,需要具有企业的适应性。企业在制定自己的管理规程时,切忌照搬法规条款,无法落地执行。
1.3 药品包材适用法规
对于药品包材法规,最高层级的法典是药品管理法[1]。在执行层面,建议从两个方面研读药品包材适用的法规,一方面是药品包材注册路径的法规、实施细则、指导原则、标准等内容,另一方面是生产现场质量管理方面的要求。
1.3.1 药品包材注册法规
在药品包材注册法规方面,建议关注2020年7月1日新实施的《药品注册管理办法》[2],以及与之关联的《关于药包材药用辅料与药品关联审评审批有关事项的公告》(2016年第134号)。具体而言,自2018年1月1日起,不再颁发药用辅料和包材证书,取而代之的是登记制度和关联审评制度。新的药品包材企业需要通过与药品制剂生产企业关联产品注册,才能获得有效的药品包材注册。对于药品包材企业会有3种可能的状态:第一种,2017年12月31日前具有有效期内的包材登记证,并有药品生产企业在用,仍然可以继续延续使用,但如果该包材用于新的药品包装,仍然需要进行关联评审;第二种,2017年12月31日前未具有包材登记证的,后续在国家药品评审中心(CDE)取得登记号,但未与药品关联的,药品包材处于未激活状态,需要有药品完成关联评审后才能变为激活状态,在CDE网站上,已经登记的药品包材处于激活和未激活的状态均可以查询到;第三种,尚未具有药品包材登记号的,需要与药品共同完成关联评审,否则该药品包材不能使用。对于药品包材注册中,需要提交的资料要求,以及药包材需要遵照的标准,可以分别参考如下内容:
注册资料提交要求:《药包材及药用辅料申报资料要求》;
直接接触药品包装材料质量标准:中国食品药品检定研究院药包材标准(http://app.nifdc.org.cn/jianybz/jybzTwoGj.do?formAction=listYbc);
《中国药典》(2020版)药包材通则:药典国家药典委员会(https://www.chp.org.cn);
国家药品评审中心药品包材登记信息(http://www.cde.org.cn/yfb.do?method=main)。
1.3.2药品包材生产质量管理法规
在生产质量管理规范方面,企业需要了解2020年7月1日实施的《药品生产监督管理办法》[3],在此监督管理办法中,明确提出药品生产企业需对药品包装材料生产企业进行供应商管理,省级药监部门会根据监管情况,对药品包材企业进行日常监督检查,必要时进行延伸检查;省级药监部门每5年对药品包材企业进行一次检查。从法规变化中可以看出,药监部门已经不再对药用辅料、药用包材企业颁发GMP证书,管理责任变成了药品生产企业作为供应商管理,药监部门的检查由定期变为不定期的监督检查。
药品生产企业通常会按照药品生产质量管理规范的标准,期待供应商能够符合GMP管理水平。因此,在生产质量管理方面,药品包材生产企业与下游客户必须在质量管理的要求上达成共识。
2 药品包材车间设计简介
上文中讲述了药品包材的法规要求,值得注意的是,在药品包材的生产车间设计以及后续管理方面,都需要充分了解未来目标制剂产品的要求,进行合理的规划与设计。
2.1 洁净级别设计
首先应当对目标客户产品的洁净等级有所了解,再设计与之相匹配的药包材洁净生产区域。有关《药包材生产质量管理指南》(T/CNPPA 3005-2019)不同功能区域的洁净分区建议[4]见表1,可供参考。
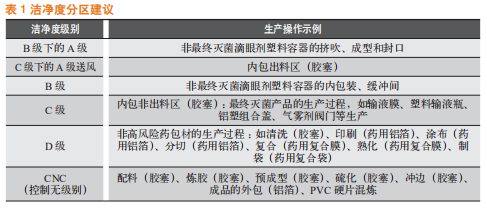
参考2010版GMP附录1无菌药品[5],和ISO14644洁净室及相关控制环境国际标准,各级洁净区的悬浮粒子与微生物标准见表2和表3。表2中还给出了洁净等级对应的ISO等级[6],对于已有洁净厂房的企业,可以参考对照。
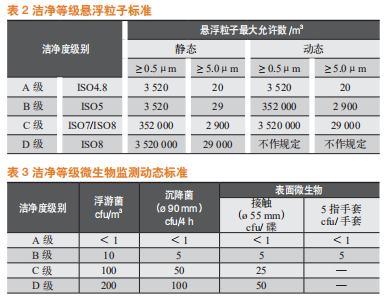
从表2和表3可以看出,洁净等级每提高一个等级则限度加严一个数量级,这意味着建造成本和运行成本也会呈数量级增长。因此,应避免洁净等级越高越好和洁净区越大越好的误区,充分分析客户产品所需洁净等级、生产工序所需洁净等级,合理设计洁净区域面积和洁净等级。
2.2 洁净厂房设计关注点
对于洁净厂房设计,有几个特殊点需要在洁净厂房设计之初予以考虑。
2.2.1 洁净分区
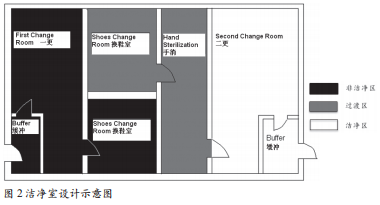
洁净分区除了考虑前文所述的合理的洁净等级设计外,还应考虑在不同洁净级别之间设计合理的缓冲或隔离区,以防止不同区域间的交叉污染,或低洁净级别区域对高洁净级别区域的污染。同时,还应考虑车间的出入口是否满足洁净分区的要求,以及“灰区”的设计。所谓的“灰区”就是无洁净级别区域到洁净区之间的过渡区域。这些区域按照洁净区设计、洁净区管理和监测,但是监测结果仅作为数据参考不进行标准判定。“灰区”的设计示意图如图2所示。图中换鞋室是一个房间,以翻转凳分隔非洁净区(黑区)和过渡区(灰区)。通过另外一个房间手消间起到缓冲间作用,保证了二次更衣室的洁净环境。
2.2.2 压差布局
在洁净区内,不同洁净级别区域的压差应大于10 Pa;相同洁净级别的不同房间,为避免交叉污染,压差应大于5 Pa。值得注意的是,在调节各区域压差时,要保证洁净室对外界大气压的正压。对于有不同洁净级别的厂房,要注意设计合理的压差梯度,以保证各级别区域间的压差满足上述的要求。在监测压差的区域,应安装压差表以动态监测压差;更为良好的实践是在压差表上粘贴合格刻度线,这样就可以随时判定压差是否合格。
2.2.3 人流与物流设计
在洁净区人流与物流的设计中,首先要考虑人流与物流的合理流向,例如,人流流向主要考虑人员更衣的合理性与便利性,以及人员在车间内行走的最优路线,并兼顾逃生的需要。物流流向主要考虑仓库与车间的物料交接(包括原材料、成品及废弃物),以及车间内部各工序间的物料转移最优路线。如果有条件的话,可以考虑人流与物流路线采用分开设计(如图3所示)。其次,在人流通道方面,应考虑设置足够的更衣区域,是否有二次更衣的需求,以避免人员带来的污染;在物流通道方面,要考虑不同洁净级别间物料的传递方式,是否需要建传递窗,以及传递窗的内部送风要求和合理的尺寸设计。最后,在人流通道与物流通道并行的区域,要考虑合理的空间设计和人员的安全因素。

2.2.4 虫害控制与地漏设计
虫害控制对于一般厂房来讲没有严格要求,而对于洁净厂房,首先应建立一套完整的虫害控制体系[7]。首先,根据厂房所处的地理位置和周边环境,判断虫害大致种类(如飞虫、爬虫、鼠害等)及虫害高发时间或季节。其次,根据分析结果和厂房布局,建立不同的虫害控制防线。在虫害高发季节,还应注意对与洁净区有关联的技术夹层的虫害控制,防止爬虫通过风口、灯罩等密封不严区域钻入洁净区。最后,日常虫害控制要定期回顾虫害发生情况数据,以及虫害控制装置设计的合理性。
在地漏设计方面,不同洁净等级的洁净室分别有不同的要求,与一般区域厂房的设计有所不同,这里需要注意的是,洁净区内不允许设计排水沟,具体要求见表4。

洁净厂房关于墙面、地面、照明、温湿度控制以及密封性具有特殊要求。有关洁净室设计与验收标准规范可以参见《医药工业洁净厂房设计标准》(GB 50457-2019)[8],《洁净室施工及验收规范》(GB 50591-2010)[9]。
3 药品包材生产质量管理简介
《药包材生产质量管理指南》(T/CNPPA 3005-2019)虽然是团体标准,但是该标准是将药品生产质量管理规范(GMP)、质量管理体系(ISO9000)和药品初包装材料生产质量管理规范(ISO15378)三者有机融合而建立的。事实上,ISO15378标准也是国际标准化组织将ISO9000标准与GMP规范结合后制定的。药品包材生产企业可以参照上述标准建立适用于自己企业的质量管理体系。在药包材生产质量管理指南的第2节术语和定义中,引入了GMP规范特有的术语,在第6~10节中主要介绍了GMP规范的要求。由于篇幅有限,本文仅对涉及药品包材质量管理的特殊的几个系统的要点与关注点进行阐述。
3.1 变更控制管理
在GMP规范下的质量管理体系中,变更控制管理是最重要的质量管理要求之一。所有对产品质量可能产生影响的变更都需要按照变更控制的要求进行记录和管理。变更控制的主要流程包括变更的发起、评估、行动项执行、通知、变更批准和变更后效果评估。变更发起阶段,识别可能对产品质量或者下游客户产品质量产生影响的变更,向公司的质量管理部门申请进行变更;变更执行前需要进行充分的风险评估,评估变更后可能带来的不良产品质量影响,必要时邀请客户参与变更评估。变更评估完成后,识别准备变更而进行的行动项,如文件的升级、工艺参数变化和图纸升版等,或由变更引发的测试、验证等工作。变更行动项完成之后,如涉及到对客户的产品质量影响,应将变更结果通知客户,并提交相关的测试、验证结果。由客户判定是否满足要求。如满足,与客户商定变更开始执行日期或供货日期。所有行动结束后,应将变更过程中执行行动项完成的证据以文件形式提交质量管理部门留存,作为变更控制的记录,并由质量管理部门批准变更执行。在变更执行后的一段时间内,应对变更效果进行评估,以判定变更是否对产品质量以及客户产品质量产生不良的影响。
3.2 偏差管理
各质量管理体系中,都要求进行偏差管理。在GMP的质量管理体系中,对偏差的闭环管理有更高的要求。首先,所有对产品质量产生影响的偏差都需要进行记录和根本原因调查;在进行根本原因调查的同时,需要对产品的放行进行判定。其次,在进行根本原因调查后,需要制定整改措施。这里要注意,一方面是纠正现有偏差,更重要的是预防类似根本原因的偏差再次发生。最后,也是最容易被忽略的就是定期要对偏差及其根本原因进行回顾。主要回顾预防纠正措施的有效性、偏差的重复发生率以及以往偏差调查根本原因的合理性。如果某种类型的偏差重复发生率相对较高,需要系统地对管理流程或设计进行回顾,并制定更为有效的预防纠正措施,将偏差管理形成闭环。另外,不建议将过多的偏差根本原因归结为人为原因,将培训作为唯一的预防纠正措施。这种方式仍然存在着偏差调查不彻底、预防纠正措施无效的风险,未来还有可能再次发生类似的偏差。
3.3 验证与确认
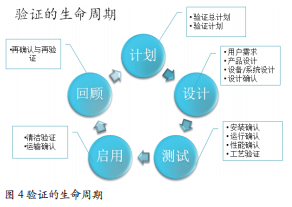
验证是要求证明操作规程(或方法)、生产工艺或系统能够达到预期结果的有文件证明的一系列活动。这是GMP管理中独有的要求,特点就是预先设定操作规程、测试方案和接受标准,进行测试后正式按照操作规程执行,可以持续地达到接受标准。这一过程需要进行完整的文件化记录。验证通常按照生命周期管理(如图4所示)的方式进行。根据系统的不同,可分为设备设施验证、计算机化系统验证、工艺验证、分析方法和分析仪器验证,所有对产品质量可能产生影响的系统均需要进行验证。GMP规范中规定,只有当系统完成必要的验证工作后,才可以用于商业化产品的生产和检验工作。由于验证涉及的内容较多是GMP实践中的一个专门话题,这里就不展开详述了。
3.4 操作规程的建立与过程记录
企业在制定标准操作规程、作业指导或工艺规程时,首先要有法规、指南或验证结果作为依据。同时,还要与日常操作的具体实际相结合,使得规程在合规的前提下具有可操作性。员工在执行过程中应严格按照文件规定进行操作,并将操作的过程进行完整如实的记录。企业的规程制定部门、管理部门应定期回顾这些规程文件的法规符合性和执行的有效性,同样形成闭环管理。
近几年,制药行业的一个热门话题就是记录的数据可靠性,归根结底就是要求数据的可追溯性、真实性、准确性、完整性和同步记录。这并不是新的要求,也不是过高的要求,只是要求一份记录能够把整个生产或检验过程完整如实地呈现出来。回归到最朴实的语言,如GMP规范的经典语录:写你所做的,做你所写的,记录你所做的。
综上所述,在GMP管理中更应强调受控管理、文件的可追溯性和闭环管理,这些是药品生产相关行业与其他行业质量管理体系相比要求相对较高的环节。
4 总结与展望
由于监管职责的转移,未来药品生产企业将更加关注原辅料及包材供应商的质量管理与监督,对供应商质量管理期望将日趋提升。可以预见,药品生产企业将比药监部门提出更为详细而具体的质量管理要求。建议药包材生产企业重点关注下游客户对包材质量控制要求,以质量源于设计的理念、体系流程化的管理保证产品质量的始终如一。
5 结束语
药品生产企业与药品包材生产企业共同担负着保障药品质量的责任,愿药品生产企业与药品包材企业携起手来,为广大患者提供安全有效、质量可控、用药可及的优质产品。
【参考文献】
[1] 全国人民代表大会常务委员会.中华人民共和国药品管理法[EB/OL].[2019-08-26].http://www.gov.cn/xinwen/2019-08/26/content_5424780.htm.
[2] 国家市场监督管理总局.药品注册管理办法[EB/OL].[2020-03-30].http://gkml.samr.gov.cn/nsjg/fgs/202003/t20200330_313670.html.
[3] 国家市场监督管理总局.药品生产监督管理办法.[EB/OL].[2020-03-30].http://www.gov.cn/xinwen/2019-08/26/content_5424780.htm.
[4] 中国医药包装协会.药包材生产管理质量指南:T/CNPPA3005-2019[EB/OL].[2019-05-08].http://www.cnppa.org/index.php/Home/Bz/show_2019/id/992.html.
[5] 中华人民共和国卫生部.药品生产质量管理规范(2010年修订)[EB/OL].[2011-01-17].http://www.gov.cn/gongbao/content/2011/content_1907093.htm.
[6] 国际标准化组织.洁净室及相关控制环境国际标准:ISO14644-2015[S].[2015-12-15].
[7] 国际标准化组织.药品初包装生产质量管理规范:ISO15378-2017[S].[2017-09].
[8] 中华人民共和国住房和城乡建设部.医药工业洁净厂房设计标准:GB 50457-2019[S].[2019-12-01].
[9] 中华人民共和国住房和城乡建设部.洁净室施工及验收规范:GB 50591-2010[S].[2010-07-15].






