生物制药工艺中“浸出物的命运”
一次性使用系统(SUS)在生物制药生产中被广泛应用——这些聚合物材料中的化合物可能会在不同阶段以浸出物形式进入生产过程中,可能会影响生产工艺效率(例如抑制细胞生长),或者成为工艺相关的药品杂质,从而潜在影响药品质量及患者安全。
目前,浸出物的研究主要集中于在“最差条件”或模拟情况下检测和评估单个组件的可提取物,并外推至工艺条件下的潜在浸出物。简单来说,“最差条件”和模型溶剂下,将可提取物数据进行累加来“预测”单个工艺单元或整个工艺中的SUS浸出物。按照这种思路,“最差条件”下“预测”在最终药品中的浸出物种类更多,浓度更高。然而,实际浸出物检测结果则与上述“预测”情况明显相反:实际工艺条件下检测到的浸出物并不会明显影响药品的纯度。
为更好地理解动态工艺乃至成品制剂中浸出物的范围和浓度,我们针对“浸出物的命运”这一概念提出了一个范式转换。基于物理-化学机理,按来源、分布和下降来描述“浸出物的命运”。
动态工艺条件下浸出物的来源,可根据菲克第二扩散定律和聚合物-基质界面质量传递(“通量”)来描述。根据这一模型,可以预测浸出物的动力学和最终平衡浓度。
任何生物制药工艺中,吸附和洗脱工艺显著影响着浸出物水平,如下游过滤、分离和纯化步骤。考虑到吸附的可逆性,特别是那些去除吸附物的工艺步骤,可作为浸出物“消失的终点”。
可以想象,一次性生物反应袋的浸出物吸附在宿主细胞表面和细胞碎片上。在收获步骤中去除宿主细胞和细胞碎片,也可去除吸附的浸出物,只有真正溶解的浸出物保留在工艺中。
之前我们能够证明在纯化步骤中过滤和膜吸附设备中的滤膜能够非常有效地清除浸出物。典型物质的清除能力,以µg/cm2膜表面积或µg/cm3膜吸附柱床体积进行衡量。
Magarian等人介绍了一项使用UF/DF清除浸出物的研究。他们证明通过渗透的方式清除浸出物,符合传统UF/DF机制。除此之外,生产过程中更多的工艺步骤可以降低浸出物含量。在进行离子交换或亲合层析时,洗脱溶液可去除浸出物。对于吸附组分来说,层析分离也是浸出物下降的一种方式。
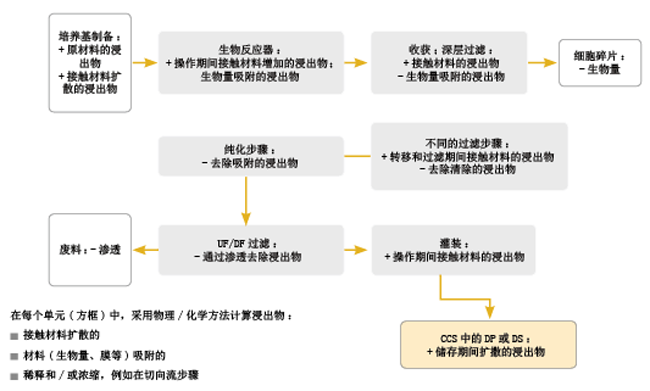
图1假定生物制药下游生产中后续工艺步骤的动态单元模型
为了实现浸出物的来源、分布和下降的可计算化,只需综合考虑它们,并计算各工艺步骤和整个下游生产中的“浸出物的命运”。图1显示的是一个用于计算假定工艺中浸出物含量的动态单元模型。该模型将工艺步骤和/或工艺设备视为独立单元,将其结合起来模拟整个工艺。在每个单元中,根据基本物理-化学机理计算浸出物的来源、分布和下降。采用物料平衡条件,各单元之间的交换或排放采用液相流动模拟。
工艺单元的输入数据包括:溶液的总体积,聚合物相的总质量,聚合物的厚度和表面积,聚合物中浸出物的原始量m0,一次性生物反应袋中的生物量,吸附剂的质量和/或表面积,以及UF/DF步骤中的透析体积。浸出物要求的输入数据包括:聚合物的扩散常数(D),聚合物和溶液之间的分配系数(KP/L),生物量和溶液之间的分配系数(KD-bio),过滤器和纯化设备的比容量(Kapfilter)以及UF/DF因子(z)。
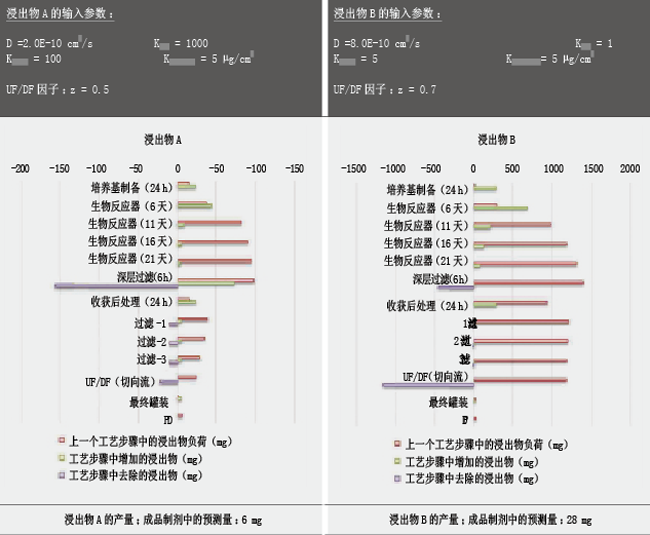
表1:浸出物A和B的输入参数概述;不同单元中A和B的计算量及制剂(DP)中A和B的最终含量
表1显示了图1中两种假定化合物A和B的单元模型计算结果。浸出物A的物理-化学参数(表1)可描述为类似于如二叔丁基苯酚异构体的添加剂降解产物,浸出物B类似于己内酰胺。对于两种化合物,我们假定它们在原材料中就存在(从包装容器中浸出),在培养基制备阶段从接触材料中迁移(混合并储存24 h)。对于浸出物A和B,可观察到一次性生物反应袋中培养基内浓度在21天内升高(图示红线);在这一时期内一次性生物反应袋聚合物材料迁移出的浸出物A和B的量逐渐降低(图示绿线)。由于浸出物A有被生物量吸附的倾向,通过分离细胞碎片能够将其从工艺中清除(图示蓝线)。这一作用对于浸出物B而言明显较弱,这是因为其水溶性好,生物量吸附的倾向较低。在工艺溶液后续处理和24 h储存阶段,工艺溶液中两种浸出物的量均增加。过滤工艺能够通过滤膜去除一部分浸出物A和B。
下列使用UF/DF步骤能够非常有效地清除浸出物B,且效率高于浸出A。浸出物A的z值较低,因此保留在回流端中的倾向更高,而浸出物B的z值为0.7,能够更有效地通过渗透从工艺中清除。对于浸出物A和B,尽管在原材料中已经存在,并在生产过程中不断从接触材料中迁移出来,不同下游工艺步骤的结合可将终产品中浸出物的含量明显降低。总之,下游生产的目的是“纯化”产品,能够像对其他不需要的工艺杂质一样有效清除可能存在的浸出物。此外,计算结果显示,“靠近”患者的概念作为常用的风险评估方法是合理的,且可通过我们的模型计算得到支持。
尽管此处预测整体工艺中浸出物的方法是基于数学模型计算,其结果能够反映实际浸出物情况明显优于“最差条件”下累加的情况。通过模型计算证明,尽管浸出物有多种来源,在生物制药工艺中浸出物的下降具有重要的意义,在浸出物(风险)评估中需要考虑进去。
赛多利斯技术团队已经开始进一步研究完善模型单元,以包含可能的浸出物反应,尤其是潜在的浸出物-蛋白质相互作用。模型经优化和微调后,需通过比较模型结果与中试或生产规模的实际测量值来进一步验证。
赛多利斯验证服务团队是可提取物和浸出物研究的先行者,已经提供了20多年的分析测试和法规技术支持。赛多利斯提供最精准的现行法规要求和行业标准解读,与客户协作以满足法规预期,并基于客户的实际工艺条件,为其药品配方确定适当的可提取物和浸出物方案设计。
文/ Armin Hauk博士,Ina Pahl,Roberto Menzel,Samuel Dorey,Isabelle Uettwiller博士
【参考文献】
Hauk A., Pahl I, Menzel R., Dorey S and Uettwiller I.: On the Fate of Leachables: An Introduction of a Concept to Investigate Leachables with a “Holistic” or System Approach; ECI Conference, Tomar Portugal, 8th -10th May.2017
Hauk A.: On the “Fate of Leachables” in Biopharmaceutical Up-Stream and Down-Stream Processes; Vonlanthen E&L-Summit, 19th October 2017, Berlin
Magarian N., Lee K., Nagpal K., Skidmore K. and Mahajan E.: Clearance of Extractables and Leachables from Single Use technology via Ultrafiltration/Diafiltration; AIChE Publication, 2016







加载更多