多方博弈:突破中国式研发困境
“有些时候,我们明明坐着最大的双引擎波音777,但是它延误一直不飞,我们也没有办法。”谈及中国药品创新研发的滞缓,中国医药创新促进会执行会长宋瑞霖这样比喻。的确,与其他新兴市场相比,中国在创新投入和产出上都处于领先位置。然而,在医药研发创新贡献的世界排名中,中国却处于第三梯队。
从表面上看,药物创新只是个技术和经济命题,实际上极为复杂。其涉及的利益相关方包括企业、监管机构、医生、患者等。目前,中国在多项医药创新指标中已显现出强劲的增长势头,特别是顶级期刊文章数、药物专利申请数和在研化合物数量上,但仍有其独特的创新困境。
【药企】难!投资回报率日益下降
创新药研发回报率日益下降是一个全球普遍存在的难题。根据美国药品研发与制造协会(PhRMA)的数据,包含研发失败的情形在内,如今一个新药的平均研发费用已经达到12亿美元。与研发成本快速增长的趋势相比,新药研发回报率却已跌至40年以来的最低谷。2013年,百时美施贵宝研发支出经济回报率为15%,罗氏为7.7%,强生为8.2%,辉瑞为-3.2%,阿斯利康为3.9%,默沙东为3.0%。与此相比,新基医药和吉利德相对较高,分别达到32.3%和20.8%。
对于中国原研药企来说,除了注册审批耗时长,新药纳入医保和基药目录也比较困难。目前主要自主创新药都未进入基药目录,进入医保的仅有13只,其中4只进入省级医保。
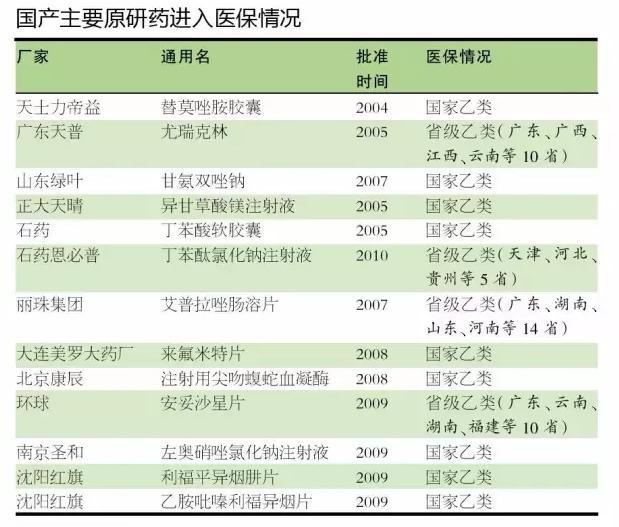
此外,新药进入临床治疗指南时间也长。非小细胞肺癌美国原研药ceritinib去年5月31日上市以后,只花了不到一周的时间就进入《NCCN临床实践指南》;而中国新药埃克替尼竟花了接近3年时间才进入《晚期非小细胞肺癌分子靶向治疗专家共识》。

与时间赛跑:结合多层面营销手段
“在研发费用越来越高,新药发现越来越难的背景下,时间要素成为左右新药利润产出的钥匙。新药在自身生命周期与巨大利润期待的对峙中艰难挣扎。”上海复星医药集团副总裁兼研发中心主任邵颖对记者说。
新药从研发到获得医保投入,德国平均需要12年的回报时间,美国、法国、日本也大多超过10年,而中国则逼近化合物专利保护期的20年。为争取更高销量,美国一些原研药企曾与印度仿制药企谈判,前者支付一定费用以后,后者延缓仿制药上市时间。
吉利德的Sovaldi堪称“重磅炸弹”中的传奇。2014年,Sovaldi为吉利德创造了100亿美元的销售额,战胜了长居榜首的辉瑞。Sovaldi的价值与利润传奇主要归因于多层面营销手段的结合。吉利德从药物经济学角度,阐述“拥有较高的治疗成本效用的高价Sovaldi,反而能够为患者节省总体成本”的道理,其不断公示药品的高治愈率数据。这些手段是值得国内创新药企借鉴的。
提高研发效率:精准医疗中国style
美国总统奥巴马提出的“精准医疗”,是基于个体基因、环境以及生活方式等信息而进行的疾病预防和治疗的新兴医疗手段。“一旦推广应用,其将极大提高新药研发效率,为企业研发节省很多时间,个性化的药物也将拥有更好的治疗效果。”沃森生物副总裁兼研发总监周新华对记者说。
今年3月科技部召开的“国家首次精准医学战略专家会议”敲定,在2030年前,中国精准医疗将投入600亿元。不久前,卫计委印发《药物代谢酶和药物作用靶点基因检测技术指南》和《肿瘤个体化治疗检测技术指南》两大指南,指出药物基因组学已成为指导临床个体化用药、评估严重药物不良反应发生风险、指导新药研发和评价新药的重要工具;肿瘤个体化治疗基因检测已在临床广泛应用,实现肿瘤个体化用药基因检测标准化和规范化,是意义重大的紧迫任务。
在业内人士看来,两大指南将加速精准医疗、基因检测发展,中国版“精准医疗”正在加速落地兑现。
【政策】支持创新借鉴他山之石
针对现实情况,尝试专利延长、增补资源、分级管理等
“我国药物创新发展政策壁垒,主要体现在新药注册审批周期、知识产权制度尚待完善、创新药物市场准入(如招标、医保等)时间长、对药物创新的财税激励不够。”宋瑞霖认为,这些因素导致新药上市后往往销售增长缓慢。
由于医保目录更新较慢,以及集中采购的延迟,中国创新药品往往上市后几年都没有医保报销,这已成为关键性障碍。
宋瑞霖表示,并非现行政策制定不够先进,当下的主要问题是政策不配套。
2009年出台的《改革药品和医疗服务价格形成机制的意见》早已提出对新药定价引入药物经济学评价方法,开放自主定价,并允许创新企业在合理期限内保持较高销售利润,也鼓励医保经办机构、医疗机构和药品供应商进行谈判协商确定医药费用及付费方式。
化合物的专利保护期为20年,而从化合物发现到临床试验结束再到申请上市,一只新药平均就已耗时12~15年,缺少符合条件的药品专利延长的相关制度。尽管允许创新企业保持较高利润,其药品上市后所剩的专利保护期已经不多,加上医保支付障碍严重掣肘推广销售,限制了新药的销售盈利。
在这个方面,欧美国家规定最多可获得5年的专利延长期。
应8月18日国务院刚出台的《关于改革药品医疗器械审评审批制度的意见》要求,药品审评中心CDE随即发布《国家食品药品监督管理总局药品审评中心审评员管理暂行办法(试行)》,拟在编制内外增招审评审批技术人员并规范管理(目前药审中心编制不到200人,远低于美国的2000人和欧盟的4000人)。除此之外,有专家建议采取分级管理,将重复申报的药品交由省级药监部门或区域性审评中心,或能较大幅度降低申报挤压问题。
【社会】PBM大发展的必要条件
作为第三方因素,PBM有望改变政府与药企的传统二元博弈格局
社会这一因素往往被忽视,而其拥有的强大力量可能改变政府与药企的传统二元博弈格局。例如,社会舆论压力可起到倒逼政策的作用,社会融资能激励创新,一些社会研究机构的卫生技术评估系统可全面评价新药的技术特性、临床安全性、有效性、经济学特性和社会适应性等,从而起到加快审批进度、为新药定价提供参考意见的作用。
近十年来,全球医药市场以年均10%左右的速度递增规模,不断增长的药品市场需求使各国支付医疗保险费用的负担逐渐加大。各国政府大多对药品价格进行了一定的控制,以保证药品的可负担性,其中美国采取的就是价格谈判方式。
对于药价的控制,在政府与药企的博弈中,若引入第三方社会机构,在政府的监管下与企业、医保机构进行多方谈判,在理想的状态下,对新药价值的传递有提高的作用,进而提高研发效率。
美国PBM运作特点
由于美国商业医保覆盖率较高,其医保制度以自由市场型为主导,于是催生了药品福利管理公司(PBM)这种控制专利药品医保费用的中介角色,在保险机构、制药公司、医院和药房间进行管理协调。
面对巨大的销量保证,企业往往愿意提供折扣将药品纳入PBM的处方集目录中;而由于保险机构拥有较为强大的买方力量,往往能以高销量为筹码压低价格,其较低药价利好必然会吸引更多参保者。
美国PBM巨头之一快捷药方(Express Scripts)数据库拥有大量病人的保单历史和医疗机构的诊疗历史数据,医院新开具的处方和药店销售药品的记录实时回传到数据库中进行匹配审核,一旦出现药品错用或滥用等情况,会立刻进行弹窗提示,以达到费用管控的目的。
中国PBM可行性探讨
“他山之石”或能给中国医保费用控制一点借鉴。然而,中国目前基本医疗制度仍覆盖广、浪费大、监管效率低,医药分开也处于初级阶段,患者购买处方新药仍依赖于医生,药品零售连锁信息化也才在近两年刚刚伴随医药电商的推广而兴起。
尽管种种因素对于发展PBM业务不利,但仍有敢于抢先“吃螃蟹”的企业。
海虹控股集团从2009年开始与快捷药方合作成立PBM公司“益虹”,是国内最早发力该业务的企业。如今其业务试点覆盖全国18省市约100个地市。有分析师测算,目前杭州地区每年医保报销额为100多亿元,海虹的PBM系统纠错率约为6%,仅试点的杭州地区,一年就可减少医保支付近10亿元。
不少业内专家认为,在医药分开达到较高程度的时候,PBM模式将得到快速发展。但是,在其能够成熟运行之前,还有几个必要条件。
首先,PBM自身应保证有较高的新药使用评估专业水平;其次,应联合卫生和药监机构通过评估新药有效性、安全性等,建立起符合国情的新药处方集目录,为新药的推广使用提供一定的保障,引导患者更实惠合理地使用新药,降低药企盈利风险。此外,监管机构应加强医疗服务行业的监督,对PBM企业有针对性地制定监督措施,强化立法与执行力度,建立信息公开机制。






