文字目录
-

国内新闻-2024制药业第一期
2024年1月2日,药明巨诺宣布与2seventy bio达成独家战略合作,开发自身免疫疾病CAR-T治疗产品;近日,康华生物与HilleVax签署重组六价诺如病毒疫苗许可协议,授权HilleVax在除中国以外地区对重组六价诺如病毒疫苗及其衍生物进行开发、生产与商业化;1月25日,复宏汉霖完成H药,斯鲁利单抗首批海外发货;1月30日,国家药典委公示了吹灌封(BFS)技术的无菌药品包装系统质量控制指导原则标准草案;1月8日,药明康德宣布其位于江苏常州及泰兴两个基地的多肽生产车间正式投产。
-

国际新闻-2024制药业第一期
2024年1月8日,百奥赛图宣布与Radiance Biopharma达成双抗ADC协议;1月24日,FDA发布了两篇针对仿制药申请人的定稿指南,旨在简化上市前审评和批准程序;1月31日,药明生物宣布其生物药原液生产七厂(MFG7)已成功完成首批1.6万升生产;1月16日,Epitomee宣布已成功完成减肥胶囊的 RESET 关键性临床试验;1月12日,丹纳赫与Jennifer Doudna及其创办的创新基因组学研究所(IGI)合作启动CRISPR 项目,致力于开发CRISPR基因编辑解决方案。
-

新技术开发-2024制药业第一期
2024年1月1日,Eppendorf中国宣布即日起正式开始销售Himac品牌旗下全系列离心机产品线;1月2日,君实生物宣布,其自主研发的抗PD-1单抗药物特瑞普利单抗注射液获批用于肺癌围手术期疗法;1月17日,药明生物宣布其双特异性抗体技术平台WuXiBody获得了美国专利商标局授权;2月8日,全新机制抗病毒药物马立巴韦片在中国开出首张处方;2月7日,信达生物制药集团宣布玛仕度肽的首个新药上市申请(NDA)已获CDE受理。
-

一致性评价对国产替米沙坦片质量的影响
随着一致性评价工作的全面展开,相关技术指导原则和质量标准的不断完善,制药行业快速发展,业内对药品质量的研究也更为深入和全面。替米沙坦片作为仿制降压药,在过去十几年,历经不断的质量研究和提升,从溶出度符合限度、溶出曲线与原研制剂相似,发展到生物等效,这是质的飞跃。也侧面反映了我国医药行业的进步和国产药的质量提升。
-

创新赋能行业,聚力共赢未来
用创新赋能行业,以合作带来共赢。2023 年 12 月 11 日,2023(第十五届)弗戈制药工程国际论坛在江苏南京嘉悦 · 印湖酒店召开。本届论坛由机械工业信息研究院 PharmaTEC 制药业主办,围绕“创新赋能 聚力共赢”的主题,邀请了来自制药行业的相关领导、专家学者、行业翘楚齐聚南京,共同探讨制药企业多元化创新发展之路,为我国制药行业的高质量可持续发展集结智慧、贡献力量。
-

坚守初心二十载 携手逐梦再出发
2023 年 12 月 11 日,PharmaTEC 制药业在 2023(第十五届)弗戈制药工程国际论坛上隆重举办了PharmaTEC制药业项目成立20周年庆典活动,与制药行业国内外合作伙伴共同回顾了20年来携手成长、共赢发展的历程,并探讨和展望了制药行业的未来发展之路。庆典活动上,PharmaTEC 制药业还重磅揭晓了制药行业评选结果,旨在塑造最具影响力的产业品牌,评选出为中国制药业发展做出杰出贡献的卓越企业和人物,为全社会树立学习优秀创新标杆的行业样板,为企业家的服务创新精神书写精彩篇章。
-
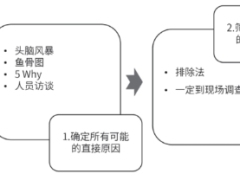
偏差流程要点分析和偏差处理成熟度的考量
本文介绍了偏差处理在制药行业应用过程中的一些重点和难点事项。偏差处理流程一般包括偏差的发现与报告、偏差分类、偏差的根本原因调查、建立纠正措施与预防措施。对此,本文推荐了一个选择偏差调查主导部门的决策树,并推荐了一种偏差根本原因分析的四步法,指出当发生重复偏差时重点应调查为什么偏差会重复发生。制药企业预提高纠正措施与预防措施的有效性,需少采用被动防错手段,多采用主动防错手段。提升偏差处理成熟度是每个制药企业提升的方向,这需要整个企业全体员工一起努力,提升企业质量文化,设置与偏差处理相关的绩效指标,促进企业持续发展。
-
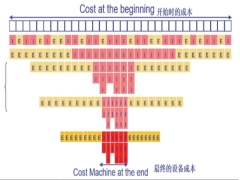
精益管理工具“快速换模 SMED”简述
2021 年 9 月 29 日,国务院办公厅印发《“十四五”全民医疗保障规划》,其中最引人注目的指标是:2025 年国家和省级药品集采品种达 500 个以上、高值医用耗材集采品种数量达 5 类以上;公立医院通过省级集采平台采购品种金额占比达 90%、高值耗材采购金额占比达 80%。“国采”将进一步推进。随着越来越多的企业优选入国采,如何通过科学的精益管理逻辑来持续确保企业始终保持高质量、高效率、低成本成长,紧跟国家脚步?本文通过精益工作坊的案例,对精益工具 SMED 的应用进行了介绍,希望能帮助行业同仁更好地理解精益管理中持续改善的思考逻辑。
-
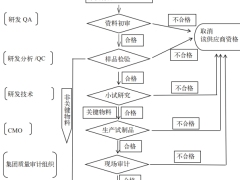
关于 B 证药品上市许可持有人供应商审计的思考
本文从目前国内法规对供应商管理及审计的要求入手,基于行业现状分析了当下 B 证企业在供应商审计中存在的风险和困难,提出了相应的风险控制措施思考,为当前 B 证药品上市许可持有人进行供应商审计提供了借鉴方法。本文提出,B 证企业应从人员技术水平、质量体系建设等方面夯实自身质量管理能力,结合当下新型的远程审计、集团共享审计结果、第三方审计等模式,在供应商管理中真正发挥主导作用,这样才能有望降低物料质量风险,确保生产出符合监管和注册要求的、安全有效且质量可控的药品。
-
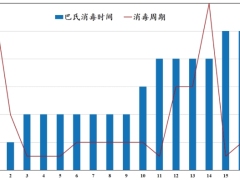
非最终灭菌无菌制剂的污染控制策略
2022 年 8 月 22 日,欧盟正式发布了 EU GMP 附录 1《无菌药品生产》,其强调应在整个设施内实施污染控制策略(Contamination Control Strategy,CCS)以确定所有关键控制点,并评估用于管理医药产品质量和安全风险的所有控制(设计、程序、技术和组织机构)和监测措施的有效性。应积极审核并酌情更新 CCS,并应推动生产和控制方法的持续改进。本文从人、机、料、法、环全方位出发,用思维导图梳理了产品污染的潜在风险,为实际工作中 CCS 的撰写提供了参考。
-
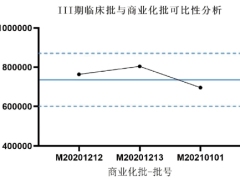
基于“以患者为中心”的疫苗药学研究策略
随着“以患者为中心”的研发理念逐步成熟,依托于创新技术的疫苗药学研究策略也在不断升级。本文聚焦于疫苗产品有效性评价的痛点开展分析,具有免疫原性替代终点的成熟疫苗远远少于当前在研疫苗数量,研发过程更应加强过程控制,在难以避免的研发变更中基于质量可比要求有效评估关键质量属性,实现每一道生产工序工艺质量可比,以此优化研究策略。
-

计算机系统在制药行业追溯体系应用中存在的问题与解决措施
本文对药品追溯体系中计算机系统应用的发展现状和存在的问题进行了详细的分析,针对现存的数据安全、兼容性、操作复杂性以及技术更新难等问题,提出了加强数据安全防护、优化系统设计、简化操作流程以及持续关注和适应技术发展等切实可行的解决策略,为进一步提升计算机系统在制药行业的科学化和精准化应用水平,提供了参考依据。
-
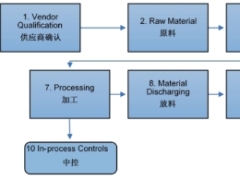
论计算机化系统和数据完整性
计算机化系统在制药行业的广泛应用,为生产、质量控制和合规性提供了重要支持。本文将探讨制药行业中计算机化系统与数据完整性的关系,相互之间的应用,如何基于系统功能、流程结合、配置和组态、数据流管理等方面的规划设计出符合数据完整性要求的计算机化系统。希望这能有助于避免行业内的教条式应用和学步邯郸。
-
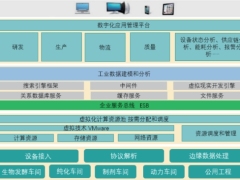
“5G+工业互联网”在制药行业中的应用探索
本文首先简单介绍了 5G 技术和工业互联网技术的技术特点和应用架构;其次,将制药行业的特点和“5G+ 工业互联网”的特点相结合,提出了制药智能制造工业互联网架构,并深度地论述了其架构的特点和该架构在制药行业中应用的典型场景,以及在实际应用实践中需要解决的相关问题;最后,根据理论和实践应用探索,探讨如何实现“5G+ 工业互联网”在制药行业的应用,从而促进制药生产过程的数字化、智能化和自动化,提升行业的竞争力。
-
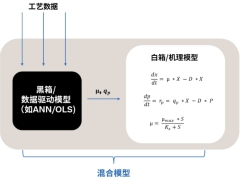
缩短生物工艺开发时间并提高效率,释放混合建模和工艺强化的力量
许多制药公司正面临着缩短工艺开发时间和高效优化工艺的挑战,希望以更快的方式将产品推向市场。本文介绍了一种动态建模方法,通过利用工艺强化技术来简化实验,并将其与混合模型得出的直观结果相结合,可以减少实验次数,有助于开创生物制品工艺快速且高效开发的新时代。
-

精准清洁
市场对压片工具的要求正在不断提高。据菲特高级产品经理 Carmen Ackermann 所述,压片机的冲头、分段中模必须能够承受巨大的载荷,并且易于更换和清洁,符合高卫生标准。菲特在德国施瓦岑贝克(Schwarzenbek)生产了许多压片工具,能够充分满足此类需求。此外,在整个产品生命周期中做好这些工具的维护也很重要。为了确保压片工具的长期耐用性和性能,一家制药化工公司选购了EasyCare 清洁系统。
-

商务信息港 产品推荐-2024制药业第一期
本期产品推荐汇集了岛津的实验室网络化数据管理系统LabSolutions CS、格律克的GMS紧凑型混合机、东富龙的PBS平行生物反应器、Romaco Tecpharm用于片剂包衣机的能量回收系统、ILC Dover公司的活性粉体转移系统DoverPac




































































